Pytanie 1
W kolbie o pojemności 250 cm3 stworzono roztwór zawierający 1,4025 g KOH. Jaką wartość pH powinien mieć otrzymany roztwór?
MKOH = 56,1 g/mol
Wynik: 19/40 punktów (47,5%)
Wymagane minimum: 20 punktów (50%)
W kolbie o pojemności 250 cm3 stworzono roztwór zawierający 1,4025 g KOH. Jaką wartość pH powinien mieć otrzymany roztwór?
MKOH = 56,1 g/mol
W celu oceny jakości masła wykonano oznaczenie liczby kwasowej LK, liczby zmydlania LZ i liczby nadtlenkowej LOO. Wyniki zapisano w tabeli.
Wartość liczby estrowej LE w badanym maśle wynosi
| Liczba | Wartość zmierzona |
|---|---|
| LZ | 196,8 mg KOH/1g |
| LK | 1,2 mg KOH/1g |
| LE | ? |
| LOO | 4,25 milirównoważnika aktywnego tlenu/ kg |
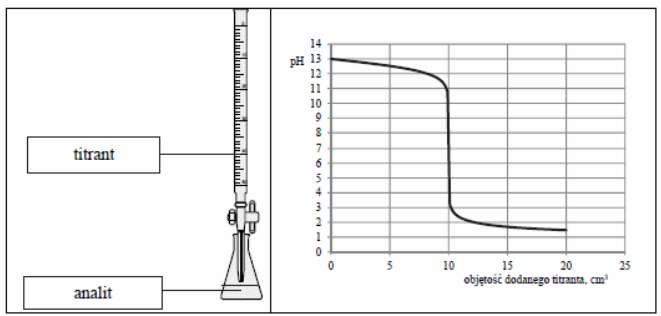
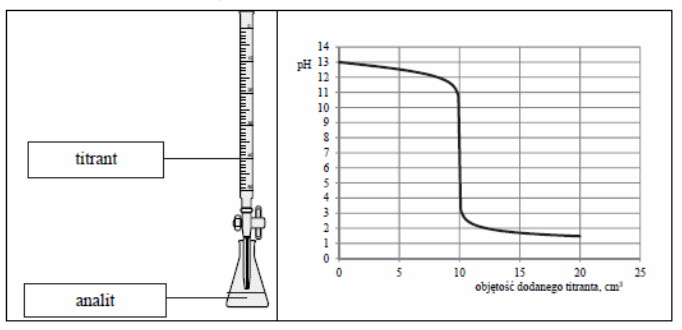
Z rysunku wynika, że analitem jest roztwór
Substancja chemiczna o najwyższym poziomie czystości nazywana jest
Podczas elektrolizy wodnego roztworu kwasu solnego na katodzie zachodzi reakcja opisana równaniem
| A. | 2 H2O + 2e− → H2 + 2 OH− |
| B. | 2 H2O + 4e− → 4H+ + O2 |
| C. | 2 Cl− → Cl2 + 2e− |
| D. | 2 H+ + 2e− → H2 |
Który zbiór zawiera jedynie odczynniki grupowe używane w analizie jakościowej jonów?
Maksymalne dopuszczalne poziomy dozwolonych substancji dodatkowych stosowanych w wybranych środkach spożywczych. W próbkach dżemów A, B, C, D oznaczono zawartość substancji dodatkowych. Na podstawie wyników przeprowadzonej analizy, wskaż próbkę dżemu, która nie spełnia podanych wymagań.
| Numer wg systemu oznaczeń Unii Europejskiej | Nazwa | Środek spożywczy | Maksymalny poziom mg/kg |
|---|---|---|---|
| E 210 E 211 | Kwas benzoesowy Benzoesan sodu | Niskocukrowe dżemy, galaretki, marmolady i podobne produkty niskokaloryczne lub bez dodatku cukru i inne produkty smarowne na bazie owoców. | 500 |
| E 220 | Dwutlenek siarki | Dżemy, galaretki, marmolady i podobne produkty smarowne łącznie z produktami niskokalorycznymi. | 50 |
| E 104 | Żółcień chinolinowa | 100 | |
| E 961 | Neotam | Dżemy, galaretki owocowe i marmolady. | 32 |
| Wyniki przeprowadzonej analizy | ||||
|---|---|---|---|---|
| Numer wg systemu oznaczeń Unii Europejskiej | Oznaczona ilość mg/kg | |||
| A. | B. | C. | D. | |
| E 104 | 65,2 | 58,5 | 74,8 | 57,5 |
| E 210 | 458,5 | 498,7 | 487,0 | 423,8 |
| E 220 | 38,0 | 47,8 | 52,0 | 25,0 |
| E 961 | 3,5 | 25,9 | 32,7 | 16,9 |
Wśród substancji konserwujących stosowanych w żywności występują CH3COONH4 (E 264) oraz C6H5COONa (E 211). Związki te można określić jako
Na rysunku przedstawiono aparat, za pomocą którego można oznaczyć
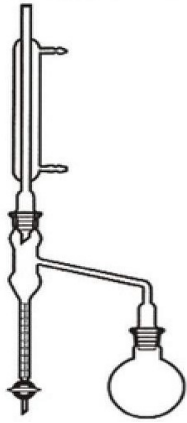
Jaką metodą oznacza się kwas solny w analizie miareczkowej?
Na podstawie informacji zamieszczonych w tabeli wskaż nazwę badanego związku.
| Dodany odczynnik | Obserwacje |
|---|---|
| Cu(OH)₂ | Zawiesina Cu(OH)₂ rozpuściła się, a roztwór przyjął szafirową barwę |
| Cu(OH)₂ | Po ogrzaniu probówki pojawił się ceglastoczerwony osad |
| [Ag(NH₃)₂]⁺ | Na ściankach probówki pojawiło się srebro metaliczne |
Które równanie przedstawia reakcję wytrącania osadu?
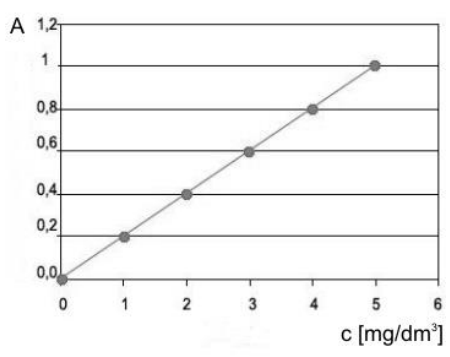
Korzystając z krzywej wzorcowej, określ stężenie badanej próbki, jeżeli absorbancja wynosi 0,6.
Ogólna twardość próbki wody stosowanej w technologiach wynosi 16,5°n, a twardość węglanowa osiąga 7,2°n. Jaką wartość ma twardość stała?
W badanym powietrzu zawartość mikroorganizmów wyniosła 33,33 w 10 dm3. Zgodnie z zamieszczonymi normami powietrze takie uważa się za
| Stopień zanieczyszczenia | Ogólna liczba bakterii w 1 m3 |
|---|---|
| Niezanieczyszczone | poniżej 1000 |
| Średnio zanieczyszczone | od 1000 do 3000 |
| Silnie zanieczyszczone | powyżej 3000 |
Działanie, które ma na celu określenie relacji pomiędzy wartościami mierzonymi dla wzorcowych próbek a odczytami systemu pomiarowego, realizowane w specyficznych warunkach, to
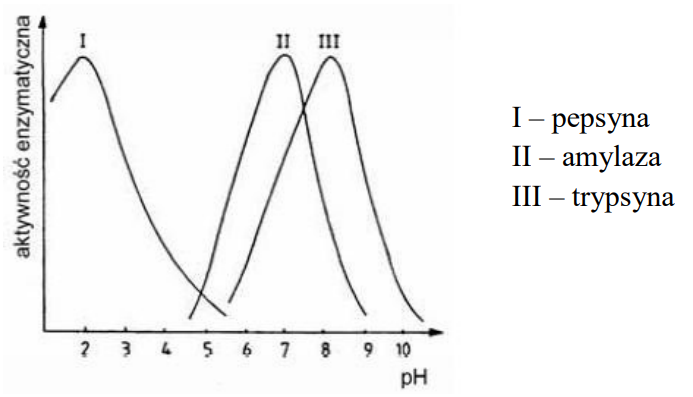
Na wykresie przedstawiono zależność aktywności enzymów od pH. Optimum aktywności amylazy występuje przy pH
Błąd pomiarowy, który stanowi różnicę pomiędzy średnim wynikiem pomiaru a wartością rzeczywistą, określa się mianem
Do początkowych zanieczyszczeń atmosferycznych zalicza się
Roztwór zawierający aniony I grupy analitycznej poddano identyfikacji metodą chromatografii cienkowarstwowej. Na chromatogramie uwidoczniono dwie plamki w odległości 5,6 cm i 3,5 cm od linii startu. Odległość czoła eluenta od linii startu wyniosła 10,1 cm, a wartości wskaźników Rf wzorców anionów wynoszą odpowiednio: Które z anionów zawierała badana próbka?
| Anion | Cl- | Br- | I- | SCN- |
| Wskaźnik Rf | 0,243 | 0,352 | 0,554 | 0,648 |
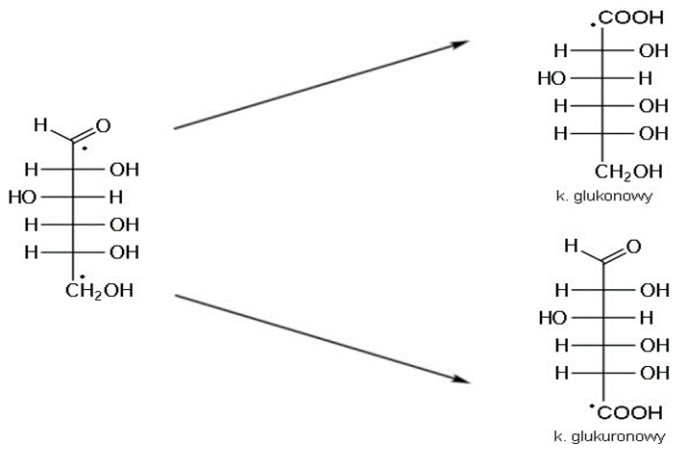
Kwas glukuronowy powstaje z glukozy w wyniku utlenienia
Urządzenie Orsata jest wykorzystywane do pomiaru
Jak nazywana jest technika analityczna, która polega na pomiarze przewodnictwa roztworu umieszczonego pomiędzy dwiema elektrodami, do których doprowadzany jest prąd przemienny?
Zjawisko polegające na chemicznej modyfikacji substancji, które prowadzi do powstania innego związku, łatwiejszego do oznaczenia przy użyciu konkretnej metody, to
Zwiększenie efektu toksycznego jednej substancji chemicznej poprzez inną substancję, która jest jednocześnie dostarczana do organizmu, nazywa się działaniem
Oznaczono LZ i LJ dla czterech różnych próbek tłuszczów. Wyniki zestawiono w tabeli. Na podstawie zamieszczonych danych o liczbach właściwych wybranych tłuszczów wskaż próbkę, którą stanowi olej rzepakowy.
| Liczby właściwe wybranych tłuszczów | ||
|---|---|---|
| Rodzaj tłuszczu | Liczba zmydlania (LZ) mg KOH / g tłuszczu | Liczba jodowa (LJ) g I₂ / 100 g tłuszczu |
| Olej lniany | 187 – 197 | 169 – 192 |
| Olej sojowy | 188 – 195 | 114 – 138 |
| Olej rzepakowy | 167 – 179 | 94 – 106 |
| Tran wielorybi | 170 – 202 | 102 – 144 |
| Masło krowie | 218 – 245 | 25 – 38 |
| Smalec wieprzowy | 193 – 200 | 46 – 66 |
| Próbka | Liczba zmydlania (LZ) | Liczba jodowa (LJ) |
|---|---|---|
| 1 | 190 | 140 |
| 2 | 171 | 99 |
| 3 | 194 | 105 |
| 4 | 195 | 60 |
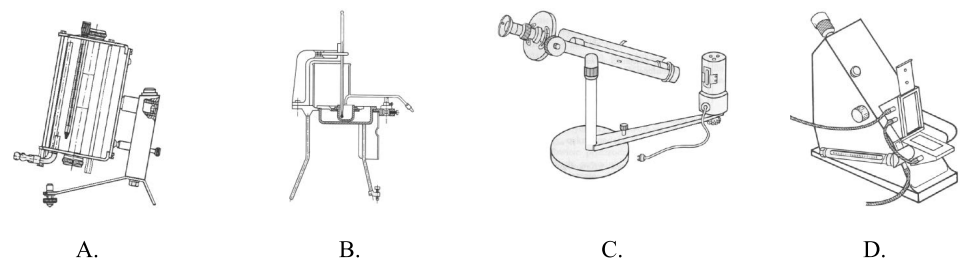
Na którym rysunku przedstawiono przyrząd do pomiaru współczynnika załamania światła?
Stężenie wielopierścieniowych węglowodorów aromatycznych (WWA) w analizowanej próbce wynosi 4 g/dm3.
Po przeliczeniu jednostki na mg/m3 stężenie WWA będzie wynosić
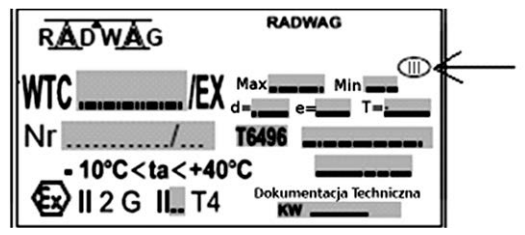
Strzałka zamieszczona na rysunku, przedstawiającym tabliczkę znamionową wagi, wskazuje na
Aby obliczyć wartość absorbancji substancji X, dokonano pomiaru absorbancji mieszaniny X i Y oraz samej substancji Y przy tych samych długościach fali. Jeśli AX+Y = 0,84, a AY = 0,56, to jaką wartość ma AX?
Czym zajmuje się System Analizy Zagrożeń i Krytycznych Punktów Kontroli (HACCP)?
Lepkość dynamiczna wody
| Tabela. Gęstość (d) i lepkość dynamiczna wody (η) w danej temperaturze (T). | ||
| T [K] | d [g/cm3] | η [cP] |
| 293 | 0,99823 | 1,0050 |
| 298 | 0,99707 | 0,8937 |
| 303 | 0,99567 | 0,8007 |
| 308 | 0,99406 | 0,7225 |
| 313 | 0,99222 | 0,6560 |
| 318 | 0,99025 | 0,5988 |
| 323 | 0,98807 | 0,5494 |
| 328 | 0,98573 | 0,5064 |
| 333 | 0,98324 | 0,4688 |
Jaką substancję oznacza się metodą Kjeldahla?
W celu identyfikacji czterech próbek cukrów zbadano ich skręcalność właściwą. Błąd systematyczny pomiaru wynosił + 10%. Wynik próbki pierwszej to + 57,8°. Na podstawie danych zawartych w tabeli można stwierdzić, że badanym cukrem jest
| Skręcalność właściwa roztworów niektórych związków optycznie czynnych (w temp. 20°C) | ||
|---|---|---|
| Substancja | Rozpuszczalnik | Skręcalność właściwa |
| Sacharoza | Woda | + 66,5° |
| Glukoza | Woda | + 52,5° |
| Fruktoza | Woda | + 93,0° |
| Maltoza | Woda | + 136,9° |
Na podstawie zamieszczonego opisu wskaż, którą metodę stosuje się do oznaczania zawartości kwasu acetylosalicylowego.
| Oznaczenie zawartości kwasu acetylosalicylowego w preparacie farmaceutycznym |
| Oznaczenie polega na hydrolizie tego kwasu na gorąco, za pomocą mianowanego roztworu wodorotlenku sodu o stężeniu 0,1 mol/dm3, do salicylanu i octanu sodu. Nadmiar NaOH odmiareczkowuje się mianowanym roztworem kwasu siarkowego(VI) wobec fenoloftaleiny jako wskaźnika. |
Hydroliza sacharozy zachodzi pod działaniem kwasów mineralnych oraz enzymu inwertazy. W wyniku tej reakcji tworzy się mieszanina
Oznaczono LZ i LJ dla czterech różnych próbek tłuszczów. Wyniki zestawiono w tabeli:
Na podstawie zamieszczonych danych o liczbach właściwych wybranych tłuszczów wskaż próbkę, którą stanowi olej rzepakowy.
| Liczby właściwe wybranych tłuszczów | ||
|---|---|---|
| Rodzaj tłuszczu | Liczba zmydlania (LZ) mg KOH / g tłuszczu | Liczba jodowa (LJ) g I₂ / 100 g tłuszczu |
| Olej lniany | 187 – 197 | 169 – 192 |
| Olej sojowy | 188 – 195 | 114 – 138 |
| Olej rzepakowy | 167 – 179 | 94 – 106 |
| Tran wielorybi | 170 – 202 | 102 – 144 |
| Masło krowie | 218 – 245 | 25 – 38 |
| Smalec wieprzowy | 193 – 200 | 46 – 66 |
| Próbka | Liczba zmydlania (LZ) | Liczba jodowa (LJ) |
|---|---|---|
| 1 | 190 | 140 |
| 2 | 171 | 99 |
| 3 | 194 | 105 |
| 4 | 195 | 60 |
Ilość flawonoidów, które wykazują działanie antyoksydacyjne, powinna wynosić dziennie 1000 mg. Oblicz, jak wiele gramów czarnej porzeczki należy zjeść, aby zaspokoić potrzebę na antyoksydanty, wiedząc, że 100 g czarnej porzeczki zawiera 640 mg flawonoidów.
Wykonano analizę mikrobiologiczną próbki wody wodociągowej o objętości 100 ml i uzyskano wyniki:
Wymagania mikrobiologiczne, jakim powinna odpowiadać woda wodociągowa wprowadzana | |||
|---|---|---|---|
| Lp. | Parametr | Wartość parametryczna | |
| liczba mikroorganizmów [jtk lub NPL] | objętość próbki [ml] | ||
| 1. | Escherichia coli | 0 | 250 |
| 2. | Enterokoki | 0 | 250 |
| 3. | Pałeczka ropy błękitnej (Pseudomonas aeruginosa) | 0 | 250 |
| 4. | Ogólna liczba mikroorganizmów w 36±2°C | 20 | 1 |
| 5. | Ogólna liczba mikroorganizmów w 22±2°C | 100 | 1 |
| Escherichia coli | nieobecne |
| Enterokoki | nieobecne |
| Pałeczki ropy błękitnej | nieobecne |
| Ogólna liczba mikroorganizmów w 37°C | 1200 |
| Ogólna liczba mikroorganizmów w 22°C | 11000 |
Wygięty pręt wykonany ze szkła, metalu lub plastiku, który służy do przeprowadzania posiewów na powierzchni i rozprowadzania materiału biologicznego, jest w mikrobiologii określany jako