Pytanie 1
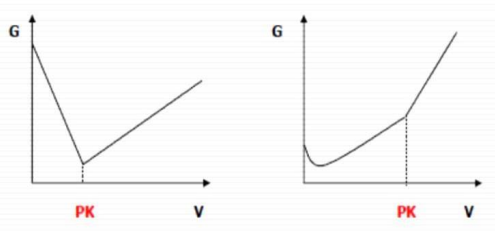
Wykresy przedstawiają przebieg krzywych miareczkowania
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Wykresy przedstawiają przebieg krzywych miareczkowania

Rozpraszanie promieniowania świetlnego przez cząstki koloidalne, które mają wymiary mniejsze od długości fali światła, to zjawisko
Aby zniwelować oddziaływanie wody obecnej w próbce materiału sypkiego na rezultat analizy składu, próbkę należy poddać
Jaką metodą oznacza się kwas solny w analizie miareczkowej?
W kulturze bakterii i grzybów nie należy używać jako pożywki
Odczynnikiem grupowym kationów IV grupy analitycznej jest
| A. | H2S w roztworze NH3(aq) i NH4Cl. |
| B. | roztwór HCl o stężeniu 2 mol/dm3. |
| C. | (NH4)2CO3 w roztworze NH3(aq) i NH4Cl. |
| D. | H2S w roztworze HCl o stężeniu 0,3 mol/dm3. |
W literaturze chromatografię określa się skrótem GC
Jakie urządzenie wykorzystuje się do pomiaru lepkości względnej?
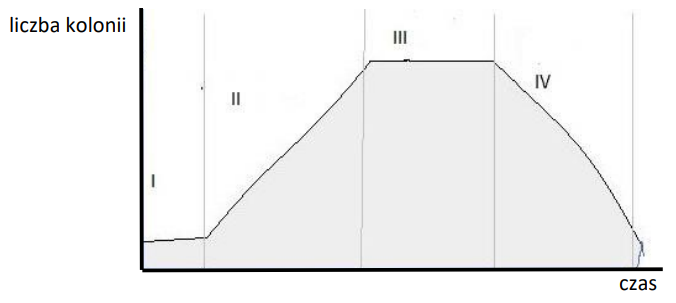
Na wykresie przedstawiającym krzywą wzrostu bakterii, cyfrą IV oznaczono fazę
Zabarwienie roztworu soli prostej w wodzie na zielono wskazuje na obecność jonu
Podłoże, które jest wykorzystywane do uzyskiwania hodowli z wysoką liczbą drobnoustrojów danego szczepu, nazywamy
Właściwością jakościową produktów technologicznych jest
Dla czterech różnych próbek gleb lekkich o odczynie kwaśnym oznaczono zawartość metali w mg/kg suchej masy. Wyniki zestawiono w tabeli:
Graniczne zawartości metali śladowych w powierzchniowej warstwie gleb bardzo lekkich | |||||
|---|---|---|---|---|---|
| Stopień zanieczyszczenia gleb | Zawartość metali w mg/kg suchej masy | ||||
| Pb | Cd | Zn | Cu | Ni | |
| 0 zawartość naturalna | 30 | 0,3 | 50 | 15 | 10 |
| 1 zawartość podwyższona | 70 | 1 | 100 | 30 | 30 |
| 2 słabe zanieczyszczenie | 100 | 2 | 300 | 50 | 50 |
| 3 średnie zanieczyszczenie | 500 | 3 | 700 | 150 | 100 |
| 4 silne zanieczyszczenie | 2500 | 5 | 3000 | 300 | 400 |
| 5 bardzo silne zanieczyszczenie | >2500 | >5 | >3000 | >300 | >400 |
| Metal | Próbka 1. | Próbka 2. | Próbka 3. | Próbka 4. |
|---|---|---|---|---|
| Pb | 180,0 | 15,0 | 25,0 | 29,0 |
| Cd | 1,6 | 0,3 | 0,2 | 0,6 |
| Zn | 40,0 | 55,5 | 48,0 | 37,0 |
| Cu | 328,0 | 25,0 | 8,0 | 56,0 |
| Ni | 135,0 | 8,0 | 8,0 | 19,0 |
Jaki wskaźnik jest używany do oceny kontaktu między wodami naturalnymi a fekaliami?
Wzór przedstawia związek chemiczny stosowany jako odczynnik grupowy kationów
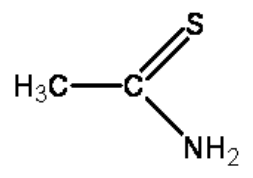
W ramce przedstawiono równania reakcji zachodzące podczas pośredniego jodometrycznego oznaczania
| 2Cu2+ + 4I- →2CuI + I2 I2 + S2O32- → 2I- + S4O62- |
Na którym rysunku przedstawiono schemat metody dokładnej i nieprecyzyjnej?
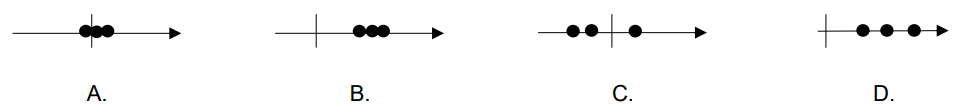
W tabeli podano kryteria energetyczno-emisyjne dla paliw stałych.
Na podstawie analizy danych zamieszczonych w tabeli wskaż numer próbki, która spełnia kryteria energetyczno-emisyjne w zakresie badanych parametrów.
| Parametr | Jedn. | Kryteria kwalifikacyjne | |
|---|---|---|---|
Analiza techniczna | Zawartość popiołu, Ar | % | ≤ 12 |
| Wartość opałowa, Qr | kJ/kg | ≥ 24 000 | |
| Zawartość siarki całkowitej, Sr | % | < 1 | |
| Spiekalność -Liczba Rogi, RI *3 | - | ||
| Temperatura spiekania popiołu w atmosferze utleniającej, TS(O) | °C | ≥ 900 | |
| Temperatura mięknienia popiołu w atmosferze utleniającej, TA(O) | °C | ≥ 1200 | |
Stężenie zanieczyszczeń w spalinach *1 | Ditlenek siarki, SO2 | [mg/m3] | ≤ 1100 |
| Tlenek węgla, CO | [mg/m3] | ≤ 1200 | |
| Tlenki azotu, NOx*2 | [mg/m3] | ≤ 400 | |
| Pył | [mg/m3] | ≤ 125 | |
| Całkowite zanieczyszczenia organiczne, TOC | [mg/m3] | ≤ 75 | |
| Wielopierścieniowe węglowodory aromatyczne, 16 WWA wg EPA | [mg/m3] | ≤ 5 | |
| Benzo(a)piren, B(a)P | [mg/m3] | ≤ 75 | |
| Badany parametr | Nr próbki | |||
|---|---|---|---|---|
| 1 | 2 | 3 | 4 | |
| SO2 [mg/m3] | 1000 | 1100 | 1200 | 1100 |
| CO [mg/m3] | 900 | 990 | 1200 | 1300 |
| Pył [mg/m3] | 150 | 125 | 125 | 125 |
Który z poniższych związków chemicznych (w odpowiednio przygotowanej postaci roztworu) stanowi odczynnik grupowy dla kationów IV grupy?
Reakcja: MnO4- + 8H+ + 5e- → Mn2+ + 4H2O jest wykorzystywana w metodzie analizy jakościowej, określanej jako
Na podstawie danych zamieszczonych w tabeli określ zależność lepkości cieczy od temperatury.
| Ciecz | Lepkość [Pa×s×10-3] | |||
|---|---|---|---|---|
| 0°C | 10°C | 30°C | 60°C | |
| Aceton | 0,397 | 0,361 | 0,296 | 0,228 |
| Toluen | 0,700 | 0,667 | 0,517 | 0,381 |
| Woda | 1,792 | 1,308 | 0,801 | 0,469 |
Rodzaj chromatografii, w której rozdzielanie składników następuje na podstawie różnic w rozpuszczalności osadów formujących się w wyniku reakcji między jonami w roztworze a osadzonym na nośniku reagentem strącającym, określa się mianem chromatografii
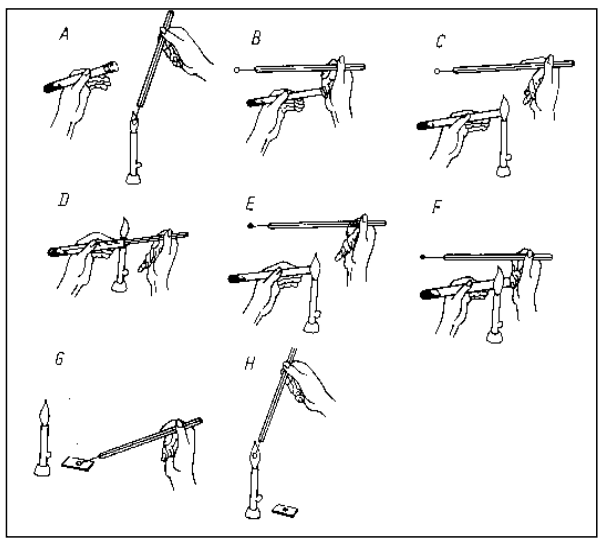
Który ze sprzętów przedstawionych na rysunkach jest niezbędny do przygotowania 250 cm3 mianowanego roztworu NaOH z fiksanalu?
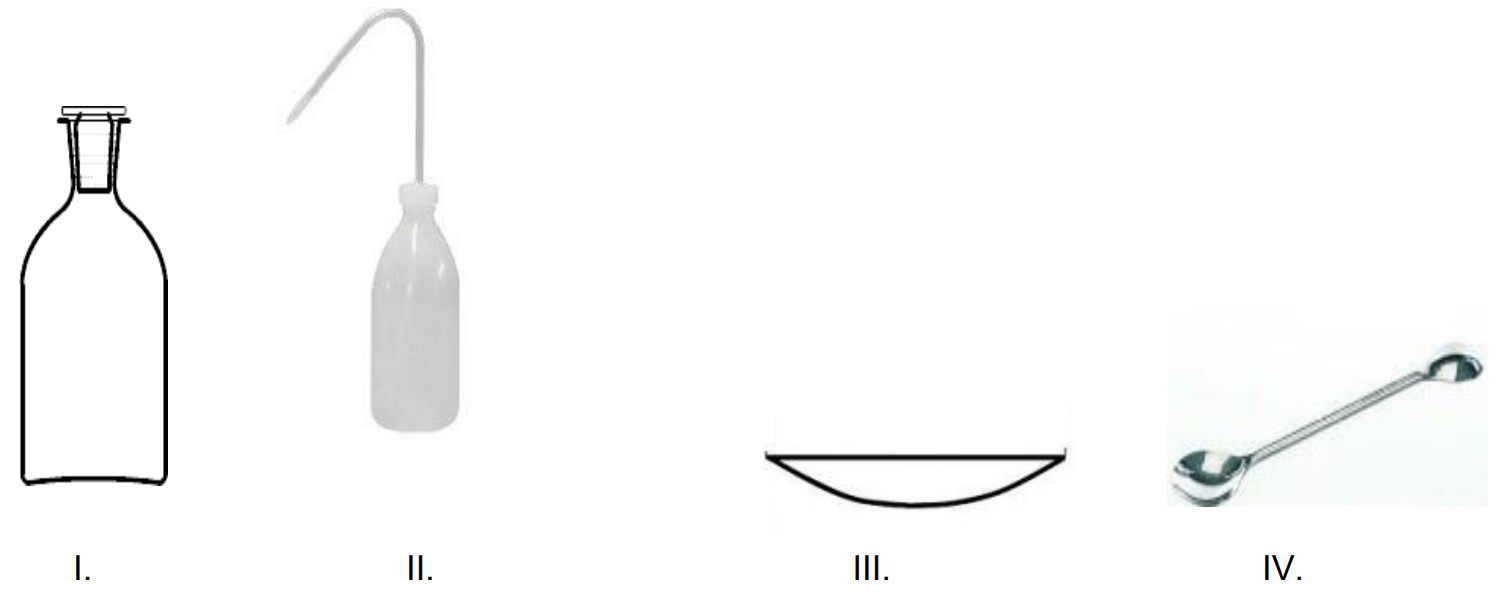
Metodą, którą można oznaczyć całkowitą zawartość siarki w paliwach stałych, jest
Którą właściwość fizyczną substancji można wyznaczyć za pomocą przyrządu przedstawionego na rysunku?
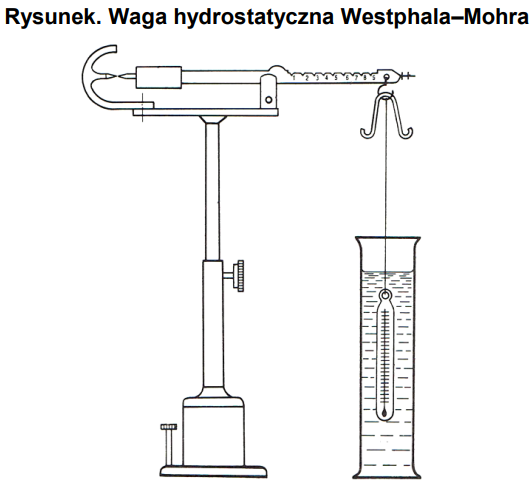
Na podstawie informacji zamieszczonych w tabeli wskaż wzór związku, który wytrąci się w postaci osadu.
| Badany kation | Odczynnik grupowy | NaOH | Barwienie płomienia |
|---|---|---|---|
| Mg2+ | brak | biały osad | |
| K+ | brak | fiołkowy | |
| Na+ | brak | żółty |
Zjawisko alkalizacji gleby jest spowodowane
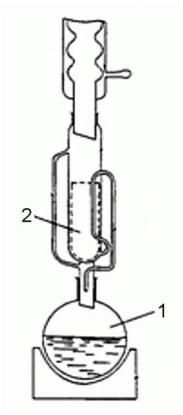
Na rysunku przedstawiono schemat szklanej elektrody zespolonej. Cyfrą 1 oznaczono
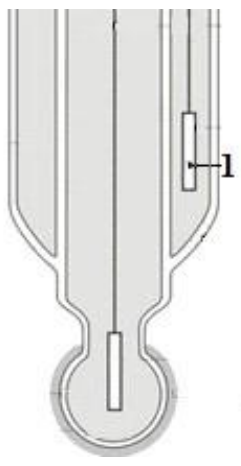
Który nawóz, spośród wymienionych w tabeli, zawiera najwięcej azotu azotanowego?
| Tabela. Zawartość składnika czynnego w nawozach azotowych | |
|---|---|
| Nawóz | Zawartość składników, % |
| Saletra potasowa | N – 13,5% |
| Saletra magnezowa | N – 10,8% |
| Saletra amonowa | N – 34% (NH4+ – 17%, NO3- – 17%) |
| Saletra wapniowa | N – 14,5% |
| Siarczan amonu | N – 21% |
| Mocznik | N – 46% |
Przyrząd, który konwertuje fizyczne lub chemiczne cechy substancji na sygnał analityczny, który można zaobserwować lub zarejestrować, to
Na podstawie zamieszczonego opisu wskaż, którą metodę stosuje się do oznaczania zawartości kwasu acetylosalicylowego.
| Oznaczenie zawartości kwasu acetylosalicylowego w preparacie farmaceutycznym |
| Oznaczenie polega na hydrolizie tego kwasu na gorąco, za pomocą mianowanego roztworu wodorotlenku sodu o stężeniu 0,1 mol/dm3, do salicylanu i octanu sodu. Nadmiar NaOH odmiareczkowuje się mianowanym roztworem kwasu siarkowego(VI) wobec fenoloftaleiny jako wskaźnika. |
Parametr jakości wody, który wskazuje minimalną objętość w cm3, w której może znajdować się jedna komórka bakterii Escherichia coli lub innych pokrewnych bakterii żyjących w jelitach człowieka, określa się mianem
W analizach kompleksometrycznych dużej grupy kationów metali jako titrant wykorzystuje się związek chemiczny o ogólnym wzorze Na2H2Y. Przebieg analizy przedstawiono w formie równania reakcji:
Me(H2O)xn+ + H2Y2- ↔ MeYn-4 + 2H3O+ + (x-2) H2O Który z kationów metali nie jest oznaczany tą techniką?
Na schemacie przedstawiającym sposób pobierania hodowli do badań ze skosu agarowego, literą A oznaczono
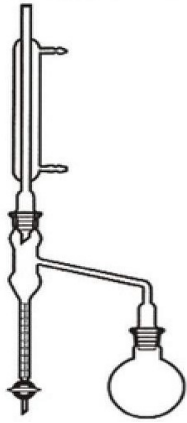
Na rysunku przedstawiono aparat, za pomocą którego można oznaczyć
Równania reakcji zamieszczone w ramce opisują oznaczanie w tłuszczach liczby
| −CH=CH− + IBr → −CHI−CHBr− IBr + KI → KBr + I2 I2+ 2Na2S2O3 →2NaI + Na2S4O6 |
Proces, w wyniku którego formy wegetatywne mikroorganizmów ulegają zniszczeniu (pozostają jedynie bakterie w postaci spor oraz tzw. wolne wirusy), nazywany jest
Jak nazywana jest technika analityczna, która polega na pomiarze przewodnictwa roztworu umieszczonego pomiędzy dwiema elektrodami, do których doprowadzany jest prąd przemienny?
W celu przeprowadzenia bezpośredniego testu ELISA należy postąpić zgodnie z procedurą

W celu przeprowadzenia oznaczenia za pomocą aparatu przedstawionego na ilustracji surowiec roślinny umieszcza się w