Pytanie 1
Jakie proporcje objętościowe powinny być zastosowane do zmieszania roztworu etanolu o stężeniu 30% (V/V) z roztworem o stężeniu 70% (V/V), aby uzyskać roztwór o stężeniu 50% (V/V)?
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
Jakie proporcje objętościowe powinny być zastosowane do zmieszania roztworu etanolu o stężeniu 30% (V/V) z roztworem o stężeniu 70% (V/V), aby uzyskać roztwór o stężeniu 50% (V/V)?
Z podanego wykazu wybierz sprzęt potrzebny do zmontowania zestawu do sączenia pod próżnią.
| 1 | 2 | 3 | 4 | 5 | 6 |
| pompka wodna | lejek z długą nóżką | kolba okrągłodenna | kolba ssawkowa | lejek sitowy | chłodnica powietrzna |
Technika kwartowania (ćwiartkowania) pozwala na redukcję masy próbki ogólnej
Osady kłaczkowe, które powstają w wyniku prostego koagulowania, określa się mianem osadów
Które spośród substancji wymienionych w tabeli pozwolą pochłonąć wydzielający się tlenek węgla(IV)?
| I | II | III | IV | V |
|---|---|---|---|---|
| Ca(OH)2(aq) | NaOH(s) | HNO3(stęż) | CuO(s) | CaO(s) |
W którym wierszu są zapisane nazwy wyłącznie rozpuszczalników palnych?
| Właściwości wybranych rozpuszczalników. | ||||
|---|---|---|---|---|
| Rozpuszczalnik | Gęstość [g/cm3] | Temperatura wrzenia [°C] | Temperatura zapłonu [°C] | Rozpuszczalność w wodzie [g/100 cm3] |
| Eter dietylowy | 0,71 | 35 | -45 | 7 |
| Heksan | 0,66 | 60-80 | -23 | 0,01 |
| Aceton | 0,79 | 57 | -18 | ∞ |
| Benzen | 0,88 | 80 | -11 | 0,07 |
| Chloroform | 1,49 | 61 | - | 0,82 |
| Tetrachlorometan | 1,59 | 77 | - | 0,08 |
| Etanol | 0,81 | 78 | 12 | ∞ |
| Chlorometan | 1,34 | 41 | - | 2 |
Próbka pobrana z próbki ogólnej, która odzwierciedla cechy partii produktu, określa się jako próbka
Czego się używa w produkcji z porcelany?
Aby przygotować miano kwasu solnego, konieczne jest odważenie węglanu sodu o masie wynoszącej około 400 mg. Jaką precyzję powinna mieć waga używana do odważenia węglanu sodu?
Do rozpuszczania próbek wykorzystuje się wodę królewską, która stanowi mieszaninę stężonych kwasów
Stosunek masowy miedzi do siarki w siarczku miedzi(I) wynosi
| 16S Siarka 32 | 29Cu Miedź 63,55 |
W trakcie określania miana roztworu NaOH, do zmiareczkowania 25,0 cm3 tego roztworu, użyto 30,0 cm3 roztworu HCl o stężeniu 0,1000 mol/dm3. Jakie miało miano zasady?
Z partii materiału należy pobrać ogólną próbkę w ilości odpowiadającej promilowi całej partii. Na podstawie podanej informacji określ, ile pierwotnych próbek, każda ważąca 10 g, trzeba pobrać z partii cukru o masie 0,5 t, aby uzyskać reprezentatywną próbkę ogólną?
Podczas pipetowania menisk górny określa się dla roztworów
Laboratoryjny stół powinien być zaopatrzony w instalację gazową oraz
Na podstawie wykresu wskaż substancję, której rozpuszczalność rośnie najszybciej w przedziale temperatury od 10°C do 20°C.
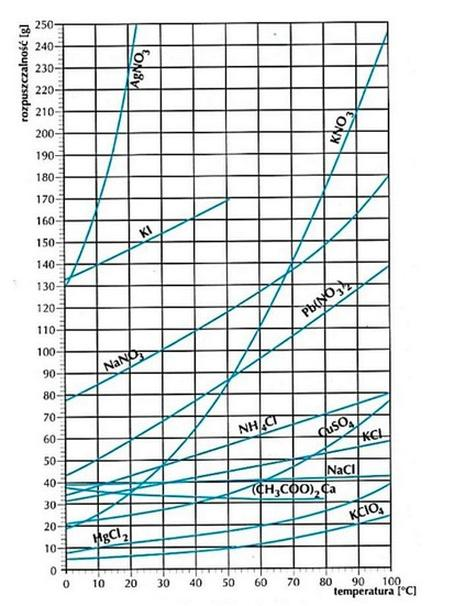
W którym wierszu tabeli podano ilości substancji i wody, potrzebne do sporządzenia 350 g roztworu o stężeniu 7%?
| Masa substancji | Masa wody | |
|---|---|---|
| A. | 24,5 g | 350 g |
| B. | 24,5 g | 325,5 g |
| C. | 7 g | 343 g |
| D. | 7 g | 350 g |
Nie należy używać gorącej wody do mycia
Metoda oczyszczania substancji, która opiera się na różnicy w rozpuszczalności substancji docelowej oraz zanieczyszczeń w zastosowanym rozpuszczalniku, nosi nazwę
Który z procesów jest endotermiczny?
Na podstawie informacji zawartej na pipecie, została ona skalibrowana na
Aby wykonać czynności analityczne wskazane w ramce, należy użyć:
| Otrzymaną do badań próbkę badanego roztworu rozcieńczyć wodą destylowaną w kolbie miarowej o pojemności 100 cm3 do kreski i dokładnie wymieszać. Następnie przenieść pipetą 10 cm3 tego roztworu do kolby stożkowej, dodać ok. 50 cm3 wody destylowanej. |
W celu wydania świadectwa kontroli jakości odczynnika chemicznego - jodku potasu cz.d.a. przeprowadzono jego analizę. Wymagania oraz wyniki badań zapisano w tabeli:
Z analizy danych zawartych w tabeli wynika, że jodek potasu cz.d.a.
| Wymagania | Wynik badania | |
|---|---|---|
| Zawartość KI | min. 99,5% | 99,65% |
| Wilgoć | max. 0,1% | 0,075% |
| Substancje nierozpuszczalne w wodzie | max. 0,005% | 0,002% |
| pH (5%, H2O) | 6 ÷ 8 | 6,8 |
| Azot ogólny (N) | max. 0,001% | 0,0007% |
| Chlorki i bromki (j. Cl) | max. 0,01% | 0,004% |
| Fosforany (PO4) | max. 0,001% | 0,0006% |
| Jodany (IO3) | max. 0,0003% | 0,0001% |
| Siarczany (SO4) | max. 0,001% | 0,0004% |
| Metale ciężkie (j. Pb) | max. 0,0005% | 0,00025% |
| Arsen (As) | max. 0,00001% | 0,000006% |
| Magnez (Mg) | max. 0,001% | 0,0004% |
| Sód (Na) | max. 0,05% | 0,015% |
| Wapń (Ca) | max. 0,001% | 0,0006% |
| Żelazo (Fe) | max. 0,0003% | 0,0003% |
W trakcie reakcji estryfikacji opisanej równaniem CH3COOH + C2H5OH ↔ CH3COOC2H5 + H2O użyto molowego stosunku alkoholu do kwasu wynoszącego 1:10. W rezultacie tego
Oddzielanie płynnej mieszanki poprzez jej odparowanie, a potem skroplenie poszczególnych składników to
Próbki pobrano z materiału o objętości \( 100 \, \text{m}^3 \), wysypanego z opakowania. Liczba miejsc poboru próbek pierwotnych z tego materiału wynosi:
$$ n = 0{,}5 \cdot \sqrt{V} $$ gdzie:
\( V \) – objętość jednostki badanej w \( \text{m}^3 \)
\( n \) – liczba miejsc poboru próbek
Na rysunku numerami rzymskimi oznaczono
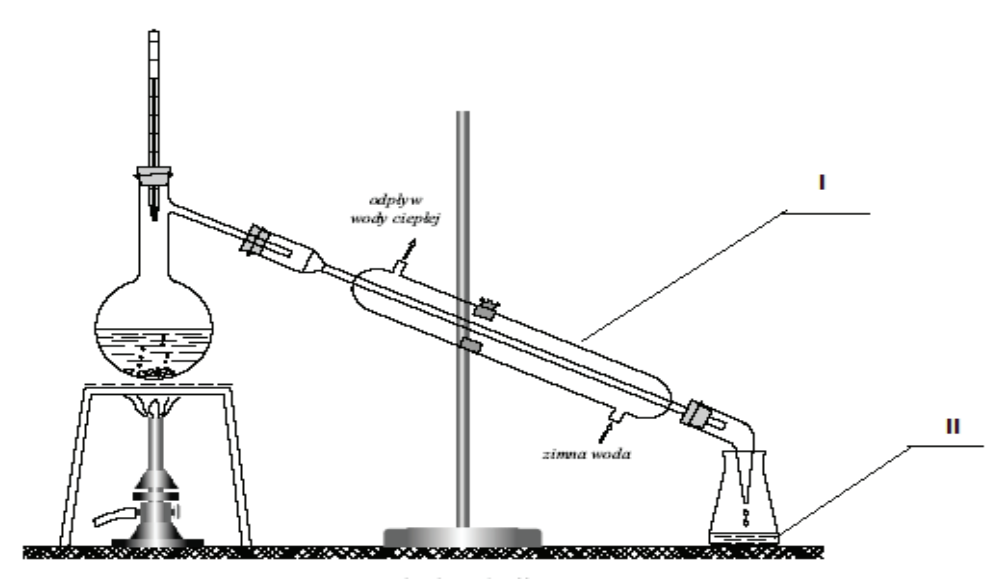
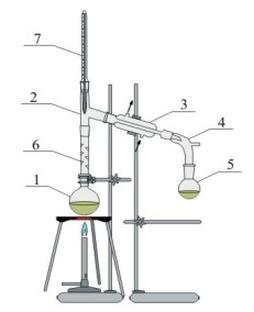
Na rysunku przedstawiono zestaw do oczyszczania jodu w procesie
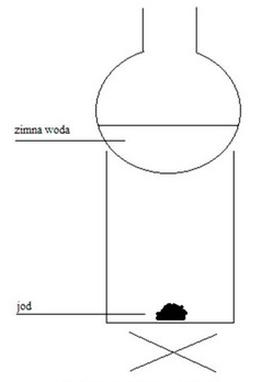
Aby podnieść stężenie mikroelementów w roztworze, próbkę należy poddać
Z uwagi na bezpieczeństwo pracy, ciecze żrące powinny być podgrzewane w łaźniach
250 cm3 roztworu kwasu octowego o stężeniu 10% objętościowych zostało rozcieńczone pięciokrotnie. Jakie jest stężenie otrzymanego roztworu?
Wszystkie pojemniki z odpadami, zarówno stałymi, jak i ciekłymi, które są przekazywane do służby zajmującej się utylizacją, powinny być opatrzone informacjami
Na rysunku przedstawiono proces
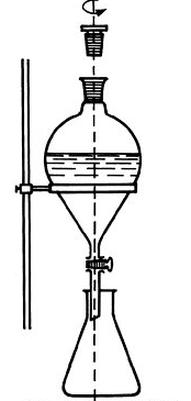
Podczas pomiaru masy substancji w naczyniu wagowym na wadze technicznej, dla zrównoważenia ciężaru na szalce umieszczono odważniki: 20 g, 2 g, 500 mg, 200 mg, 20 mg, 10 mg, 10 mg oraz 5 g. Całkowita masa substancji z naczynkiem wyniosła
Zestaw przedstawiony na rysunku służy do
Podczas analizowania zmienności składu wód płynących w skali rocznej, próbki wody powinny być zbierane i badane przynajmniej raz na
Pobieranie próbek wody z zbiornika wodnego, który zasila system wodociągowy, powinno odbywać się
Proces nitrowania najczęściej realizuje się, stosując organiczny substrat
Aby uniknąć trwałego połączenia szlifowanych części sprzętu laboratoryjnego, co należy zrobić?
Na podstawie danych w tabeli próbkę, w której będzie oznaczany BZT, należy przechowywać
| Oznaczany parametr | Rodzaj naczynia do przechowywania | Sposób utrwalania | Dopuszczalny czas przechowywania |
|---|---|---|---|
| barwa | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C | 24 h |
| fosforany ogólne | szklane lub polietylenowe | - zakwaszenie kwasem siarkowym(VI) - schłodzenie do temperatury 2-5°C | 4 h 48 h |
| BZT | szklane | - schłodzenie do temperatury 2-5°C - przechowywanie w ciemności | 24 h |
| azot azotanowy(V) | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C - dodanie 2 cm3 chloroformu do 1 dm3 próbki | 24 h 48 h |