Pytanie 1
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na zmiareczkowanie 10 cm3 NaOH zużyto 2 cm3 0,1-molowego roztworu H2SO4. Ilość wodorotlenku sodu w badanej próbce w g/100 cm3 wynosi (Na — 23 g/mol, O — 16 g/mol, H — 1 g/mol)
W metodzie analitycznej zapisano. Który parametr metody analitycznej opisano w ramce?
| Różnica w otrzymanych wynikach dwóch oznaczeń wykonanych równocześnie lub w krótkim przedziale czasu na tej samej próbce, przez tego samego analityka, w takich samych warunkach, nie może przekraczać 1,5 g na 100 g oznaczanej próbki. |
Który z poniższych związków chemicznych (w odpowiednio przygotowanej postaci roztworu) stanowi odczynnik grupowy dla kationów IV grupy?
Który ze związków będzie barwny w świetle widzialnym?
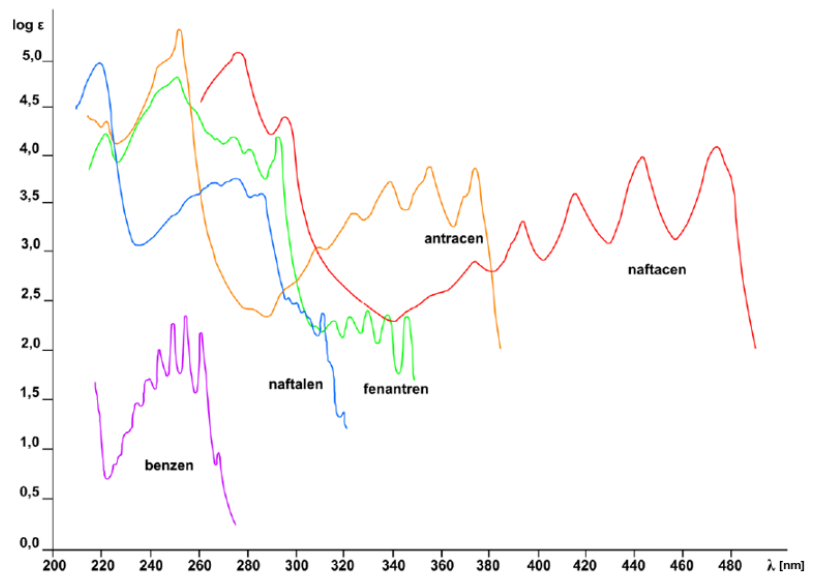
Metoda obrączkowa jest wykorzystywana do rozpoznawania jonu
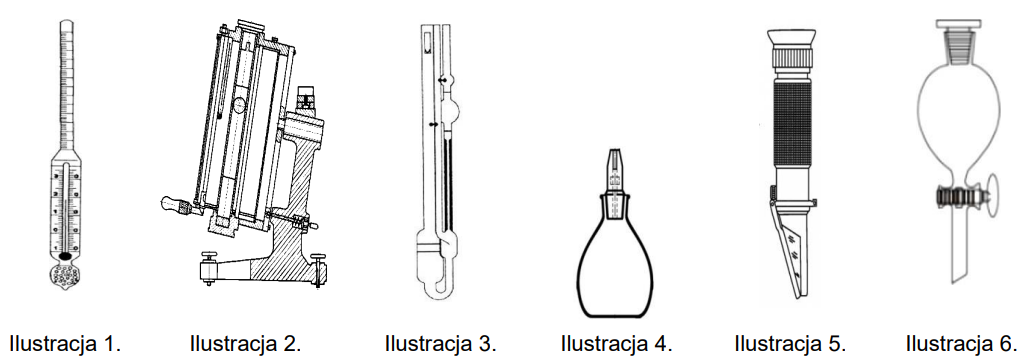
Na których ilustracjach są przedstawione przyrządy służące do wyznaczania gęstości cieczy?
Na podstawie przedstawionych wyników pomiarów zawartości tlenu, pH, suchej pozostałości oraz zawartości jonów rtęci w wodzie wskaż, która próbka wody jest prawidłowo zaklasyfikowana.
| Próbka | Wynik pomiaru wskaźnika | |||
|---|---|---|---|---|
| Zawartość O2 [mg/dm3] | pH | Sucha pozostałość [mg/dm3] | Zawartość Hg2+ [mg/dm3] | |
| 1 | 4 | 9 | 1200 | 0,006 |
| 2 | 5 | 8,5 | 600 | 0,0001 |
| 3 | 5,5 | 9 | 900 | 0,0001 |
| Klasa | Wartości dopuszczalne | |||
| I | 6 i powyżej | 6,5 ÷ 8 | 500 i poniżej | 0,001 i poniżej |
| II | 5 i powyżej | 6,5 ÷ 9 | 1000 i poniżej | 0,005 i poniżej |
| III | 4 i powyżej | 6 ÷ 9 | 1200 i poniżej | 0,01 i poniżej |
| Numer próbki wody | Klasa wody | |
|---|---|---|
| A. | 1 | II |
| B. | 2 | II |
| C. | 2 | I |
| D. | 3 | III |
Jaką substancję oznacza się metodą Kjeldahla?
Zielonkawo lub żółtozielono zabarwiony płomień palnika sygnalizuje obecność jonów
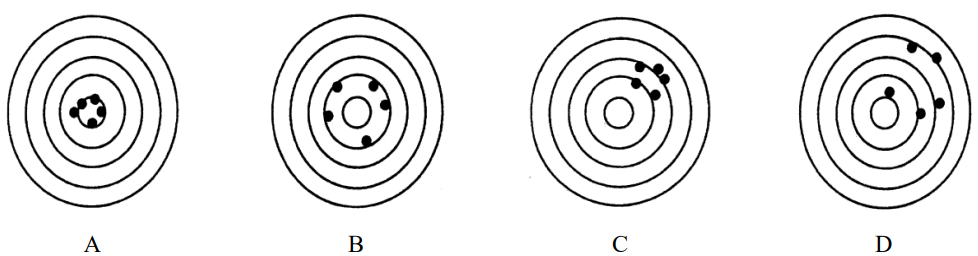
Na rysunkach przedstawiono serie pomiarów o różnej dokładności i precyzji (środek najmniejszego okręgu oznacza wartość prawdziwą). Serię pomiarów nieprecyzyjnych, ale dokładnych, przedstawiono na rysunku
Zamieszczony w ramce opis określa liczbę
| Liczba gramów fluorowca, przeliczona na gramy jodu, który w określonych warunkach ulega reakcji addycji do atomów węgla związanych wiązaniem wielokrotnym, zawartych w 100 g badanego tłuszczu. Jest ona proporcjonalna do liczby wiązań wielokrotnych w tłuszczach. |
Podstawą klasyfikacji kationów w analizie jakościowej jest wydzielanie trudno rozpuszczalnych osadów?
Określ wartość opałową (Qi) węgla kamiennego, którego ciepło spalania jest równe 18752 J/g, zawartość popiołu wynosi 8,7%, zawartość wilgoci wynosi 4,1%.
| Qi = Qsp - 24,42 · (W + 8,94 · ZH) |
Qsp – ciepło spalania, J/g W – zawartość wilgoci, % 24,42 – ciepło parowania wody w temp. 25°C odpowiadające 1% wody w paliwie, J/g 8,94 – współczynnik przeliczenia wodoru na wodę, % ZH – zawartość wodoru w próbce paliwa, % Zawartość wodoru w próbce należy obliczyć z dokładnością do części dziesiątych ze wzoru: ZH = (100 - W - A) / 18,5 A – zawartość popiołu, % |
Po przeprowadzeniu analizy wagowej uzyskano 253 mg Mg2P2O7. Jaką ilość gramów magnezu zawierała zbadana próbka, jeśli współczynnik analityczny wynosi 0,2185?
Rysunek przedstawia
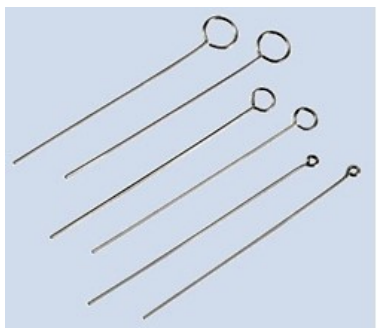
Metodą, którą można oznaczyć całkowitą zawartość siarki w paliwach stałych, jest
Analiza obecności pałeczek Salmonella w żywności zalicza się do badań
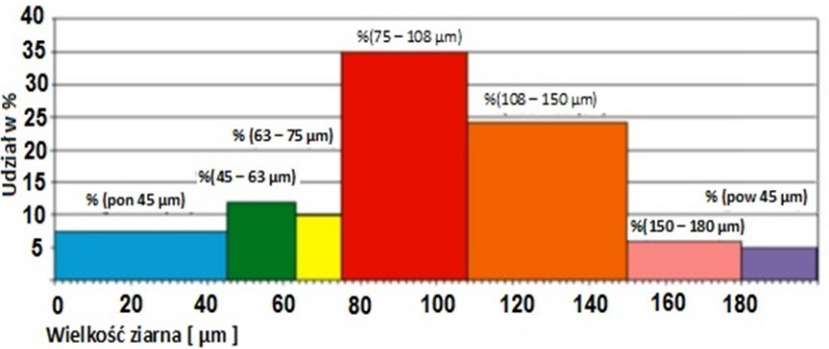
Na diagramie słupkowym przedstawiono wyniki analizy sitowej surowca w formie proszkowej. W jakiej kolejności zamontowano sita w wytrząsarce, licząc je od naczynia zbierającego?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Błąd miareczkowania w oznaczeniach objętościowych nie występuje, gdy
W zamieszczonej informacji przedstawiono równania reakcji zachodzące podczas oznaczania chlorków metodą
| Ag+ + Cl- → AgCl ↓ Ag+ + SCN- → AgSCN ↓ Fe3+ + SCN- → Fe(SCN)2+ |
Do optycznych metod instrumentalnych wykorzystywanych w chemicznej analizie zalicza się
Rozpuszczono próbkę technicznego chlorku sodu w wodzie, a jony chlorkowe strącono przy pomocy AgNO3, w postaci AgCl, którego masa po wysuszeniu wyniosła 1,5000 g. Oblicz ilość chloru w analizowanej próbce. Mnożnik analityczny dla chloru w AgCl to 0,2474.
Jaką metodę analityczną stosuje się do pomiaru przewodnictwa cieczy umieszczonej między dwiema elektrodami, do których dostarczany jest prąd zmienny?
Jaką metodę kontroli stanu mikrobiologicznego powietrza opisano w zamieszczonej informacji?
| Otwarte płytki Petriego z podłożem stałym pozostawiono na 30 minut na wysokości 1 metra od podłogi, a następnie inkubowano przez 48 godzin w temperaturze 37°C. Po tym czasie wyhodowane kolonie zliczono i zidentyfikowano ich szczepy. |
W celu identyfikacji czterech próbek cukrów zbadano ich skręcalność właściwą. Błąd systematyczny pomiaru wynosił + 10%. Wynik próbki pierwszej to + 57,8°. Na podstawie danych zawartych w tabeli można stwierdzić, że badanym cukrem jest
| Skręcalność właściwa roztworów niektórych związków optycznie czynnych (w temp. 20°C) | ||
|---|---|---|
| Substancja | Rozpuszczalnik | Skręcalność właściwa |
| Sacharoza | Woda | + 66,5° |
| Glukoza | Woda | + 52,5° |
| Fruktoza | Woda | + 93,0° |
| Maltoza | Woda | + 136,9° |
W procedurze analitycznej zapisano. Ile wynosi zawartość procentowa Na2B4O7 • H2O w badanej próbce boraksu, jeżeli na zmiareczkowanie 0,3 g próbki zużyto 15,4 cm3 roztworu NaOH?
| 1 cm3 roztworu NaOH o stężeniu 0,1 mol/dm3 odpowiada 19,07 mg tetraboranu sodu Na2B4O7·H2O |
W autoklawach realizuje się proces sterylizacji
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Czym charakteryzuje się barwa roztworu zawierającego jony Cr2O72-?
W świadectwie jakości roztworu amoniaku cz. podana jest informacja: zawartość amoniaku 30÷32% m/m Uwzględniając informacje zawarte w tabeli, określ gęstość tego roztworu w temperaturze 20°C.
| Zależność gęstości roztworu amoniaku od stężenia w 20°C | |||||||
|---|---|---|---|---|---|---|---|
| % wagowy | 1 | 6 | 10 | 16 | 20 | 26 | 30 |
| gęstość [g/cm³] | 0,9939 | 0,9730 | 0,9575 | 0,9362 | 0,9229 | 0,9040 | 0,8920 |
Na etykiecie odczynnika chemicznego zawarte są następujące informacje:
Z informacji wynika, że odczynnik ten może być zastosowany do sporządzenia roztworu o stężeniu około 0,1 mol/dm3 z dokładnością do
| NH4SCN amonu tiocyjanian | 0,1 mol/l |
| Stężenie po rozcieńczeniu do 1000 ml w 20°C | 0,1 mol/l ± 0,2 % |
W laboratorium mikrobiologicznym do przeprowadzania jałowienia na zimno wykorzystuje się
W opisie przeprowadzonego eksperymentu
(...) obecność węgla wykrywa się poprzez spalenie próbki i określenie ilości CO2 przy użyciu roztworu wody barytowej. Azot w trakcie spalania próbki z sodem metalicznym generuje cyjanek, który może być wykryty po dodaniu FeSO4 jako błękit pruski (...) Jakiego rodzaju analizę zastosowano w opisywanym doświadczeniu?
Analiza wody basenowej w celu wykrycia bakterii polega na podgrzewaniu próbki w inkubatorze przez 48 godzin w temperaturze 36±2°C. Jaki proces jest opisany?
Wielkość określająca zmienność wyników przy wielokrotnym pomiarze tego samego składnika tą samą metodą nosi nazwę
Wartość logarytmu stosunku natężenia wiązki padającej do natężenia wiązki przechodzącej przez badany ośrodek (log I0/I) nazywana jest
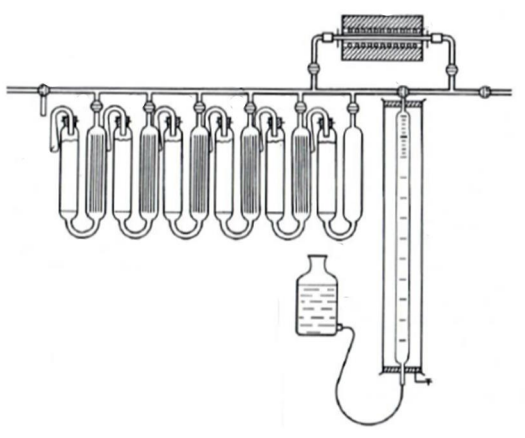
Na rysunku przedstawiono schemat aparatu
Iloczyn rozpuszczalności trudno rozpuszczalnego związku Ca3(PO4)2 wyrażony jest równaniem:
| A. | KSO = [Ca2+] · [PO43-] |
| B. | KSO = [Ca3+]2 · [PO42-]3 |
| C. | KSO = [Ca2+]3 · [PO43-]2 |
| D. | KSO = 3[Ca2+] · 2[PO43-] |