Pytanie 1
Do 300 g wody o temperaturze 30oC dodano 120 g substancji, co zaowocowało powstaniem roztworu nasyconego. Jaką ma rozpuszczalność ta substancja w temperaturze 30oC?
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
Do 300 g wody o temperaturze 30oC dodano 120 g substancji, co zaowocowało powstaniem roztworu nasyconego. Jaką ma rozpuszczalność ta substancja w temperaturze 30oC?
Jakie urządzenie wykorzystuje się do określania lepkości płynów?
Podczas łączenia bezwodnego etanolu z wodą występuje zjawisko kontrakcji. Gdy zmieszamy 1000 cm3 wody oraz 1000 cm3 etanolu, otrzymujemy roztwór o objętości
Jakie jest stężenie roztworu NaOH, który zawiera 4 g wodorotlenku sodu w 1 dm3 (masa molowa NaOH = 40 g/mol)?
Jakie są zalecenia dotyczące postępowania z odpadowymi roztworami kwasów oraz zasad?
Wodę do badań mikrobiologicznych powinno się pobierać do butelek
Komora przeszklona w formie dużej szafy, wyposażona w wentylator, która zapobiega wydostawaniu się szkodliwych substancji do atmosfery laboratorium oraz chroni przed pożarami i eksplozjami, to
Gęstość próbki cieczy wyznacza się przy użyciu
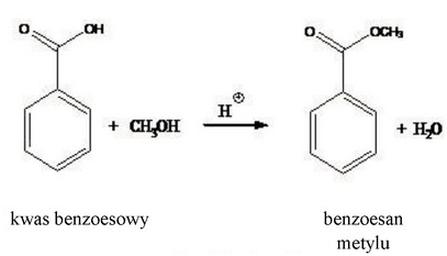
Do reakcji estryfikacji użyto 150 g kwasu benzoesowego (M = 122,12 g/mol), w wyniku której otrzymano czysty preparat benzoesanu metylu (M = 136,2 g/mol). Ile gramów benzoesanu metylu otrzymano, jeżeli reakcja przebiegała z wydajnością 92%?
Proces nastawiania miana kwasu solnego na wodorowęglan potasu KHCO3 przebiega zgodnie z następującą instrukcją:
Na wadze analitycznej odmierzyć 1 g KHCO3 (z precyzją 0,00001 g) i przesypać go ilościowo do kolby stożkowej, dodać około 50 cm3 destylowanej wody i dokładnie wymieszać roztwór. Następnie dodać kilka kropel roztworu czerwieni metylowej. Przeprowadzić miareczkowanie kwasem aż do pierwszej zmiany koloru wskaźnika.
W tym przypadku titrantem jest
W laboratorium chemicznym systemy wodne zazwyczaj oznacza się kolorem zielonym
Które z poniższych równań ilustruje reakcję, w której powstają produkty gazowe?
Co oznacza skrót AKT?
Korzystając z danych w tabeli wskaż, ile cm3 36% roztworu HCl należy użyć, aby przygotować 250 cm3 0,1-molowego roztworu tego kwasu.
| % wagowy [%] | d420 [g/cm3] | m HCl w 100 cm3 [g/100cm3] | CM HCl [mol/dm3] |
|---|---|---|---|
| 30 | 1,1492 | 34,48 | 9,46 |
| 32 | 1,1593 | 37,10 | 10,17 |
| 34 | 1,1691 | 39,75 | 10,90 |
| 36 | 1,1789 | 42,44 | 11,64 |
Aby przeprowadzić syntezę substancji organicznej w temperaturze 150°C, należy zastosować łaźnię
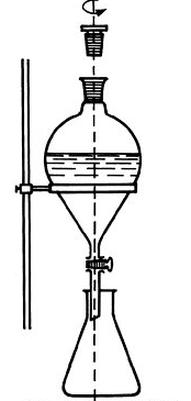
Na rysunku przedstawiono proces
Jakie jest stężenie procentowe roztworu HCl (M=36,46 g/mol) o gęstości 1,19 g/cm3 oraz stężeniu molowym 12 mol/dm3?
Aby oddzielić połączenia szlifów, należy w miejscu ich styku wprowadzić
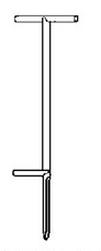
Przedstawiony na rysunku zagłębnik stosuje się do pobierania próbek
Miesięczne zapotrzebowanie laboratorium analitycznego na 2-propanol wynosi 500 cm3. Na jak długo wystarczy ta substancja?
Sączenie osadów kłaczkowatych odbywa się przy użyciu sączków
Proces chemiczny, który polega na przejściu substancji w stanie stałym do roztworu, związany z reakcją tej substancji z rozpuszczalnikiem, to
Jakie oznaczenie znajduje się na naczyniach szklanych kalibrowanych do wlewu?
Próbka pobrana z próbki ogólnej, która odzwierciedla cechy partii produktu, określa się jako próbka
Oblicz, ile moli gazu można zebrać w pipecie gazowej o pojemności 500 cm3, jeśli gaz będzie gromadzony w warunkach normalnych. (W normalnych warunkach jeden mol gazu ma objętość 22,4 dm3)
Losowo należy pobierać próbki z opakowań
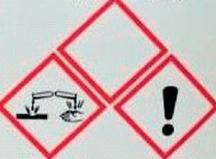
Według zasady pierwszeństwa, znajdując na opakowaniu zbiorczym odczynnika piktogramy pokazane na rysunku, należy zwrócić szczególną uwagę na to, że substancja jest
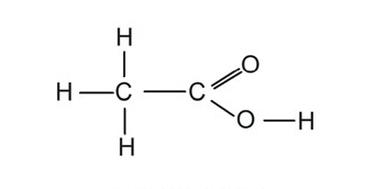
Związek o podanym wzorze to kwas
Po połączeniu 50 cm3 wody z 50 cm3 alkoholu etylowego, objętość otrzymanej mieszanki jest poniżej 100 cm3. Zjawisko to jest spowodowane
Wybór lokalizacji do poboru próbek wody z rzeki nie jest uzależniony od
Jaką masę NaCl uzyskuje się poprzez odparowanie do sucha 250 g roztworu 10%?
Instalacja, do której należy podłączyć palnik, powinna być pokryta farbą w kolorze
W przypadku rozlania żrącego odczynnika chemicznego na skórę pierwszym poprawnym działaniem jest:
Wskaź sprzęt laboratoryjny, który znajduje się w zestawie do filtracji pod obniżonym ciśnieniem?
Aby uzyskać Cr2O3, dichromian(VI) amonu został poddany rozkładowi. Po rozpoczęciu, egzotermiczna reakcja rozkładu przebiega samorzutnie.
(NH4)2Cr2O7 → Cr2O3 + 4 H2O + N2 Jak oceniasz zakończenie tej reakcji?
Na rysunku przedstawiono palnik Bunsena. Którym numerem oznaczono element do regulowania dopływu powietrza?

Aby uzyskać drobnokrystaliczny osad BaSO4, należy wykonać poniższe kroki:
Do zlewki wlać 20 cm3 roztworu BaCl2, następnie dodać 100 cm3 wody destylowanej oraz kilka kropli roztworu HCl. Zawartość zlewki podgrzać na łaźni wodnej, a potem, ciągle mieszając, dodać 35 cm3 roztworu H2SO4.
Mieszaninę ogrzewać na łaźni wodnej przez 1 godzinę. Osad odsączyć i przepłukać kilkakrotnie gorącą wodą zakwaszoną kilkoma kroplami roztworu H2SO4.
Według przedstawionej procedury, do uzyskania osadu BaSO4 potrzebne są:
Jaką masę wodorotlenku potasu trzeba odważyć, żeby przygotować 500 cm3 roztworu o stężeniu 0,02 mola? Masy molowe poszczególnych pierwiastków wynoszą: potas K - 39 g/mol, tlen O - 16 g/mol, wodór H - 1 g/mol?
Najskuteczniejszą techniką separacji ketonu oraz kwasu karboksylowego obecnych w roztworze benzenowym jest
Jakie substancje wykorzystuje się do wykrywania obecności jonów chlorkowych w wodzie mineralnej?