Pytanie 1
Podczas reakcji chlorku żelaza(III) z wodorotlenkiem potasu dochodzi do wytrącenia wodorotlenku żelaza(III) w formie
Wynik: 3/40 punktów (7,5%)
Wymagane minimum: 20 punktów (50%)
Podczas reakcji chlorku żelaza(III) z wodorotlenkiem potasu dochodzi do wytrącenia wodorotlenku żelaza(III) w formie
Który z procesów jest endotermiczny?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Naczynia miarowe kalibrowane "na wlew" mają oznaczenie w postaci symbolu
Temperatura topnienia mocznika wynosi 133 °C. W celu określenia czystości preparatów tej substancji, przeprowadzono badania temperatury ich topnienia, uzyskując wyniki przedstawione w tabeli. Wskaż preparat o najmniejszym stopniu czystości.
| Preparat | A | B | C | D |
|---|---|---|---|---|
| Zakres temperatury topnienia [°C] | 132-133 | 130-133 | 125-133 | 128-133 |
W laboratoriach roztwór potasu dichromianu(VI) w stężonym kwasie siarkowym(VI) wykorzystuje się do
Brak odpowiedzi na to pytanie.
Zestaw do filtracji nie zawiera
Brak odpowiedzi na to pytanie.
Aby wykonać czynności analityczne wskazane w ramce, należy użyć:
| Otrzymaną do badań próbkę badanego roztworu rozcieńczyć wodą destylowaną w kolbie miarowej o pojemności 100 cm3 do kreski i dokładnie wymieszać. Następnie przenieść pipetą 10 cm3 tego roztworu do kolby stożkowej, dodać ok. 50 cm3 wody destylowanej. |
Brak odpowiedzi na to pytanie.
Woda, która została poddana dwukrotnej destylacji, to woda
Brak odpowiedzi na to pytanie.
Przedstawiony zestaw stosowany jest w laboratorium do przeprowadzenia procesu
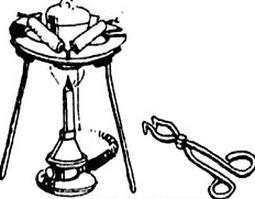
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Roztwór zawierający 16,00 g siarczanu(VI) miedzi(II) nasycono siarkowodorem. Masa wytrąconego siarczku miedzi(II), po odsączeniu i wysuszeniu, wynosiła 8,64 g. Oblicz procentową wydajność tej reakcji.
Równanie reakcji:
\( \text{CuSO}_4 + \text{H}_2\text{S} \rightarrow \text{CuS} + \text{H}_2\text{SO}_4 \)
\( \text{M CuSO}_4 = 160 \, \text{g/mol} \)
\( \text{M CuS} = 96 \, \text{g/mol} \)
Brak odpowiedzi na to pytanie.
W karcie charakterystyki chemikaliów znajduje się informacja o przechowywaniu dichromianu(VI) potasu: .. powinien być przechowywany w odpowiednio oznakowanych, szczelnie zamkniętych pojemnikach, w chłodnym, suchym i dobrze wentylowanym magazynie, który posiada instalację elektryczną i wentylacyjną. Z tego opisu wynika, że ten chemikal może być przechowywany
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Sprzęt laboratoryjny przedstawiony na ilustracji stanowi element zestawu do

Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Dla cieczy bezbarwnej odczyt w biurecie pokazanej na rysunku wynosi

Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Próbka pobrana z próbki ogólnej, która odzwierciedla cechy partii produktu, określa się jako próbka
Brak odpowiedzi na to pytanie.
Aby przygotować miano kwasu solnego, konieczne jest odważenie węglanu sodu o masie wynoszącej około 400 mg. Jaką precyzję powinna mieć waga używana do odważenia węglanu sodu?
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Próbka laboratoryjna posiadająca cechy higroskopijne powinna być pakowana
Brak odpowiedzi na to pytanie.
Jakim rozpuszczalnikiem o niskiej temperaturze wrzenia wykorzystuje się do suszenia szkła laboratoryjnego?
Brak odpowiedzi na to pytanie.
Między wodorotlenkiem baru a chlorkiem amonu dochodzi do spontanicznej reakcji, która powoduje silne schłodzenie mieszaniny oraz wydobycie się charakterystycznego zapachu amoniaku.
Ba(OH)2(s) + 2 NH4Cl(s) → BaCl2(aq) + 2 H2O(c) + 2 NH3(g) Wskaź, które sformułowanie właściwie wyjaśnia to zjawisko.
nieodwracalnie jej równowagę.
Brak odpowiedzi na to pytanie.
Do metalowego sprzętu laboratoryjnego używanego w praktykach analitycznych zalicza się
Brak odpowiedzi na to pytanie.
Aby przeprowadzać ręczną obróbkę szkła w laboratorium, konieczne jest posiadanie okularów ochronnych oraz rękawic.
Brak odpowiedzi na to pytanie.
Jakie jest stężenie molowe kwasu siarkowego(VI) o zawartości 96% i gęstości 1,84 g/cm3?
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Zgłębniki o konstrukcji przypominającej świder są wykorzystywane do pobierania próbek różnych materiałów
Brak odpowiedzi na to pytanie.
Aby przygotować 0,5 dm3 roztworu HCl o stężeniu 0,2 mol/dm3, jaką kolbę miarową o pojemności należy wykorzystać?
Brak odpowiedzi na to pytanie.
Jaki jest błąd względny pomiaru na wadze o precyzji 0,1 g dla próbki o wadze 1 g?
Brak odpowiedzi na to pytanie.
W trakcie pobierania próbek wody, które mają być analizowane pod kątem składników podatnych na rozkład fotochemiczny, należy
Brak odpowiedzi na to pytanie.
Na podstawie informacji zawartych w tabeli wskaż mieszaninę oziębiającą o temperaturze -21 °C.
| Temperatura mieszaniny | Skład mieszaniny | Stosunek masowy |
| -15 °C | lód + octan sodu | 10:9 |
| -18 °C | lód + chlorek amonu | 10:3 |
| -21 °C | lód + chlorek sodu | 3:1 |
| -25 °C | lód + azotan amonu | 1:9 |
Brak odpowiedzi na to pytanie.
Instrukcja dotycząca przygotowania wzorcowego roztworu NaCl
0,8242 g NaCl, które wcześniej wysuszono w temperaturze 140 °C do stałej masy, należy rozpuścić w kolbie miarowej o pojemności 1 dm3 w wodzie podwójnie destylowanej, a następnie uzupełnić do kreski tym samym rodzajem wody.
Z treści instrukcji wynika, że odpowiednio skompletowany sprzęt wymagany do sporządzenia wzorcowego roztworu NaCl, oprócz naczynia wagowego, powinien zawierać
Brak odpowiedzi na to pytanie.
W celu sprawdzenia stężenia kwasu siarkowego(VI) odważono 1 g badanego kwasu i przeprowadzono analizę miareczkową, w której zużyto 20,4 \( \text{cm}^3 \) roztworu NaOH.
Stężenie procentowe badanego kwasu, obliczone na podstawie wzoru wynosi
$$ C_p = \frac{0,02452 \cdot V_{NaOH}}{mp} \cdot 100\% $$gdzie:
\( C_p \) – stężenie procentowe badanego kwasu; \( \% \)
\( 0,02452 \) – współczynnik przeliczeniowy; \( \text{g/cm}^3 \)
\( V_{NaOH} \) – objętość roztworu NaOH, zużyta w miareczkowaniu; \( \text{cm}^3 \)
\( mp \) – odważka badanego kwasu; g
Brak odpowiedzi na to pytanie.
Wykonano ocenę jakości dostarczonej partii wodorotlenku sodu.
Zgodne ze specyfikacją towaru są
| Parametr oznaczany | Jednostka | Wartość parametru | |
|---|---|---|---|
| Według specyfikacji | Zbadana analitycznie | ||
| Zawartość wodorotlenku sodu | % | >=98 | 98,3 |
| Zawartość węglanu sodu | % | <=0,4 | 0,39 |
| Zawartość chlorku sodu | % | <=0,015 | 0,015 |
Brak odpowiedzi na to pytanie.
W nieopisanej butelce prawdopodobnie znajduje się roztwór zasadowy. Wskaż odczynnik, który pozwoli to zweryfikować?
Brak odpowiedzi na to pytanie.
Piktogram nie jest konieczny dla
Brak odpowiedzi na to pytanie.
Ogrzewanie organicznych substancji w atmosferze powietrza w otwartym naczyniu, mające na celu przemianę tych substancji w związki nieorganiczne, określa się jako mineralizacja?
Brak odpowiedzi na to pytanie.