Pytanie 1
Badanie przewodu pokarmowego metodą podwójnego kontrastu wiąże się z podaniem pacjentowi
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
Badanie przewodu pokarmowego metodą podwójnego kontrastu wiąże się z podaniem pacjentowi
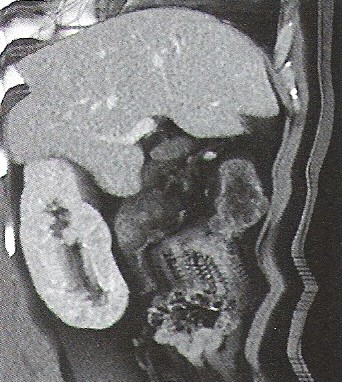
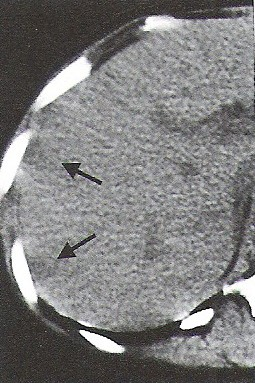
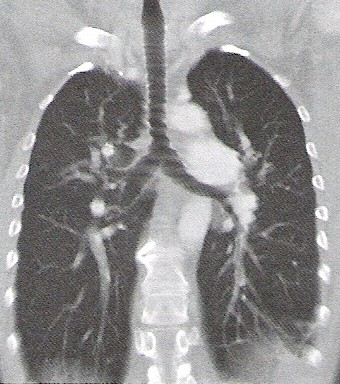
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
Artefakty zarejestrowane na elektrokardiogramie zostały wywołane przez
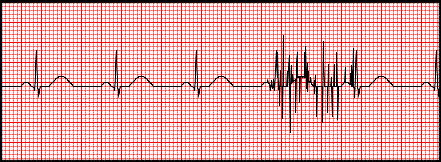
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
Na radiogramie uwidoczniono złamanie nasady
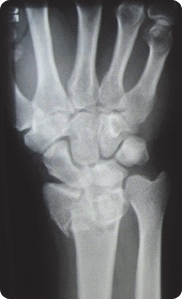
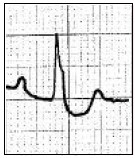
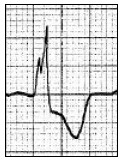
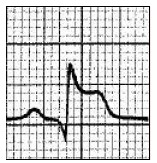
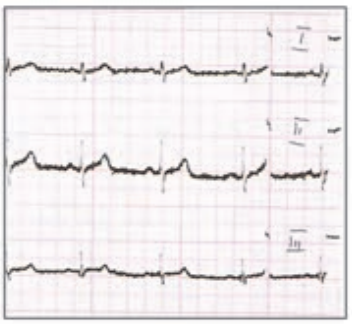
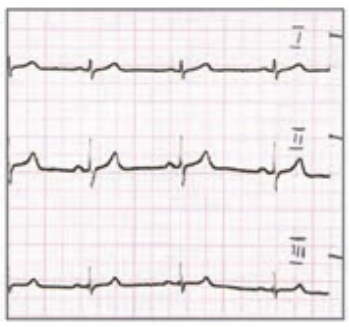
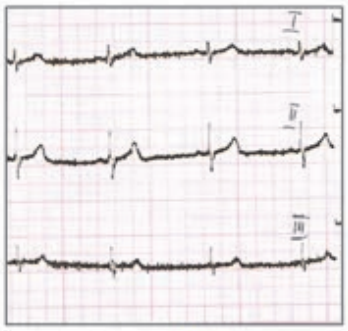
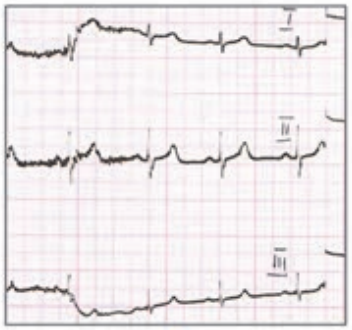
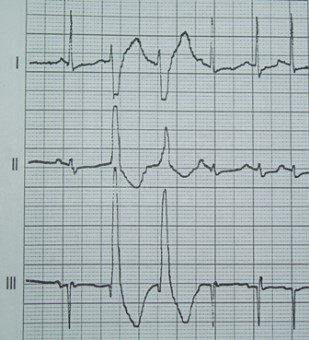
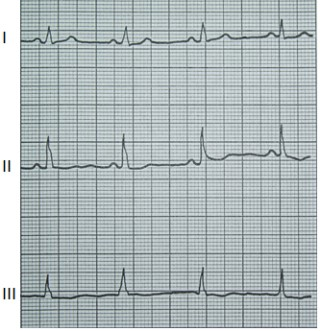
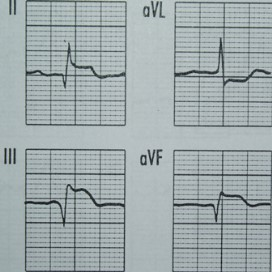
Który zapis EKG przedstawia falę Pardee'go?

Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
Który elektrokardiogram jest poprawny technicznie?
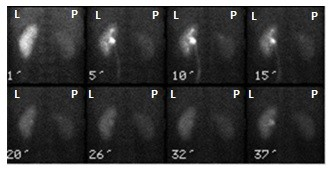
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
W brachyterapii MDR stosowane są dawki promieniowania
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
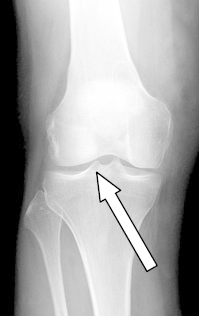
Którą strukturę anatomiczną oznaczono strzałką na radiogramie stawu kolanowego?
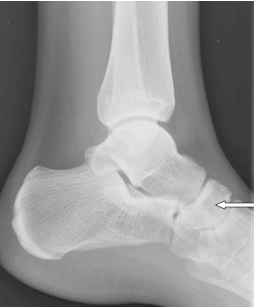
Na radiogramie strzałką oznaczono
Który radioizotop stosuje się do badania scyntygraficznego kości?
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Testy specjalistyczne aparatów rentgenowskich do zdjęć wewnątrzustnych są przeprowadzane
W którym miejscu, zgodnie z zasadami wykonywania badania EKG, należy umocować żółtą elektrodę przedsercową V2?
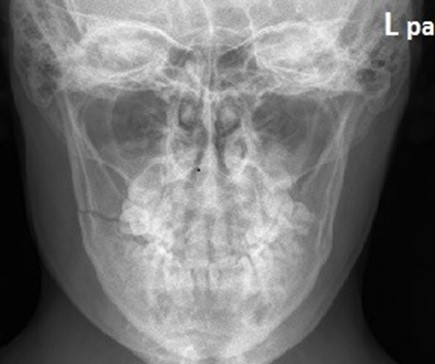
Na radiogramie żuchwy uwidoczniono złamanie w okolicy
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
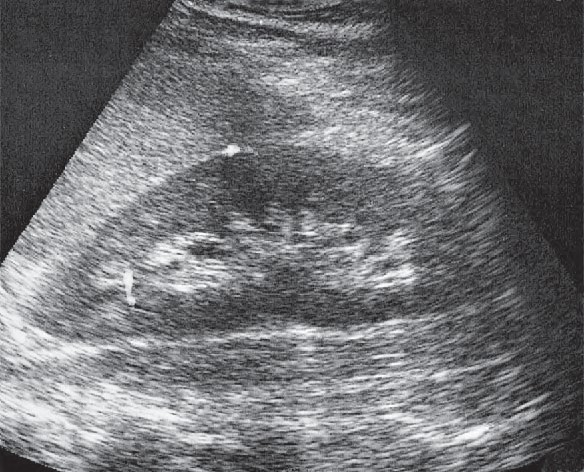
Który narząd widoczny jest na wydruku badania ultrasonograficznego?
Promieniowanie rentgenowskie jest
Które urządzenie zostało przedstawione na fotografii i w jakiej pracowni znajduje zastosowanie?
Jaki kolor ma warstwa korowa kości w badaniu MR na obrazie T1- zależnym?
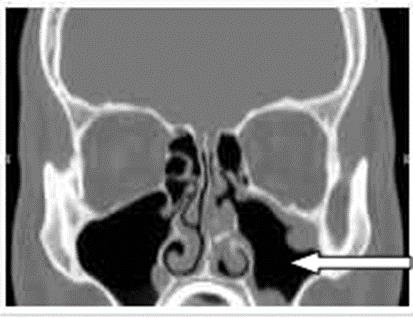
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
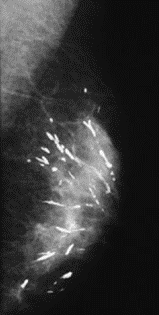
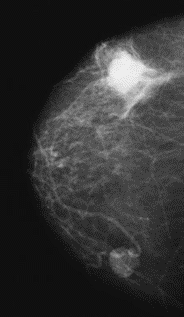
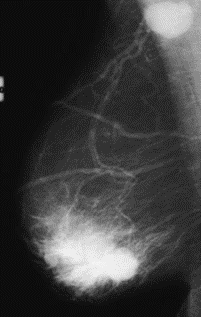
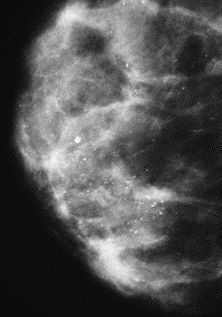
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
W radioterapii hadronowej leczenie odbywa się przy użyciu
Kasety do pośredniej radiografii cyfrowej CR są wyposażone
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Na którym z zapisów EKG została uwidoczniona fala Pardee'go?
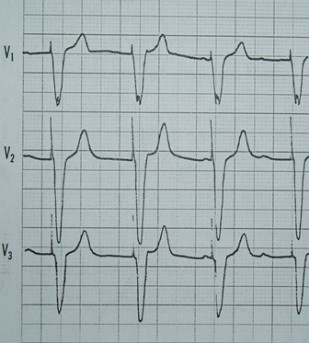
W której próbie stroikowej przystawia się stroik do czoła (u podstawy nosa) lub na szczycie głowy i porównuje się przewodnictwo kostne ucha prawego i lewego?