Pytanie 1
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
Czas połowicznego zaniku jest wykorzystywany
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym
Przedstawiony obraz został zarejestrowany podczas wykonania
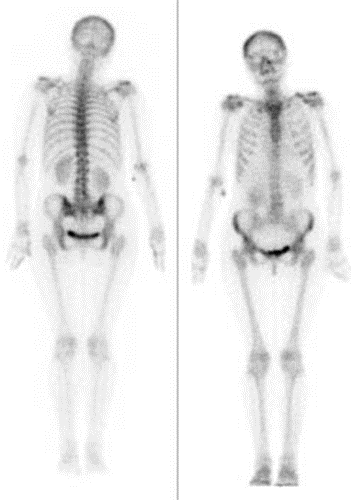
Który radiofarmaceutyk należy podać pacjentowi w scyntygrafii perfuzyjnej mózgu?
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
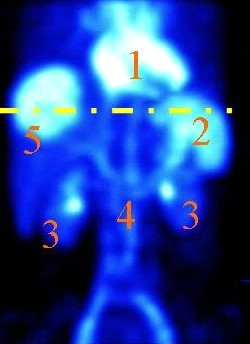
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
Na scyntygramie tarczycy uwidoczniono guzek
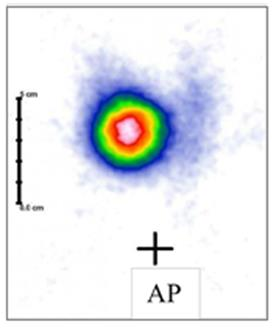
Na scyntygramie kości strzałkami oznaczono ogniska
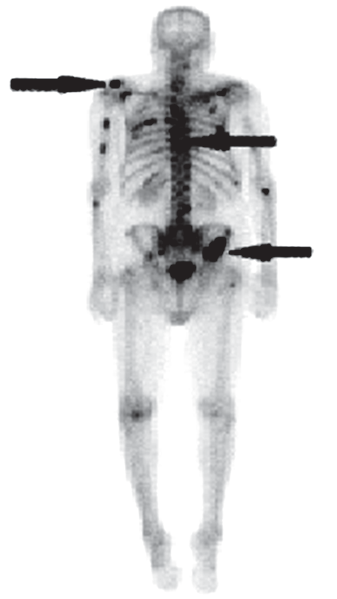
Radiofarmaceutyki stosowane w medycynie nuklearnej powstają dzięki połączeniu radioizotopu
Które znaczniki są wykorzystywane w scyntygrafii tarczycy?
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Który radioizotop jest stosowany w diagnostyce i terapii raka tarczycy?
Podczas badania gammakamerą źródłem promieniowania jest
Na scyntygramie tarczycy został uwidoczniony guzek
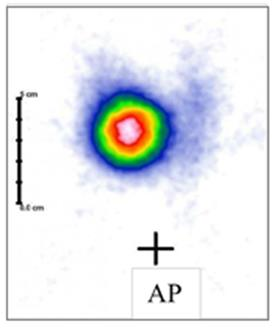
W scyntygrafii perfuzyjnej płuc pacjentowi podawany jest radioizotop
Które urządzenie zostało przedstawione na fotografii i w jakiej pracowni znajduje zastosowanie?
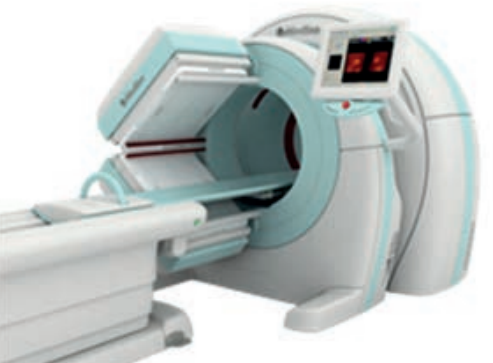
W scyntygrafii dynamiczne badanie najczęściej rozpoczyna się
W badaniu PETCT radioizotop ulega
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Który radioizotop jest stosowany w scyntygrafii perfuzyjnej mózgu?
W badaniu PET stosuje się tylko radioizotopy emitujące
Na którym obrazie zarejestrowano badanie scyntygraficzne?
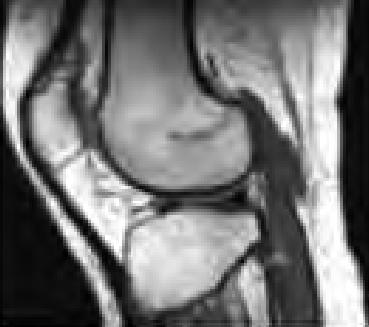
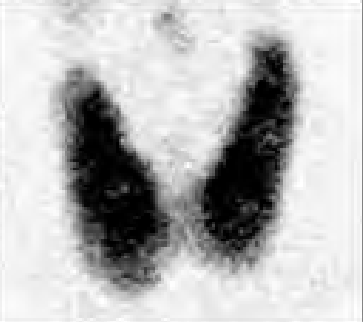
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
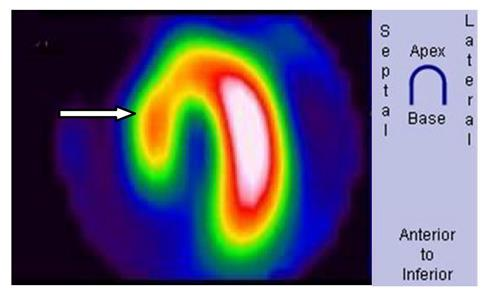
Które informacje należy zamieścić na strzykawce z radiofarmaceutykiem przygotowanym przez technika elektroradiologa?
„Ognisko zimne” w obrazie scyntygraficznym oznacza
Który radioizotop stosuje się do badania scyntygraficznego kości?
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Podstawowym elementem diagnostycznym aparatury izotopowej wykorzystującej emisyjne metody pomiaru jest
Diagnozowanie metodą PET oparte jest na zjawisku
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Scyntygrafia kości „whole body” jest wskazana podczas diagnostyki
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem
Który radioizotop jest emiterem promieniowania alfa?
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Ligand stosuje się