Pytanie 1
Podczas pobierania skoncentrowanego roztworu kwasu solnego konieczne jest pracowanie w włączonym dygestorium oraz zastosowanie
Wynik: 16/40 punktów (40,0%)
Wymagane minimum: 20 punktów (50%)
Podczas pobierania skoncentrowanego roztworu kwasu solnego konieczne jest pracowanie w włączonym dygestorium oraz zastosowanie
Jaką masę wodorotlenku potasu trzeba odważyć, żeby przygotować 500 cm3 roztworu o stężeniu 0,02 mola? Masy molowe poszczególnych pierwiastków wynoszą: potas K - 39 g/mol, tlen O - 16 g/mol, wodór H - 1 g/mol?
Deminimalizowaną wodę można uzyskać przez
Podczas rozkładu chloranu(V) potasu powstają chlorek potasu oraz tlen. Ile gramów tlenu zostanie wydzielonych w trakcie rozkładu 24,5 g chloranu(V) potasu, jeśli jednocześnie uzyskano 14,9 g chlorku potasu? Masy molowe pierwiastków: K = 39 g/mol, Cl = 35,5 g/mol, O=16 g/mol?
Laboratoryjna apteczka powinna zawierać m.in.
Jak nazywa się naczynie o płaskim dnie, które wykorzystuje się do pozyskiwania substancji stałej poprzez stopniowe odparowanie rozpuszczalnika z roztworu?
Mając wagę laboratoryjną z dokładnością pomiaru 10 mg, nie da się wykonać odważki o masie
Przedstawiono wyciąg z karty charakterystyki substancji chemicznej. Na podstawie informacji zawartej w zamieszczonym fragmencie karty wskaż wzór chemiczny substancji, której można użyć jako materiału neutralizującego lodowaty kwas octowy.
Kwas octowy lodowaty 99,5% Materiały zapobiegające rozprzestrzenianiu się skażenia i służące do usuwania skażenia Jeżeli to możliwe i bezpieczne, zlikwidować lub ograniczyć wyciek (uszczelnić, zamknąć dopływ cieczy, uszkodzone opakowanie umieścić w opakowaniu awaryjnym). Ograniczyć rozprzestrzenianie się rozlewiska przez obwałowanie terenu; zebrane duże ilości cieczy odpompować. Małe ilości rozlanej cieczy przysypać niepalnym materiałem chłonnym (ziemia, piasek oraz materiałami neutralizującymi kwasy, np. węglanem wapnia lub sodu, zmielonym wapieniem, dolomitem), zebrać do zamykanego pojemnika i przekazać do zniszczenia. Zanieczyszczoną powierzchnię spłukać wodą. Popłuczyny zebrać i usunąć jako odpad niebezpieczny. |
Jednym z sposobów oddzielania jednorodnych mieszanin jest
Jakie roztwory chemiczne powinny być stanowczo pobierane przy włączonym dygestorium?
Jakie jest stężenie roztworu HNO3, który powstał w wyniku połączenia 50 cm3 roztworu HNO3 o stężeniu 0,2 mol/dm3 oraz 25 cm3 roztworu HNO3 o stężeniu 0,5 mol/dm3?
Wskaź sprzęt laboratoryjny, który znajduje się w zestawie do filtracji pod obniżonym ciśnieniem?
Jaką masę siarczanu(VI) miedzi(II)-woda(1/5) należy poddać suszeniu, aby otrzymać 300 g soli bezwodnej?
| CuSO4 · 5H2O → CuSO4 + 5H2O |
| (MCuSO4·5H2O = 249,5 g/mol, MCuSO4 = 159,5 g/mol, MH2O = 18,0 g/mol) |
Etykiety chemikaliów zawierają zwroty H, które informują o rodzaju zagrożenia. Cyfra "3" pojawiająca się po literze "H" w oznaczeniu, definiuje rodzaj zagrożenia?
Wagi laboratoryjne można klasyfikować według nośności oraz precyzji na
Jakie jest stężenie procentowe roztworu uzyskanego poprzez rozpuszczenie 25 g jodku potasu w 100 cm3 destylowanej wody (o gęstości 1 g/cm3)?
Aparat przedstawiony na rysunku służy do
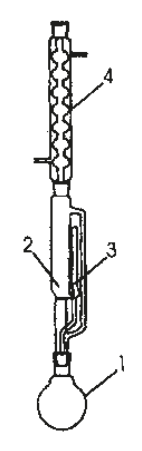
Transformacja zolu w żel to zjawisko określane jako
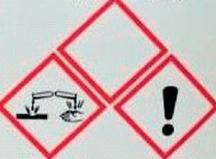
Według zasady pierwszeństwa, znajdując na opakowaniu zbiorczym odczynnika piktogramy pokazane na rysunku, należy zwrócić szczególną uwagę na to, że substancja jest
Ile wynosi objętość roztworu o stężeniu 0,5 mol/dm3, jeśli przygotowano go z 0,1 mola KOH?
Aby poprawić efektywność reakcji opisanej równaniem: HCOOH + C2H5OH ⇄ HCOOC2H5 + H2O, należy
Na podstawie zmierzonej temperatury topnienia można określić związek organiczny oraz ustalić jego
Proces oddzielania składników jednorodnej mieszaniny, polegający na eliminacji jednego lub większej ilości składników z roztworu lub substancji stałej przy użyciu odpowiednio wybranego rozpuszczalnika, to
Co oznacza skrót AKT?
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Jakie są zalecenia dotyczące postępowania z odpadowymi roztworami kwasów oraz zasad?
Najskuteczniejszą techniką separacji ketonu oraz kwasu karboksylowego obecnych w roztworze benzenowym jest
Ile masy kwasu mrówkowego jest wymagane do uzyskania 11,2 dm3 tlenku węgla(II) (w warunkach normalnych) w procesie odwodnienia kwasu mrówkowego (M = 46 g/mol) za pomocą kwasu siarkowego(VI), zakładając efektywność procesu na poziomie 70%?
Dokonano pomiaru pH dwóch roztworów, uzyskując wartości pH= 2 oraz pH= 5. Wskaźnij poprawnie sformułowany wniosek.
Po rozpuszczeniu substancji w kolbie miarowej, należy odczekać przed dopełnieniem jej wodą "do kreski" miarowej. Taki sposób postępowania jest uzasadniony
Procedura przygotowania roztworu Zimmermana-Reinharda
70 g MnSO4·10H2O rozpuścić w 500 cm3 wody destylowanej, dodając ostrożnie 125 cm3 stężonego H2SO4 i 125 cm3 85% H3PO4, ciągle mieszając. Uzupełnić wodą destylowaną do objętości 1dm3.
Który zestaw ilości odczynników jest niezbędny do otrzymania 0,5 dm3 roztworu Zimmermana-Reinharda, zgodnie z podaną procedurą?
| MnSO4·10H2O [g] | Stężony H2SO4 [cm3] | 85% H3PO4 [cm3] | Woda destylowana [cm3] | |
|---|---|---|---|---|
| A. | 35 g | 62,5 cm3 | 62,5 cm3 | ok. 370 cm3 |
| B. | 35 g | 62,5 cm3 | 62,5 cm3 | ok. 420 cm3 |
| C. | 70 g | 125 cm3 | 125 cm3 | ok. 500 cm3 |
| D. | 70 g | 125 cm3 | 125 cm3 | ok. 800 cm3 |
Podczas oznaczania kwasu siarkowego zachodzi reakcja:
H2SO4 + 2NaOH → Na2SO4 + 2H2OZgodnie z zamieszczoną instrukcją, roztwór poreakcyjny należy
| Fragmenty instrukcji zbierania, utylizacji i eliminacji odpadów chemicznych | |
|---|---|
| Lista substancji, które mogą być usunięte z odpadami komunalnymi w postaci stałej, lub wprowadzone do systemu kanalizacyjnego w postaci rozcieńczonych roztworów wodnych, o ile ich ilość nie przekracza jednorazowo 100 g. | |
| Związki nieorganiczne Siarczany sodu, potasu, magnezu, wapnia, amonu | |
| Kwasy nieorganiczne Stężone kwasy ostrożnie rozcieńczyć przez wkroplenie z równoczesnym mieszaniem do wody z lodem, a następnie zneutralizować roztworem wodorotlenku sodowego. Po neutralizacji doprowadzić pH roztworu do zakresu 6-8 przelać do pojemnika S. Małe ilości kwasów takich jak siarkowy, solny, azotowy czy fosforowy (nie więcej niż 10 g) po rozcieńczeniu wodą i neutralizacji roztworem wodorotlenku sodowego oraz doprowadzeniu pH takiego roztworu do zakresu 6-8 można wylać do zlewu i obficie spłukać wodą. | |
| Sole nieorganiczne Stałe sole nieorganiczne – pojemnik N. Obojętne roztwory soli nieorganicznych pojemnik S. Sole metali ciężkich, sole o właściwościach toksycznych – pojemnik TN. |
Podczas łączenia bezwodnego etanolu z wodą występuje zjawisko kontrakcji. Gdy zmieszamy 1000 cm3 wody oraz 1000 cm3 etanolu, otrzymujemy roztwór o objętości
Jak przebiega procedura unieszkodliwiania rozlanego kwasu siarkowego(VI)?
W karcie charakterystyki substancji znajduje się piktogram, którym powinna być oznakowana substancja

Naważkę NaOH o masie 0,0400 g rozpuścić w małej ilości wody, a następnie przelać ten roztwór do kolby miarowej o pojemności 500 cm3 i uzupełnić kolbę miarową wodą do tzw. kreski. Masa molowa NaOH wynosi 40,0 g/mol. Jakie jest stężenie molowe przygotowanego roztworu?
Masa molowa kwasu azotowego(V) wynosi 63,0 g/mol. Jakie jest stężenie molowe 20% roztworu tego kwasu o gęstości 1,1 g/cm3?
Jakie substancje wykorzystuje się do wykrywania obecności jonów chlorkowych w wodzie mineralnej?
Co oznacza zapis cz.d.a. na etykiecie opakowania odczynnika chemicznego?
W którym z podanych równań reakcji dochodzi do zmiany stopni utlenienia atomów?