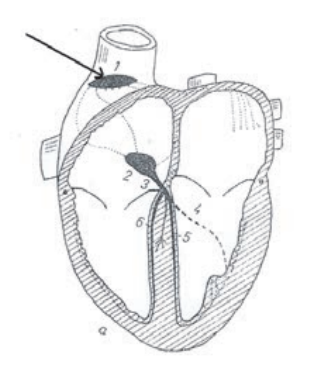
Pytanie 1
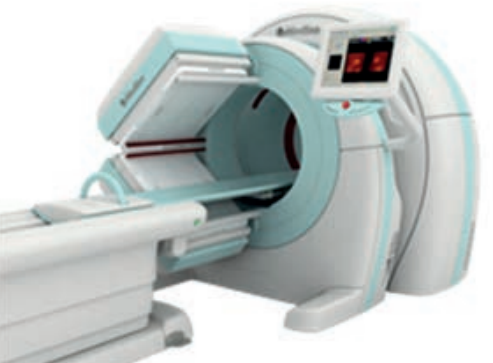
Które urządzenie zostało przedstawione na fotografii i w jakiej pracowni znajduje zastosowanie?
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
Które urządzenie zostało przedstawione na fotografii i w jakiej pracowni znajduje zastosowanie?

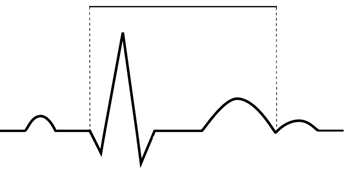
Na wykresie EKG zaznaczono
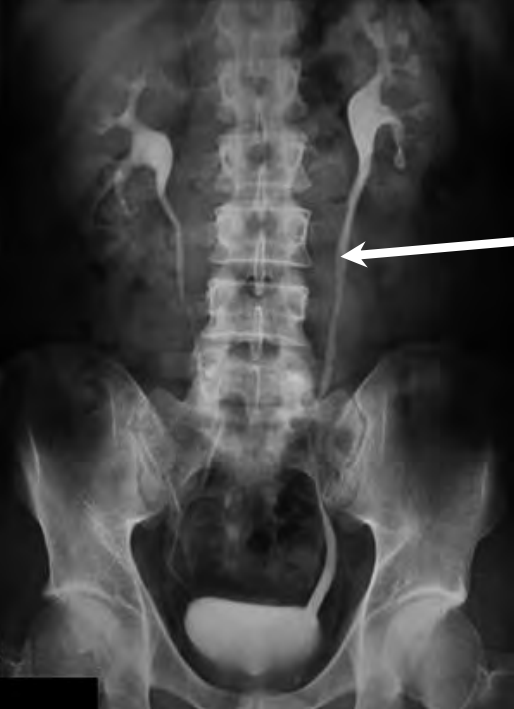
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
Zdjęcie którego zęba górnego zlecił na skierowaniu lekarz stomatolog?
Skrótem CTV w radioterapii oznacza się
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
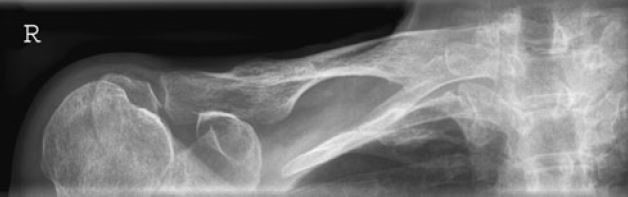
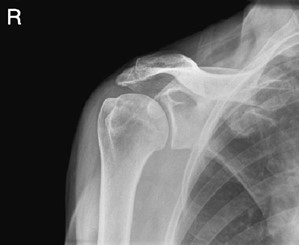
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
Który radioizotop stosuje się do badania scyntygraficznego kości?
Celem radioterapii paliatywnej nie jest
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
Jaki sposób frakcjonowania dawki jest stosowany w radioterapii konwencjonalnej?
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
W zapisie EKG załamek U występuje bezpośrednio po załamku
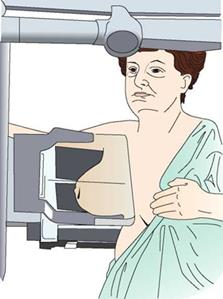
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




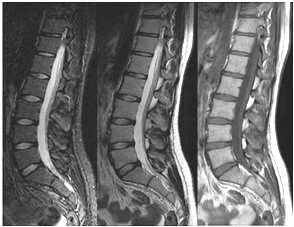
Które kolejne sekwencje badania kręgosłupa lędźwiowego uwidoczniono na przedstawionych obrazach?
Który obraz MR mózgu został wykonany w sekwencji DWI?
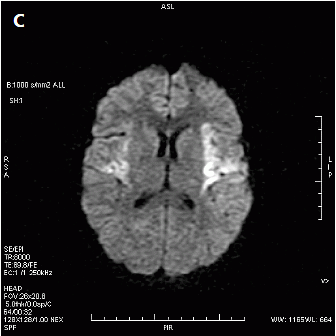
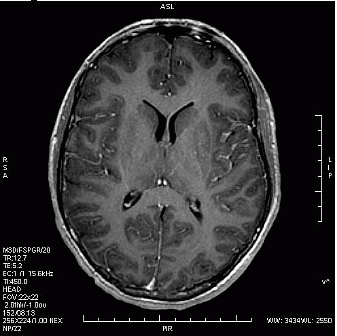
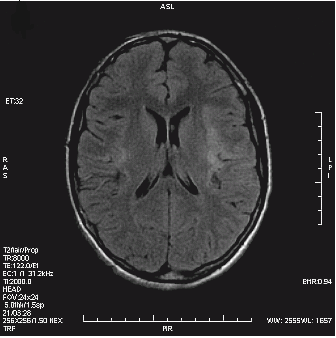
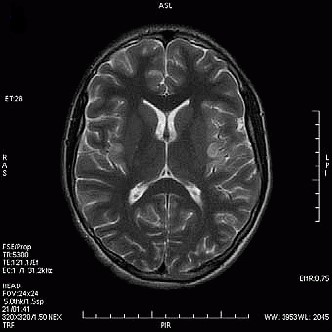
W leczeniu izotopowym tarczycy należy podać
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
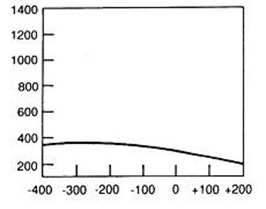
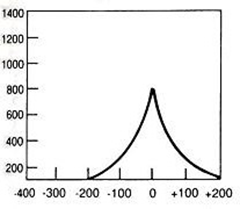
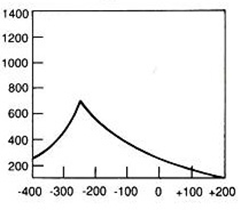
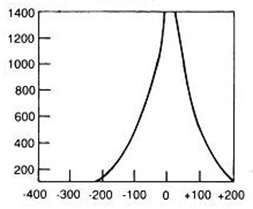
Na radiogramie uwidoczniono
Które obszary napromieniowania powinien określić lekarz radioterapeuta u pacjenta z nowotworem stercza po wcześniejszej prostatektomii?
Która metoda leczenia onkologicznego zaliczana jest do leczenia systemowego?
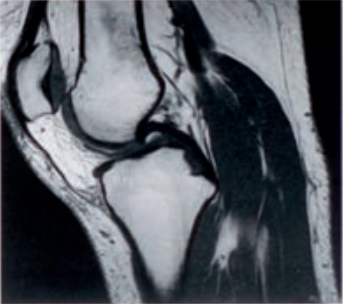
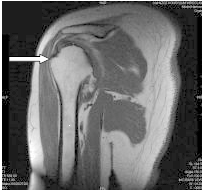
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
W badaniu audiometrycznym do oceny przewodnictwa kostnego wybranego ucha słuchawkę kostną należy przyłożyć do
Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
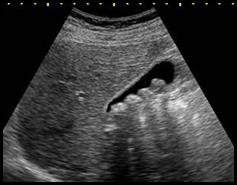
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
Audiometria impedancyjna polega na pomiarze
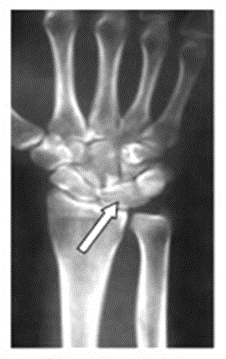
Na zamieszczonym obrazie radiologicznym nadgarstka strzałką wskazano kość
Diagnozowanie metodą PET oparte jest na zjawisku
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
Rytm alfa i beta rejestruje się podczas badania
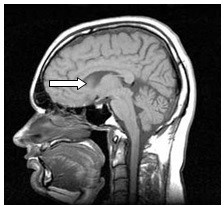
Którą strukturę anatomiczną oznaczono na obrazie rezonansu magnetycznego?
Planowany obszar napromieniania PTV obejmuje
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
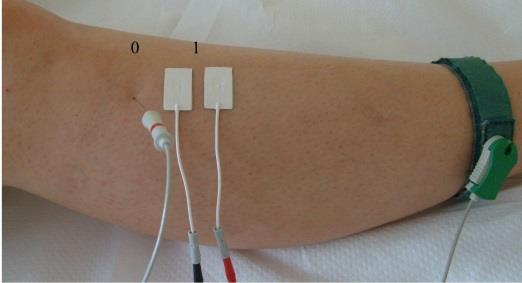
Na ilustracji przedstawiono przygotowanie pacjenta do badania
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
Strzałką na schemacie oznaczono