Pytanie 1
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
Obrazowanie w sekwencjach STIR, FLAIR, SE wykonywane jest w badaniu
Zadaniem technika elektroradiologii w pracowni badań naczyniowych jest
Planowany obszar napromieniania PTV obejmuje
Cholangiografia to badanie radiologiczne
Pielografia zstępująca umożliwia diagnostykę
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
W radiologii stomatologicznej ząb o numerze 23 to kieł
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
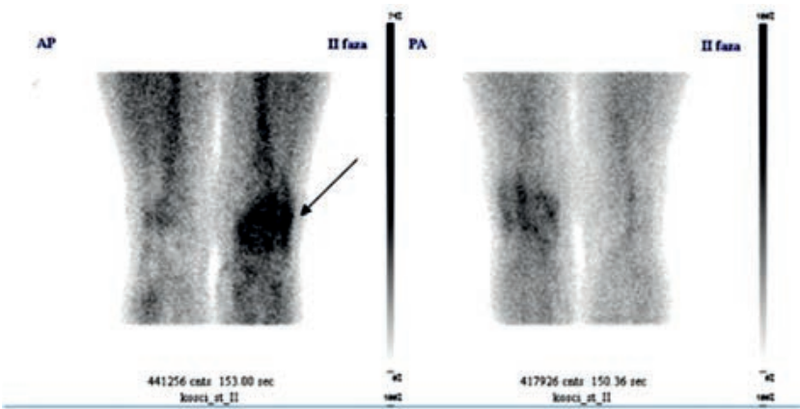
Na przedstawionym scyntygramie ukazano duży obszar
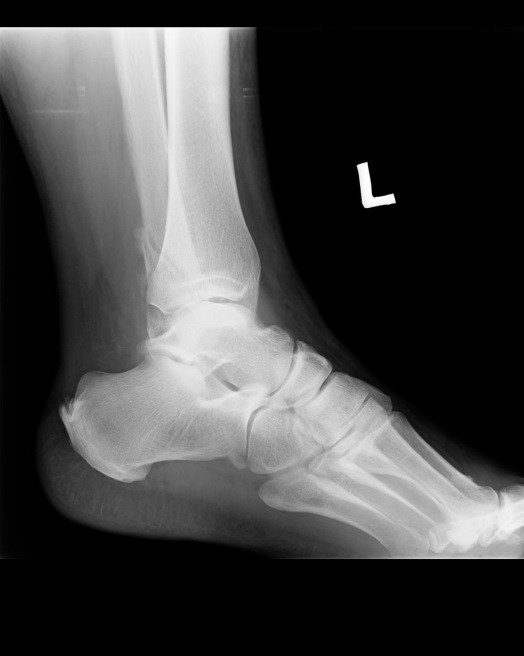
Na obrazie radiologicznym uwidoczniono złamanie kości
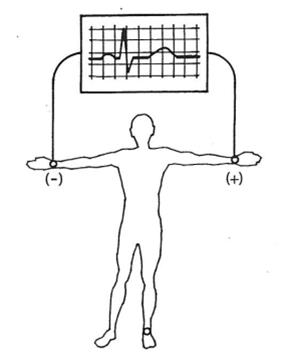
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
„Ognisko zimne” w obrazie scyntygraficznym oznacza
Rozpraszanie promieniowania X, w wyniku którego następuje zwiększenie długości fali promieniowania, to zjawisko
Przy podejrzeniu ciała obcego w oczodole należy wykonać
W obrazowaniu MR wykorzystuje się moment magnetyczny
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Cholangiografia to badanie radiologiczne
Urografia polega na
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?
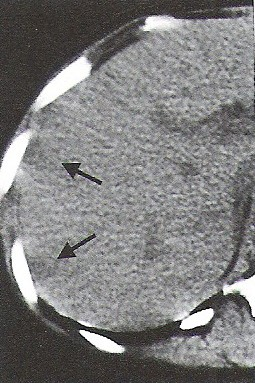
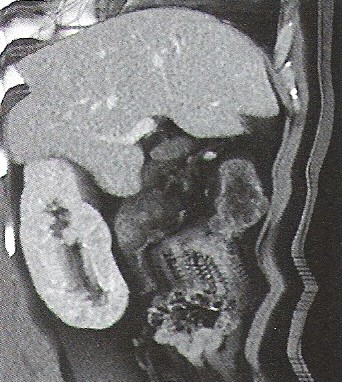

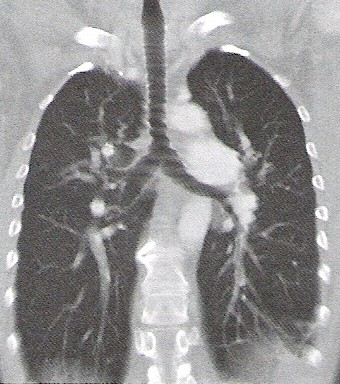
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
Fotostymulacja wykonywana jest podczas badania
Który artefakt uwidoczniono na skanie RM głowy?
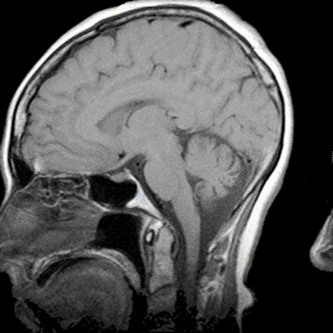
Który radioizotop jest emiterem promieniowania alfa?
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
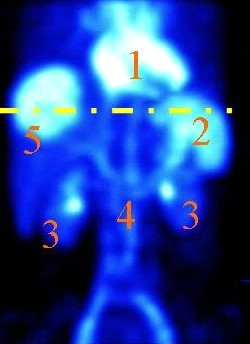
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
Które badanie, zgodnie z zakresem kompetencji, może samodzielnie wykonać technik elektroradiolog?
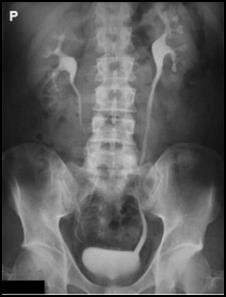
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
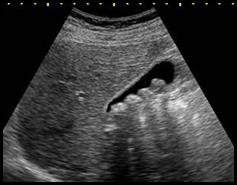
Którą strukturę anatomiczną uwidoczniono na zamieszczonym obrazie USG?
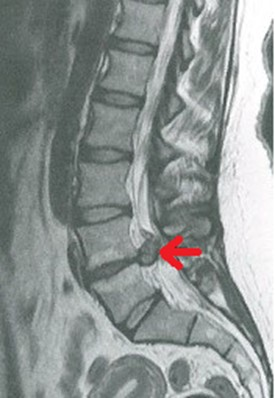
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano
Jak przebiega promień centralny w projekcji AP czaszki?
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki