Pytanie 1
Czułość bezwzględna wagi definiuje się jako
Wynik: 0/40 punktów (0,0%)
Wymagane minimum: 20 punktów (50%)
Czułość bezwzględna wagi definiuje się jako
Substancje kancerogenne to
Brak odpowiedzi na to pytanie.
W wyniku rozkładu 100 g węglanu wapnia, otrzymano 25 g tlenku wapnia. Wydajność procentowa reakcji wynosi
| MCaCO3 = 100g / mol | MCaO = 56g / mol |
Brak odpowiedzi na to pytanie.
Sód metaliczny powinien być przechowywany w laboratorium
Brak odpowiedzi na to pytanie.
Przedstawiono wyciąg z karty charakterystyki substancji chemicznej. Na podstawie informacji zawartej w zamieszczonym fragmencie karty wskaż wzór chemiczny substancji, której można użyć jako materiału neutralizującego lodowaty kwas octowy.
Kwas octowy lodowaty 99,5% Materiały zapobiegające rozprzestrzenianiu się skażenia i służące do usuwania skażenia Jeżeli to możliwe i bezpieczne, zlikwidować lub ograniczyć wyciek (uszczelnić, zamknąć dopływ cieczy, uszkodzone opakowanie umieścić w opakowaniu awaryjnym). Ograniczyć rozprzestrzenianie się rozlewiska przez obwałowanie terenu; zebrane duże ilości cieczy odpompować. Małe ilości rozlanej cieczy przysypać niepalnym materiałem chłonnym (ziemia, piasek oraz materiałami neutralizującymi kwasy, np. węglanem wapnia lub sodu, zmielonym wapieniem, dolomitem), zebrać do zamykanego pojemnika i przekazać do zniszczenia. Zanieczyszczoną powierzchnię spłukać wodą. Popłuczyny zebrać i usunąć jako odpad niebezpieczny. |
Brak odpowiedzi na to pytanie.
Sączenie na gorąco powinno być użyte, aby
Brak odpowiedzi na to pytanie.
Na rysunku przedstawiono wagę

Brak odpowiedzi na to pytanie.
Odważka analityczna wodorotlenku sodu, przygotowana fabrycznie, zawiera 0,1 mola NaOH. Jaką objętość wody destylowanej należy dodać w kolbie miarowej, aby uzyskać roztwór wodorotlenku sodu o stężeniu 0,0500 mol/dm3?
Brak odpowiedzi na to pytanie.
Fosfor biały, z uwagi na swoje właściwości, powinien być przechowywany
Brak odpowiedzi na to pytanie.
W jakiej standardowej temperaturze są kalibrowane szklane naczynia pomiarowe?
Brak odpowiedzi na to pytanie.
W procesie oddzielania osadu od roztworu, po przeniesieniu osadu na sączek, najpierw należy go
Brak odpowiedzi na to pytanie.
Aby uzyskać wodorotlenek wapnia, odważono 30 g węglanu wapnia, który następnie wyprażono. Powstały tlenek wapnia dodano do 100 cm3 wody, a otrzymany osad wysuszono i zważono, uzyskując 18,5 g wodorotlenku wapnia. Jaką wydajność miała ta reakcja?
Ca – 40 g/mol; O – 16 g/mol; C – 12 g/mol; H – 1 g/mol
Brak odpowiedzi na to pytanie.
W wyniku reakcji 100 g azotanu(V) ołowiu(II) z jodkiem potasu otrzymano 120 g jodku ołowiu(II). Wydajność reakcji wyniosła
| Pb(NO3)2 + 2KI → PbI2 + 2KNO3 | |
| (MPb(NO3)2 = 331 g/mol, MKI = 166 g/mol, MPbI2 = 461 g/mol, MKNO3 = 101 g/mol) |
Brak odpowiedzi na to pytanie.
Proces oddzielania cieczy od osadu nazywa się
Brak odpowiedzi na to pytanie.
Aby oczyścić zwęglone osady w probówce, należy zastosować
Brak odpowiedzi na to pytanie.
Aby przygotować 250 cm3 roztworu wodorotlenku potasu o stężeniu 0,25 mola, potrzebne będzie
Brak odpowiedzi na to pytanie.
Jakiego koloru nabierze lakmus w roztworze NaOH?
Brak odpowiedzi na to pytanie.
Naczynia miarowe o kształcie rurek poszerzonych w środku, z wąskim i wydłużonym dolnym końcem, przeznaczone do pobierania i transportowania cieczy o ściśle określonej objętości, to
Brak odpowiedzi na to pytanie.
Czego się używa w produkcji z porcelany?
Brak odpowiedzi na to pytanie.
Określ, jakie informacje powinny być zarejestrowane w ewidencji wydania substancji niebezpiecznych, stosowanych w badaniach laboratoryjnych?
Brak odpowiedzi na to pytanie.
Jakie jest stężenie procentowe roztworu uzyskanego poprzez rozpuszczenie 25 g jodku potasu w 100 cm3 destylowanej wody (o gęstości 1 g/cm3)?
Brak odpowiedzi na to pytanie.
Wybierz spośród wymienionych właściwości tę, która nie dotyczy naczyń kwarcowych.
Brak odpowiedzi na to pytanie.
Reakcja neutralizacji wodorotlenku sodu z kwasem solnym zrealizowana jest zgodnie z równaniem:
NaOH + HCl → NaCl + H2O Masy molowe: MNaOH = 40 g/mol, MHCl = 36,5 g/mol Aby zneutralizować 10 g wodorotlenku sodu, wymagane jest
Brak odpowiedzi na to pytanie.
Oblicz stężenie molowe 250 cm3 roztworu NaOH, w którym znajduje się 0,5 g substancji. Masa molowa NaOH wynosi 40 g/mol
Brak odpowiedzi na to pytanie.
Na podstawie zmierzonej temperatury topnienia można określić związek organiczny oraz ustalić jego
Brak odpowiedzi na to pytanie.
Piknometr służy do określania
Brak odpowiedzi na to pytanie.
Roztwory, które wykorzystuje się do kalibracji pehametrów, to
Brak odpowiedzi na to pytanie.
Aby uzyskać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy rozpuścić w wodzie destylowanej i dopełnić kolbę wodą destylowaną do zaznaczonej kreski.
Brak odpowiedzi na to pytanie.
Podaj nazwę reagentu chemicznego, który w specyficznych warunkach reaguje tylko z jednym jonem, pierwiastkiem lub związkiem chemicznym?
Brak odpowiedzi na to pytanie.
Podczas oznaczania kwasu siarkowego zachodzi reakcja:
H2SO4 + 2NaOH → Na2SO4 + 2H2OZgodnie z zamieszczoną instrukcją, roztwór poreakcyjny należy
| Fragmenty instrukcji zbierania, utylizacji i eliminacji odpadów chemicznych | |
|---|---|
| Lista substancji, które mogą być usunięte z odpadami komunalnymi w postaci stałej, lub wprowadzone do systemu kanalizacyjnego w postaci rozcieńczonych roztworów wodnych, o ile ich ilość nie przekracza jednorazowo 100 g. | |
| Związki nieorganiczne Siarczany sodu, potasu, magnezu, wapnia, amonu | |
| Kwasy nieorganiczne Stężone kwasy ostrożnie rozcieńczyć przez wkroplenie z równoczesnym mieszaniem do wody z lodem, a następnie zneutralizować roztworem wodorotlenku sodowego. Po neutralizacji doprowadzić pH roztworu do zakresu 6-8 przelać do pojemnika S. Małe ilości kwasów takich jak siarkowy, solny, azotowy czy fosforowy (nie więcej niż 10 g) po rozcieńczeniu wodą i neutralizacji roztworem wodorotlenku sodowego oraz doprowadzeniu pH takiego roztworu do zakresu 6-8 można wylać do zlewu i obficie spłukać wodą. | |
| Sole nieorganiczne Stałe sole nieorganiczne – pojemnik N. Obojętne roztwory soli nieorganicznych pojemnik S. Sole metali ciężkich, sole o właściwościach toksycznych – pojemnik TN. |
Brak odpowiedzi na to pytanie.
Mianowanie roztworu KMnO4 następuje według poniższej procedury:
Około 0,2 g szczawianu sodu, ważonego z dokładnością ±0,1 mg, przenosi się do kolby stożkowej, rozpuszcza w około 100 cm3 wody destylowanej, następnie dodaje się 10 cm3 roztworu kwasu siarkowego(VI) i podgrzewa do temperatury około 70 °C. Miareczkowanie przeprowadza się roztworem KMnO4 do momentu uzyskania trwałego, jasnoróżowego koloru.
Powyższa procedura odnosi się do miareczkowania
Brak odpowiedzi na to pytanie.
W karcie charakterystyki chemikaliów znajduje się informacja o przechowywaniu dichromianu(VI) potasu: .. powinien być przechowywany w odpowiednio oznakowanych, szczelnie zamkniętych pojemnikach, w chłodnym, suchym i dobrze wentylowanym magazynie, który posiada instalację elektryczną i wentylacyjną. Z tego opisu wynika, że ten chemikal może być przechowywany
Brak odpowiedzi na to pytanie.
Jak przebiega procedura unieszkodliwiania rozlanego kwasu siarkowego(VI)?
Brak odpowiedzi na to pytanie.
Z etykiety wynika, że dany związek mógł być

Brak odpowiedzi na to pytanie.
Aby oddzielić mieszankę etanolu i wody, konieczne jest przeprowadzenie procesu
Brak odpowiedzi na to pytanie.
W probówce połączono roztwory CuSO4 oraz NaOH. Powstał niebieski osad, który po podgrzaniu zmienił kolor na czarny. Czarnym osadem jest
Brak odpowiedzi na to pytanie.
Transportuje się pobrane próbki wody do analiz fizykochemicznych
Brak odpowiedzi na to pytanie.
Zdjęcie przedstawia oparzenie cieplne
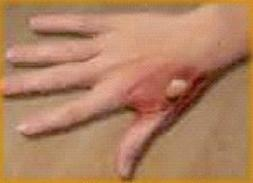
Brak odpowiedzi na to pytanie.
W przypadku zanieczyszczeń szklanych naczyń osadami o charakterze nieorganicznym, takimi jak wodorotlenki, tlenki oraz węglany, do ich oczyszczania używa się
Brak odpowiedzi na to pytanie.
Oblicz, jaką ilość węglanu sodu w gramach należy przygotować, aby uzyskać 500 cm3 roztworu tej soli o stężeniu 0,1000 mol/dm3.
MNa = 23 g/mol, MC = 12 g/mol, MO = 16 g/mol
Brak odpowiedzi na to pytanie.