Pytanie 1
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wynik: 0/40 punktów (0,0%)
Wymagane minimum: 20 punktów (50%)
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na schemacie przedstawiającym sposób pobierania hodowli do badań ze skosu agarowego, literą A oznaczono
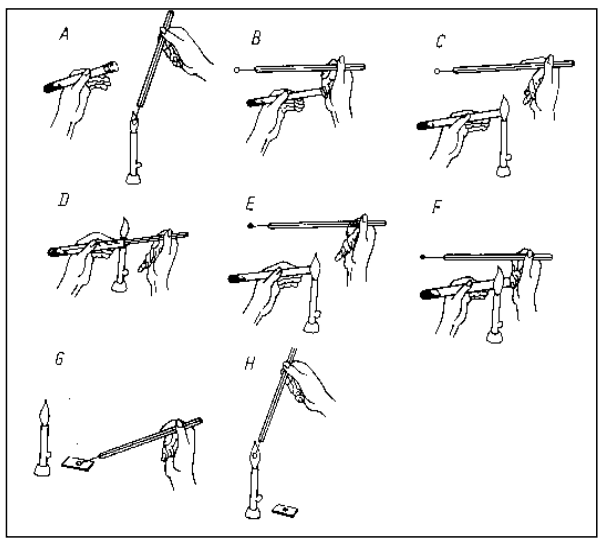
Brak odpowiedzi na to pytanie.
W jakich oznaczeniach analitycznych wykorzystuje się fenoloftaleinę jako wskaźnik?
Brak odpowiedzi na to pytanie.
Które ilustracje przedstawiają formy cylindryczne bakterii?
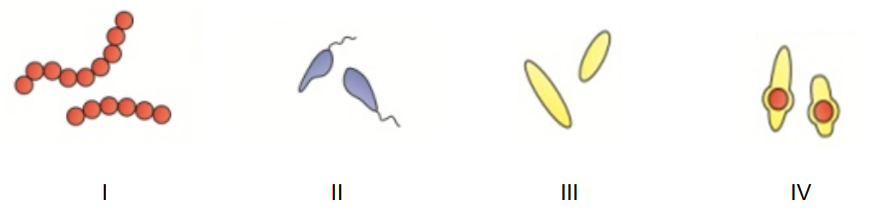
Brak odpowiedzi na to pytanie.
Prawidłowy przebieg reakcji redukcji jonu MnO4- w środowisku kwaśnym przedstawia równanie
| A. | MnO4- + H+ + e- → MnO42- + H+ |
| B. | MnO4- + 8H+ + 5e- → Mn2+ + 4H2O |
| C. | MnO4- + 4H+ + 3e- → MnO2 + 2H2O |
| D. | 2MnO4- + 10H+ + 8e- → Mn2O3 + 5H2O |
Brak odpowiedzi na to pytanie.
Jaką metodą określa się stężenie cukrów redukujących w produktach owocowych?
Brak odpowiedzi na to pytanie.
Konduktywność elektrolityczna wody destylowanej stosowanej w laboratorium chemicznym wynosi 0,001 mS cm-1. Z analizy danych przedstawionych na rysunku wynika, że woda ta jest
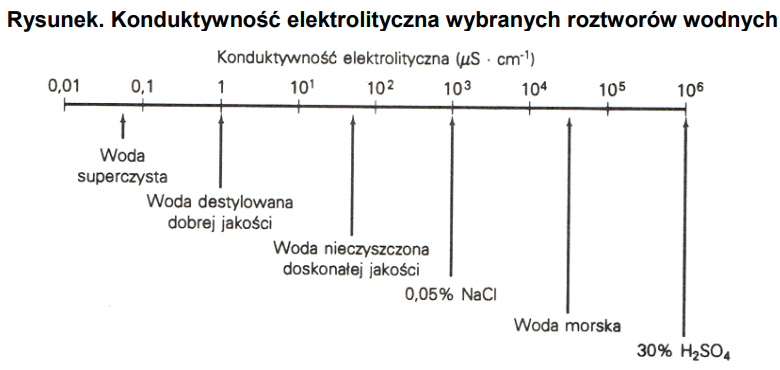
Brak odpowiedzi na to pytanie.
Metalowe wskaźniki są wykorzystywane w analizach
Brak odpowiedzi na to pytanie.
Substancją wskaźnikową w miareczkowaniu alkacymetrycznym nie jest
Brak odpowiedzi na to pytanie.
W wyniku badań mikrobiologicznych wody przeznaczonej do produkcji soków, po 3 dniach inkubacji stwierdzono w 1 ml próbki 100 j.t.k. bakterii, w tym 2 j.t.k Escherichia coli.
Ustal jakość wody na podstawie informacji zamieszczonych w tabeli.
| Wymagania mikrobiologiczne, jakim powinna odpowiadać woda | ||
|---|---|---|
| Lp. | Parametr | Najwyższa dopuszczalna wartość liczby jednostek tworzących kolonię [j.t.k] |
| 1 | Escherichia coli | 0 |
| 2 | Enterokoki | 0 |
| 3 | Pseudomonas aeruginosa | 0 |
| 4 | Ogólna liczba mikroorganizmów w (36±2) °C po 48h | 20 |
| 5 | Ogólna liczba mikroorganizmów w (22±2) °C po 72h | 100 |
Brak odpowiedzi na to pytanie.
Reakcja, na której opiera się oznaczenie liczby zmydlania (LZ) tłuszczów, to
Brak odpowiedzi na to pytanie.
Przedstawiony wzór opisuje titrant stosowany podczas miareczkowania
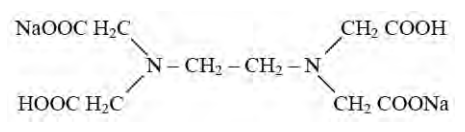
Brak odpowiedzi na to pytanie.
Dział analizy objętościowej, który dotyczy reakcji zobojętniania, to
Brak odpowiedzi na to pytanie.
Czym zajmuje się System Analizy Zagrożeń i Krytycznych Punktów Kontroli (HACCP)?
Brak odpowiedzi na to pytanie.
Zjawisko opisane w zamieszczonej informacji to
| Jeżeli w wodzie zostanie rozpuszczona α-D-glukopiranoza, to roztwór tuż po rozpuszczeniu wykazuje skręcalność właściwą [α]D = +112,2°, lecz w miarę upływu czasu skręcalność ta stopniowo spada do wartości charakterystycznej w stanie równowagi, mianowicie [α]D = +52,7° |
Brak odpowiedzi na to pytanie.
Jakie urządzenie jest wykorzystywane do inkubacji próbek mikrobiologicznych?
Brak odpowiedzi na to pytanie.
Podłoże, które zawiera wyłącznie substancje niezbędne do rozwoju mikroorganizmów, określane jest jako
Brak odpowiedzi na to pytanie.
Czym jest eluent?
Brak odpowiedzi na to pytanie.
Jaką wartość współmierności ma kolba miarowa o objętości 500 cm3 oraz pipeta jednomiarowa o objętości 20 cm3?
Brak odpowiedzi na to pytanie.
Roztwór tiocyjanianu amonu NH4SCN jest wykorzystywany jako titrant w oznaczaniu bromków przy użyciu metody miareczkowania?
Brak odpowiedzi na to pytanie.
Analiza wody basenowej w celu wykrycia bakterii polega na podgrzewaniu próbki w inkubatorze przez 48 godzin w temperaturze 36±2°C. Jaki proces jest opisany?
Brak odpowiedzi na to pytanie.
W celu preparatywnego rozdzielania aminokwasów wykorzystuje się metodę elektroforezy, która bazuje na
Brak odpowiedzi na to pytanie.
Na rysunku przedstawiono graficzną interpretację zależności wynikających z prawa
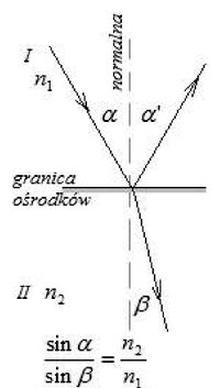
Brak odpowiedzi na to pytanie.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakiego koloru płomień uzyskuje się dzięki sole miedzi?
Brak odpowiedzi na to pytanie.
Który z kationów nadaje płomieniowi palnika barwę ceglastoczerwoną?
Brak odpowiedzi na to pytanie.
Do optycznych metod instrumentalnych wykorzystywanych w chemicznej analizie zalicza się
Brak odpowiedzi na to pytanie.
W dwóch niezidentyfikowanych probówkach znajdują się roztwory: w jednej - glukozy, a w drugiej - sacharozy. Jakiego odczynnika należy użyć, aby rozpoznać glukozę?
Brak odpowiedzi na to pytanie.
Metoda, która polega na przemieszczaniu się naładowanych cząstek do odpowiednich elektrod podłączonych do źródła prądu stałego, używana m.in. do separacji białek, nazywa się
Brak odpowiedzi na to pytanie.
Mangan ulega utlenieniu w reakcji
| A. | Mn2+ + 2OH− → Mn(OH)2 |
| B. | 2Mn(OH)2 + O2 → 2 MnO(OH)2 |
| C. | MnO(OH)2 + 4H+ → Mn4+ + 3H2O |
| D. | Mn4+ + 2I− → Mn2+ + I2 |
Brak odpowiedzi na to pytanie.
Przeniesienie pasma absorpcyjnego w kierunku fal krótszych to
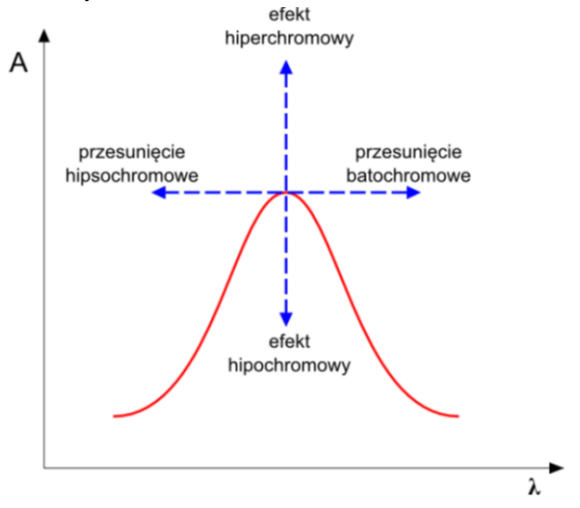
Brak odpowiedzi na to pytanie.
Jakim urządzeniem mierzy się zasolenie gleby?
Brak odpowiedzi na to pytanie.
Do wyznaczania gęstości cieczy służą przyrządy oznaczone numerami
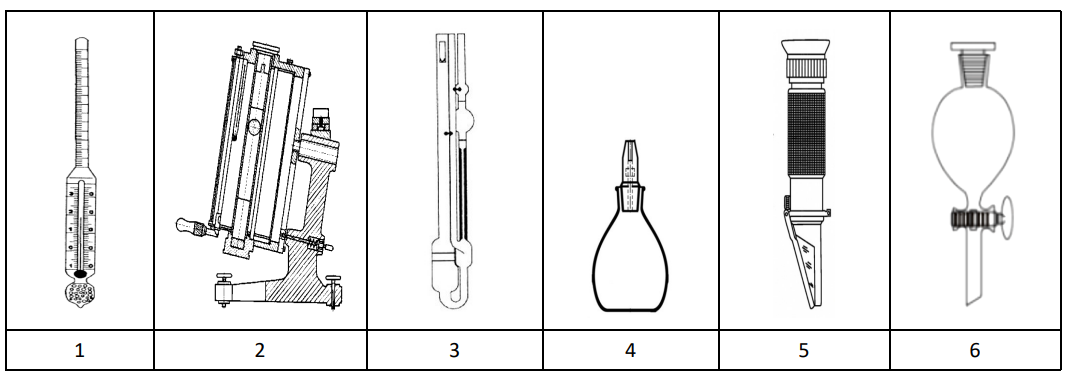
Brak odpowiedzi na to pytanie.
Oblicz stężenie glukozy w surowicy krwi, jeżeli absorbancja tej próby wynosi 0,350, a wzorzec o stężeniu 0,2 mg/ml wykazuje absorbancję 0,120.
Użyj wzoru:$$ \text{stężenie glukozy [mg/ml]} = \frac{A_p}{A_w} \cdot c_w $$gdzie:
\( A_p \) - absorbancja próbki
\( A_w \) - absorbancja wzorca
\( c_w \) - stężenie wzorca [mg/ml]
Brak odpowiedzi na to pytanie.
Wskaż nazwy sprzętów laboratoryjnych przedstawionych na rysunku.
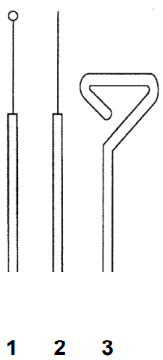
Brak odpowiedzi na to pytanie.
W celu identyfikacji cukru przeprowadzono następujące doświadczenia:
Identyfikowanym cukrem jest
| Doświadczenie | Wynik doświadczenia |
|---|---|
| Próba Trommera | pozytywna |
| Próba Tollensa | pozytywna |
| Hydroliza | nie zachodzi |
Brak odpowiedzi na to pytanie.
Jedna z analizowanych cech jakości wody ma wartość 0,8 NTU. Cechą tą jest
Brak odpowiedzi na to pytanie.
W wyniku oznaczenia wagowego otrzymano 0,2451 g tlenku żelaza(III). Ile gramów żelaza zawierała analizowana próbka?
| MFe = 55,845 g/mol, MO = 15,999 g/mol |
Brak odpowiedzi na to pytanie.
Błąd miareczkowania w oznaczeniach objętościowych nie występuje, gdy
Brak odpowiedzi na to pytanie.
W równaniu dotyczącym iloczynu rozpuszczalności siarczanu(VI) baru: Kso = [Ba2+][SO42-], jonowe stężenia Ba2+ oraz SO42- są przedstawione jako
Brak odpowiedzi na to pytanie.