Pytanie 1
Na podstawie danych w tabeli określ, jaką masę próbki należy pobrać, jeżeli wielkość ziarna wynosi 1·10-5 m.
| Wielkość ziaren lub kawałków [mm] | Poniżej 1 | 1-10 | 11-50 | Ponad 50 |
|---|---|---|---|---|
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
Wynik: 31/40 punktów (77,5%)
Wymagane minimum: 20 punktów (50%)
Na podstawie danych w tabeli określ, jaką masę próbki należy pobrać, jeżeli wielkość ziarna wynosi 1·10-5 m.
| Wielkość ziaren lub kawałków [mm] | Poniżej 1 | 1-10 | 11-50 | Ponad 50 |
|---|---|---|---|---|
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
W chemicznym laboratorium apteczka pierwszej pomocy powinna zawierać
Wybierz spośród wymienionych właściwości tę, która nie dotyczy naczyń kwarcowych.
Z 250 g benzenu (M = 78 g/mol) uzyskano 350 g nitrobenzenu (M = 123 g/mol). Jaka jest wydajność reakcji nitrowania?
Intensywna reakcja z FeCl3 jest wykorzystywana do identyfikacji
Ze względu na czystość, substancja oznakowana zamieszczoną etykietą powinna być wykorzystywana głównie do

W celu sprawdzenia stężenia kwasu siarkowego(VI) odważono 1 g badanego kwasu i przeprowadzono analizę miareczkową, w której zużyto 20,4 \( \text{cm}^3 \) roztworu NaOH.
Stężenie procentowe badanego kwasu, obliczone na podstawie wzoru wynosi
$$ C_p = \frac{0,02452 \cdot V_{NaOH}}{mp} \cdot 100\% $$gdzie:
\( C_p \) – stężenie procentowe badanego kwasu; \( \% \)
\( 0,02452 \) – współczynnik przeliczeniowy; \( \text{g/cm}^3 \)
\( V_{NaOH} \) – objętość roztworu NaOH, zużyta w miareczkowaniu; \( \text{cm}^3 \)
\( mp \) – odważka badanego kwasu; g
W którym wierszu tabeli podano ilości substancji i wody, potrzebne do sporządzenia 350 g roztworu o stężeniu 7%?
| Masa substancji | Masa wody | |
|---|---|---|
| A. | 24,5 g | 350 g |
| B. | 24,5 g | 325,5 g |
| C. | 7 g | 343 g |
| D. | 7 g | 350 g |
Oddzielanie płynnej mieszanki poprzez jej odparowanie, a potem skroplenie poszczególnych składników to
W trakcie korzystania z odczynnika opisanego na etykiecie, należy szczególnie zwrócić uwagę na zagrożenia związane
Fosfor biały, z uwagi na swoje właściwości, powinien być przechowywany
Aby rozpuścić próbkę tłuszczu o wadze 5 g, wykorzystuje się 50 cm3 mieszanki 96% alkoholu etylowego oraz eteru dietylowego, połączonych w proporcji objętościowej 1 : 2. Jakie ilości cm3 każdego ze składników są potrzebne do przygotowania 150 cm3 tej mieszanki?
Z przedstawionego opisu wynika, że kluczową właściwością próbki analitycznej jest jej
Próbka analityczna to fragment materiału stworzony z myślą o przeprowadzeniu badania lub obserwacji. Powinna odzwierciedlać przeciętny skład i cechy materiału, który jest badany.
Próbki pobrano z materiału o objętości \( 100 \, \text{m}^3 \), wysypanego z opakowania. Liczba miejsc poboru próbek pierwotnych z tego materiału wynosi:
$$ n = 0{,}5 \cdot \sqrt{V} $$ gdzie:
\( V \) – objętość jednostki badanej w \( \text{m}^3 \)
\( n \) – liczba miejsc poboru próbek
Zamieszczony piktogram odnosi się do substancji o klasie i kategorii zagrożenia:
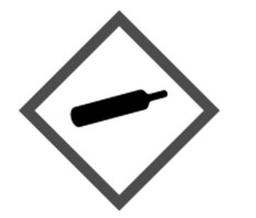
W urządzeniu Soxhleta wykonuje się
Woda, która została poddana dwukrotnej destylacji, to woda
Odpady z rozpuszczalników organicznych, takich jak benzen czy aceton, zawierające co najmniej 80% danego rozpuszczalnika, należy
Poniżej jest równanie reakcji prażenia węglanu wapnia. 200 g węglanu wapnia zawierającego 10% zanieczyszczeń poddano prażeniu. Masa otrzymanego tlenku wapnia wyniosła
| CaCO3 → CaO + CO2 |
| (MCaCO3 = 100 g/mol, MCaO = 56 g/mol, MCO2 = 44 g/mol) |
Jakie środki stosuje się do czyszczenia szkła miarowego, które zostało zanieczyszczone substancjami tłustymi?
Aby otrzymać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy
W standardowym układzie destylacyjnym, który ma ukośną chłodnicę, wykorzystuje się chłodnicę
Na etykietach substancji chemicznych można znaleźć oznaczenia literowe R i S (zgodnie z regulacjami CLP: H i P), które wskazują
Błąd związany z odczytem poziomu cieczy w kolbie miarowej, spowodowany niewłaściwą pozycją oka w stosunku do skali, nazywany jest błędem
Jaką objętość roztworu NaOH o stężeniu 1 mol/dm3 należy użyć, aby przygotować 50 cm3 roztworu NaOH o stężeniu 0,4 mol/dm3?
Proces przesiewania próbki prowadzi się za pomocą urządzenia przedstawionego na rysunku

Który zestaw zawiera niezbędne urządzenia laboratoryjne do przygotowania 10% (m/m) roztworu NaCl?
Aby przygotować 500 g roztworu o stężeniu 10% (m/m), ile substancji należy odważyć?
Zaleca się schładzanie próbek wody transportowanych do laboratorium do temperatury
Ile masy kwasu mrówkowego jest wymagane do uzyskania 11,2 dm3 tlenku węgla(II) (w warunkach normalnych) w procesie odwodnienia kwasu mrówkowego (M = 46 g/mol) za pomocą kwasu siarkowego(VI), zakładając efektywność procesu na poziomie 70%?
Na etykiecie kwasu siarkowego(VI) znajduje się piktogram pokazany na rysunku. Oznacza to, że substancja ta jest
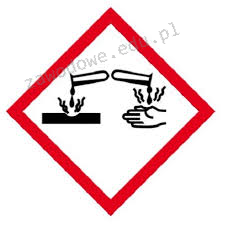
Próbka, której celem jest ustalenie poziomu składników, dla których oznaczenia przygotowane przez różne laboratoria są niezgodne, to próbka
Na zdjęciu przedstawiono proces

Na rysunku przedstawiono
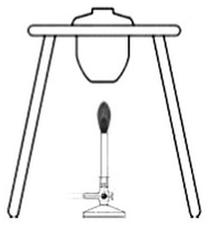
Przedstawiony na rysunku zagłębnik stosuje się do pobierania próbek
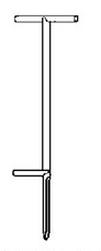
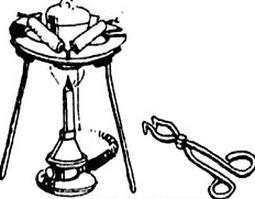
Przedstawiony zestaw stosowany jest w laboratorium do przeprowadzenia procesu
Odważka analityczna wodorotlenku sodu, przygotowana fabrycznie, zawiera 0,1 mola NaOH. Jaką objętość wody destylowanej należy dodać w kolbie miarowej, aby uzyskać roztwór wodorotlenku sodu o stężeniu 0,0500 mol/dm3?
Miesięczne zapotrzebowanie laboratorium analitycznego na 2-propanol wynosi 500 cm3. Na jak długo wystarczy ta substancja?
W laboratorium chemicznym przewody instalacji rurowych są oznaczane różnymi kolorami, zgodnie z obowiązującymi normami. Polska Norma PN-70 N-01270/30 określa kolor dla wody jako
Instrukcja dotycząca przygotowania wzorcowego roztworu NaCl
0,8242 g NaCl, które wcześniej wysuszono w temperaturze 140 °C do stałej masy, należy rozpuścić w kolbie miarowej o pojemności 1 dm3 w wodzie podwójnie destylowanej, a następnie uzupełnić do kreski tym samym rodzajem wody.
Z treści instrukcji wynika, że odpowiednio skompletowany sprzęt wymagany do sporządzenia wzorcowego roztworu NaCl, oprócz naczynia wagowego, powinien zawierać