Pytanie 1
Aby przygotować mianowany roztwór KMnO4, należy odważyć wysuszone Na2C2O4 o masie zbliżonej do 250 mg, z dokładnością wynoszącą 1 mg. Jaką masę powinna mieć prawidłowo przygotowana odważka?
Wynik: 36/40 punktów (90,0%)
Wymagane minimum: 20 punktów (50%)
Aby przygotować mianowany roztwór KMnO4, należy odważyć wysuszone Na2C2O4 o masie zbliżonej do 250 mg, z dokładnością wynoszącą 1 mg. Jaką masę powinna mieć prawidłowo przygotowana odważka?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Intensywna reakcja z FeCl3 jest wykorzystywana do identyfikacji
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Roztwory o ściśle określonym stężeniu, używane w analizach miareczkowych, nazywamy
Zaleca się schładzanie próbek wody transportowanych do laboratorium do temperatury
Reakcja miedzi metalicznej z stężonym kwasem azotowym(V) prowadzi do powstania azotanu(V) miedzi(II) oraz jakiego związku?
Z próbki zawierającej siarczany(VI) należy najpierw wydzielić metodą filtracji zanieczyszczenia, które są nierozpuszczalne w wodzie. Dokładność wypłukania tych zanieczyszczeń weryfikuje się za pomocą roztworu
Naważkę NaOH o masie 0,0400 g rozpuścić w małej ilości wody, a następnie przelać ten roztwór do kolby miarowej o pojemności 500 cm3 i uzupełnić kolbę miarową wodą do tzw. kreski. Masa molowa NaOH wynosi 40,0 g/mol. Jakie jest stężenie molowe przygotowanego roztworu?
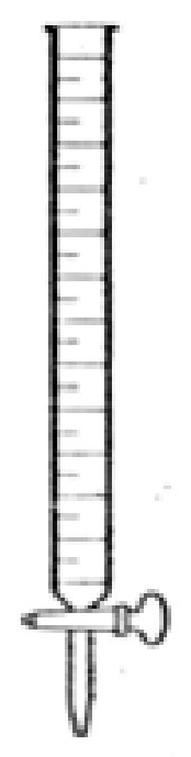
Dla cieczy bezbarwnej odczyt w biurecie pokazanej na rysunku wynosi

Aby w badanej próbie w trakcie zmiany pH nastąpiła zmiana barwy na malinową, należy użyć
| Zmiany barw najważniejszych wskaźników kwasowo-zasadowych | ||||
|---|---|---|---|---|
| Wskaźnik | Barwa w środowisku | Zakres pH zmiany barwy | ||
| Kwasowym | Obojętnym | Zasadowym | ||
| oranż metylowy | czerwona | żółta | żółta | 3,2÷4,4 |
| lakmus (mieszanina substancji) | czerwona | fioletowa | niebieska | 4,5÷8,2 |
| fenoloftaleina | bezbarwna | bezbarwna | malinowa | 8,2÷10,0 |
| wskaźnik uniwersalny (mieszanina substancji) | czerwona (silnie kwaśne) pomarańczowa (słabo kwaśne) | żółta | niebieska (silnie zasadowe) zielona (słabo zasadowe) | co jeden stopień skali |
| herbata | żółta | czerwona-brunatna | brązowa | |
| sok z czerwonej kapusty | fioletowa | niebieska | zielona | |
Jakie urządzenie służy do pomiaru temperatury topnienia substancji chemicznych?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Gęstość próbki cieczy wyznacza się przy użyciu
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wskaż, do jakiego typu należą zamieszczone równania reakcji.
| I. 2 Mg + O2 → 2 MgO |
| II. 2 KMnO4 → K2MnO4 + MnO2 + O2 |
| III. BaCl2 + H2SO4→ BaSO4 + 2 HCl |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wodę do badań mikrobiologicznych powinno się pobierać do butelek
Substancje kancerogenne to
Skuteczny środek do osuszania
Metoda oczyszczania substancji, która opiera się na różnicy w rozpuszczalności substancji docelowej oraz zanieczyszczeń w zastosowanym rozpuszczalniku, nosi nazwę
Próbka pobrana z próbki ogólnej, która odzwierciedla cechy partii produktu, określa się jako próbka
Część partii pobrana w sposób jednorazowy z jednego źródła towaru zapakowanego lub z jednego opakowania jednostkowego określana jest mianem próbki
Rysunek przedstawia etapy zmniejszania próbki ogólnej. Jest to metoda
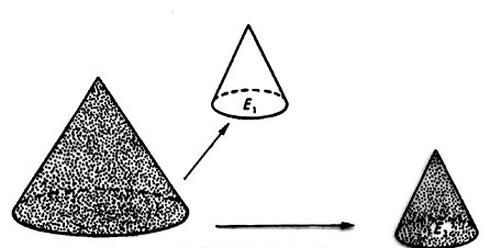
Na podstawie informacji zawartych w tabeli wskaż mieszaninę oziębiającą o temperaturze -21 °C.
| Temperatura mieszaniny | Skład mieszaniny | Stosunek masowy |
| -15 °C | lód + octan sodu | 10:9 |
| -18 °C | lód + chlorek amonu | 10:3 |
| -21 °C | lód + chlorek sodu | 3:1 |
| -25 °C | lód + azotan amonu | 1:9 |
Przedstawiony sprzęt szklany to
Na podstawie danych w tabeli próbkę, w której będzie oznaczany BZT, należy przechowywać
| Oznaczany parametr | Rodzaj naczynia do przechowywania | Sposób utrwalania | Dopuszczalny czas przechowywania |
|---|---|---|---|
| barwa | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C | 24 h |
| fosforany ogólne | szklane lub polietylenowe | - zakwaszenie kwasem siarkowym(VI) - schłodzenie do temperatury 2-5°C | 4 h 48 h |
| BZT | szklane | - schłodzenie do temperatury 2-5°C - przechowywanie w ciemności | 24 h |
| azot azotanowy(V) | szklane lub polietylenowe | - schłodzenie do temperatury 2-5°C - dodanie 2 cm3 chloroformu do 1 dm3 próbki | 24 h 48 h |
Z analizy wykresu wynika, że substancją o najniższej rozpuszczalności w wodzie w temperaturze 100°C jest
Aby przygotować 250 cm3 0,2-molowego roztworu wodorotlenku sodu, należy odważyć
| MNaOH = 40g / mol |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Woda używana w laboratorium chemicznym, uzyskana poprzez filtrację przez wymieniacz jonowy, jest określana mianem wody
Sączenie na gorąco powinno być użyte, aby
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Do metalowego sprzętu laboratoryjnego używanego w praktykach analitycznych zalicza się
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Zgodnie z instrukcją dotyczącą pobierania próbek nawozów (na podstawie normy PN-EN 12579:2001), liczbę punktów pobierania próbek pierwotnych ustala się według wzoru nsp = 0,5·√V, gdzie V oznacza objętość jednostki badanej w m3. Wartość nsp zaokrągla się do liczby całkowitej, a dodatkowo nie może być mniejsza niż 12 ani większa niż 30.
Dlatego dla objętości V = 4900 m3, nsp wynosi
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.