Pytanie 1
Na etykiecie kwasu siarkowego(VI) znajduje się zapis:
Określ gęstość kwasu siarkowego(VI).
KWAS SIARKOWY MIN. 95% CZ.D.A. H2SO4 M = 98,08 g/mol 1 l – 1,84 kg |
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
Na etykiecie kwasu siarkowego(VI) znajduje się zapis:
Określ gęstość kwasu siarkowego(VI).
KWAS SIARKOWY MIN. 95% CZ.D.A. H2SO4 M = 98,08 g/mol 1 l – 1,84 kg |
Jakim kolorem oznacza się instalację gazową w laboratorium analitycznym?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jaką masę NaCl uzyskuje się poprzez odparowanie do sucha 250 g roztworu 10%?
W trakcie kalibracji stężenia roztworu kwasu solnego na przynajmniej przygotowany roztwór zasady sodowej ma miejsce reakcja
Który sposób przechowywania próbek żywności jest niezgodny z Rozporządzeniem Ministra Zdrowia?
| Fragment Rozporządzenia Ministra Zdrowia w sprawie pobierania i przechowywania próbek żywności przez zakłady żywienia zbiorowego typu zamkniętego |
| (...) Zakład przechowuje próbki, przez co najmniej 3 dni, licząc od chwili, kiedy cała partia została spożyta w miejscu wyłącznym właściwym do tego celu oraz w warunkach zapewniających utrzymanie temperatury +4°C lub niższej, w zależności od przechowywanego produktu. Miejsce przechowywania próbek musi być tak zabezpieczone, aby dostęp do niego posiadał tylko kierujący zakładem lub osoba przez niego upoważniona. |
Jaką objętość powinna mieć kolba miarowa, aby przygotować mianowany roztwór NaOH o stężeniu 0,050 M z analitycznej odważki, która zawiera 0,1 mola NaOH?
Masa molowa kwasu azotowego(V) wynosi 63,0 g/mol. Jakie jest stężenie molowe 20% roztworu tego kwasu o gęstości 1,1 g/cm3?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
W tabeli przedstawiono wymiary, jakie powinny mieć oznaczenia opakowań substancji niebezpiecznych.
Korzystając z informacji w tabeli, określ minimalne wymiary, jakie powinno mieć oznaczenie dla cysterny o pojemności 32840 dm3.
| Pojemność opakowania | Wymiary (w centymetrach) |
|---|---|
| Nieprzekraczająca 3 litrów | co najmniej 5,2 x 7,4 |
| Ponad 3 litry, ale nieprzekraczająca 50 litrów | co najmniej 7,4 x 10,5 |
| Ponad 50 litrów, ale nieprzekraczająca 500 litrów | co najmniej 10,5 x 14,8 |
| Ponad 500 litrów | co najmniej 14,8 x 21,0 |
Na rysunku numerami rzymskimi oznaczono
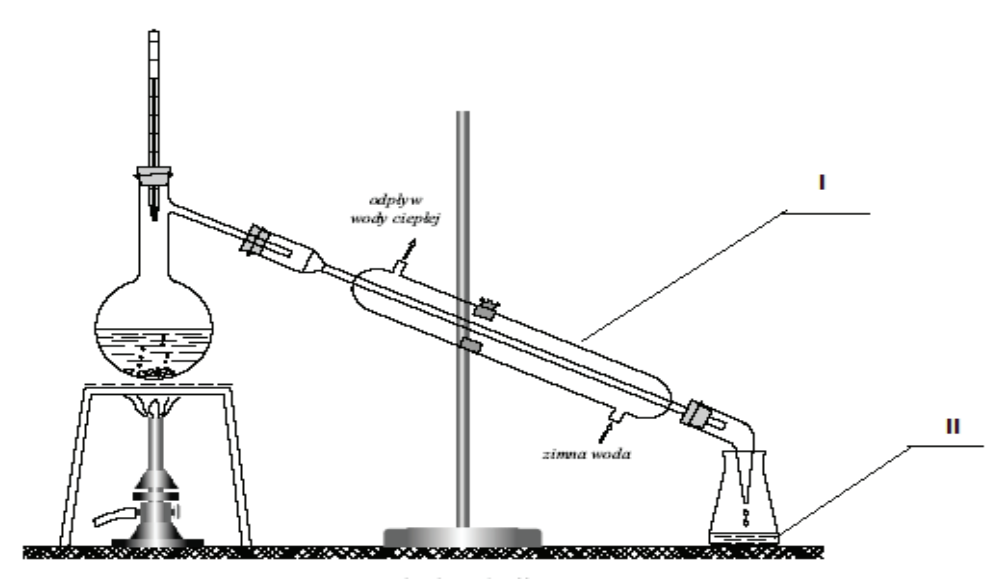
Sposoby utrwalania i przechowywania próbek wody przeznaczonych do badań fizykochemicznych.
Próbkę wody przeznaczoną do oznaczenia zawartości metali poddaje się utrwalaniu za pomocą
| Oznaczenie | Sposób utrwalania i przechowywania |
|---|---|
| Barwa | Przechowywać w ciemności |
| Mętność | Przechowywać w ciemności |
| Twardość | pH = 3 z użyciem HNO3 |
| OWO | 0,7 ml HCl/30 ml próbki |
| ChZT | pH 1- 2 z użyciem H2SO4 |
| Fosfor | Przechowywać w temperaturze 1-5°C |
| Glin | pH 1-2 z użyciem HNO3 |
| Żelazo | pH 1-2 z użyciem HNO3 |
| Utlenialność | pH1-2 z użyciem H2SO4, Przechowywać w ciemności |
Oblicz stężenie molowe 250 cm3 roztworu NaOH, w którym znajduje się 0,5 g substancji. Masa molowa NaOH wynosi 40 g/mol
Z próbek przygotowuje się ogólną próbkę
Procedura oznaczenia kwasowości mleka. Do wykonania analizy, zgodnie z powyższą procedurą, potrzebne są
| Do kolby stożkowej o pojemności 300 cm3 pobrać dokładnie 25 cm3 badanego mleka i rozcieńczyć wodą destylowaną do objętości 50 cm3. Dodać 2-3 krople fenoloftaleiny i miareczkować mianowanym roztworem wodorotlenku sodu do uzyskania lekko różowego zabarwienia. |
Po rozpuszczeniu substancji w kolbie miarowej, należy odczekać przed dopełnieniem jej wodą "do kreski" miarowej. Taki sposób postępowania jest uzasadniony
Korzystając z danych w tabeli wskaż, ile cm3 36% roztworu HCl należy użyć, aby przygotować 250 cm3 0,1-molowego roztworu tego kwasu.
| % wagowy [%] | d420 [g/cm3] | m HCl w 100 cm3 [g/100cm3] | CM HCl [mol/dm3] |
|---|---|---|---|
| 30 | 1,1492 | 34,48 | 9,46 |
| 32 | 1,1593 | 37,10 | 10,17 |
| 34 | 1,1691 | 39,75 | 10,90 |
| 36 | 1,1789 | 42,44 | 11,64 |
Do 200 g roztworu NaOH (M = 40 g/mol) o stężeniu 10 % dodano wodę destylowaną w kolbie miarowej o pojemności 500 cm3 do znaku. Jakie jest stężenie molowe powstałego roztworu?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na rysunku przedstawiono
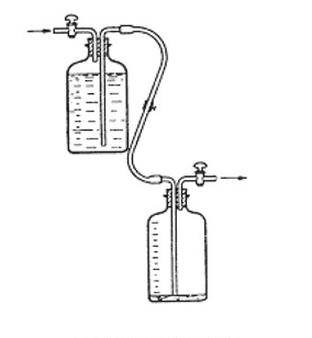
Przedstawiony na rysunku zestaw służy do destylacji
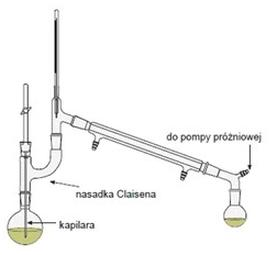
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na rysunku przedstawiono zestaw do
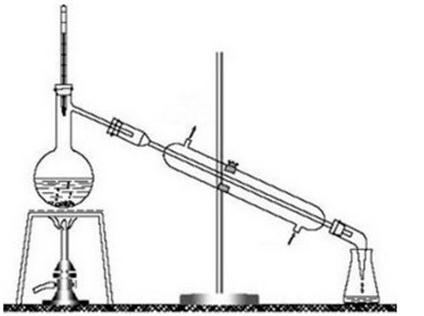
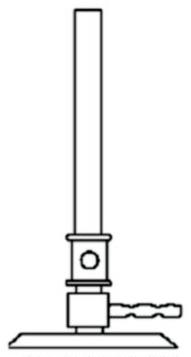
Na rysunku przedstawiono palnik gazowy
Ekstrakcję w trybie ciągłym przeprowadza się
Nie należy podgrzewać cieczy w szczelnie zamkniętych pojemnikach, ponieważ
Sączków o najmniejszych średnicach, nazywanych "twardymi" i oznaczonych kolorem niebieskim, używa się do filtracji osadów?
Do kolby destylacyjnej wprowadzono 200 cm3 zanieczyszczonego acetonu o gęstości d = 0,9604 g/cm3 oraz czystości 90% masowych. W celu oczyszczenia przeprowadzono proces destylacji, w wyniku czego uzyskano 113,74 g czystego acetonu. Jakie były straty acetonu podczas destylacji?
Proces chemiczny, który polega na przejściu substancji w stanie stałym do roztworu, związany z reakcją tej substancji z rozpuszczalnikiem, to
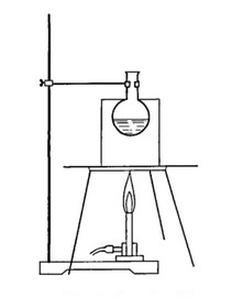
Na rysunku przedstawiono ogrzewanie kolby z cieczą w łaźni
Która z metod pozwala na oddzielanie składników mieszaniny na podstawie różnic w ich zachowaniu w układzie składającym się z dwóch faz, z których jedna jest fazą stacjonarną, a druga porusza się w określonym kierunku względem niej?
Wagi laboratoryjne można klasyfikować według nośności oraz precyzji na
Z kolby miarowej o pojemności 1 dm3, zawierającej roztwór HCl o stężeniu 0,1 mol/dm3, pobrano pipetą 2,5 cm3, a następnie przeniesiono do kolby miarowej o pojemności 20 cm3 i rozcieńczono wodą "do kreski" miarowej. Jakie stężenie ma otrzymany roztwór?
Który zestaw zawiera niezbędne urządzenia laboratoryjne do przygotowania 10% (m/m) roztworu NaCl?
Wskaż jaka zawartość chlorków w próbce wody pozwala na wykorzystanie tej wody do produkcji betonu zgodnie z normą PN-EN 1008.
| Wymagania dotyczące zawartości chlorków w wodzie do produkcji betonu według normy PN-EN 1008 | |
| substancja | dopuszczalna wartość w mg/dm3 |
| chlorki | 1000 |
Czułość bezwzględna wagi definiuje się jako
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wskaż zbiór substancji, które po rozpuszczeniu w wodzie stają się elektrolitami?
Oblicz, ile moli gazu można zebrać w pipecie gazowej o pojemności 500 cm3, jeśli gaz będzie gromadzony w warunkach normalnych. (W normalnych warunkach jeden mol gazu ma objętość 22,4 dm3)