Pytanie 1
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
Wynik: 19/40 punktów (47,5%)
Wymagane minimum: 20 punktów (50%)
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
Na radiogramie uwidoczniono
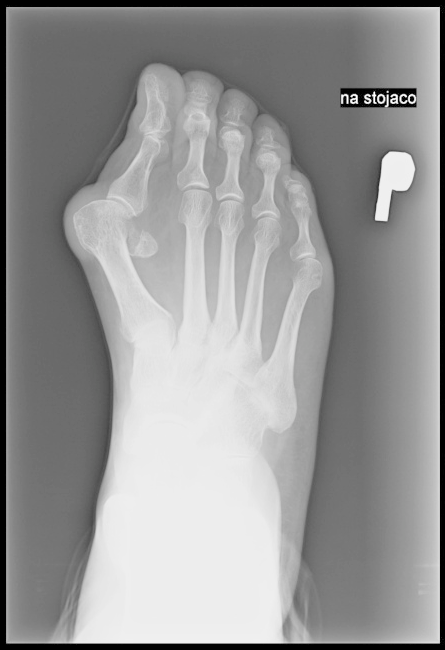
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
Zarejestrowane na elektrokardiogramie miarowe fale f w kształcie „zębów piły” poprzedzielane prawidłowymi zespołami QRS są charakterystyczne dla
Podczas wykonywania zdjęcia rentgenowskiego lewobocznego czaszki promień centralny powinien przebiegać
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
Na elektrokardiogramie uwidoczniono
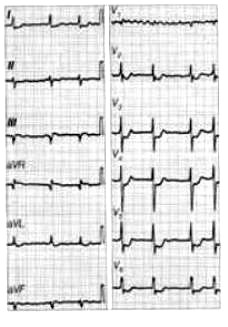
Szczytowy przepływ wydechowy zarejestrowany w trakcie badania maksymalnie natężonego wydechu jest oznaczany skrótem
Audiometria impedancyjna polega na pomiarze
Teleterapia polega na napromienowaniu
Radiogram przedstawia
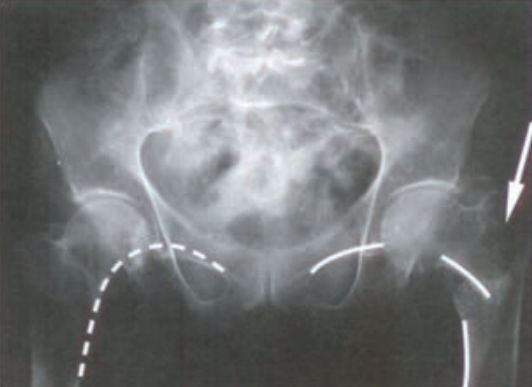
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
Na przedstawionym scyntygramie ukazano duży obszar
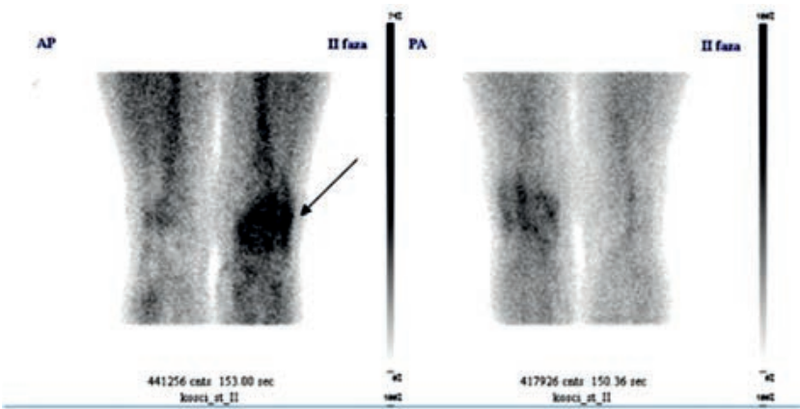
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Jakie źródła promieniowania stosowane są w brachyterapii?
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
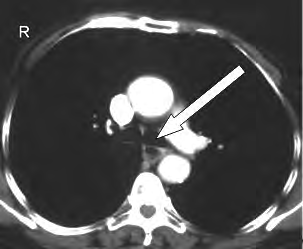
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono
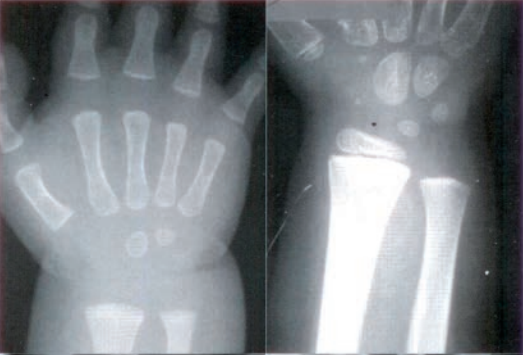
Zestaw rentgenogramów przedstawia
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm × 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
W standardowym badaniu elektrokardiologicznym elektrodę C4 należy umocować
W jaki sposób należy oprzeć stroik w audiometrycznym badaniu przewodnictwa kostnego?
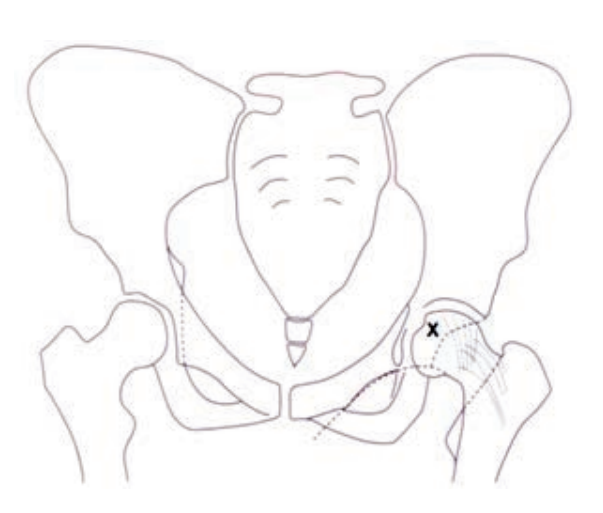
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
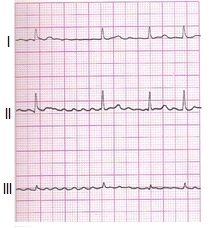
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
Cholangiografia to badanie radiologiczne
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Z kratką przeciwrozproszeniową należy wykonać zdjęcie
W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest
W których projekcjach wykonuje się standardowe badanie mammograficzne?
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Ile razy i jak zmieni się wartość natężenia promieniowania X przy zwiększeniu odległości OF ze 100 cm do 200 cm?
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej