Pytanie 1
Klamrę koferdamu wykonaną z metalu należy po zabiegu
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Klamrę koferdamu wykonaną z metalu należy po zabiegu
Zgodnie z klasyfikacją Spauldinga, narzędzia oraz sprzęt medyczny, które mają kontakt z nienaruszonymi błonami śluzowymi, klasyfikowane są w kategorii
Ile gramów środka odkażającego należy przygotować do dezynfekcji w sposób zanurzeniowy, aby uzyskać 1,5 litra roztworu tego środka o stężeniu 3%?
Aby zachować prawidłową higienę jamy ustnej, po wyjęciu z ust protezę całkowitą należy przechowywać
Raport z wewnętrznej kontroli dotyczącej działań mających na celu zapobieganie rozprzestrzenianiu się infekcji oraz chorób zakaźnych, który powinien być przeprowadzany co najmniej raz na sześć miesięcy, należy archiwizować w
Czas przechowywania odpadów medycznych zakaźnych o kodzie 18 01 03 w temperaturze nieprzekraczającej 10°C nie powinien być dłuższy niż
Jaki preparat wykorzystuje się do dezynfekcji kanałów korzeniowych podczas leczenia zgorzeli miazgi zęba?
Worek zawierający odpady medyczne, w którym znajdują się żywe patogeny lub ich toksyny, powinien być oznaczony kodem
Jak często powinno się wykonywać wewnętrzną kontrolę procesu sterylizacji przy użyciu testu biologicznego oraz zlecać jego ocenę?
Zanurzeniowo nie można przeprowadzać dezynfekcji
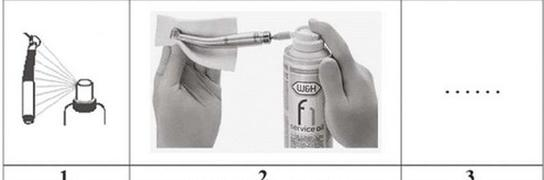
Jaki preparat warto wykorzystać do smarowania kątnic na mikrosilnik oraz turbinę przed ich sterylizacją w autoklawie?
Zgodnie z klasyfikacją Spauldinga, obszar o wysokim ryzyku odnosi się do
Brakującą czynnością wykonywaną po zabiegach w celu dezynfekcji sprzętu układu ssącego jest
| przygotowanie roztworu preparatu dezynfekcyjnego |
| ↓ |
| ... |
| ↓ |
| odwieszenie węża na uchwyt |
| ↓ |
| odessanie preparatu bezpośrednio po dezynfekcji |
Przed umieszczeniem końcówek stomatologicznych w pakiecie papierowo-foliowym, powinny one być przetarte
Aby przygotować 2 litry 4% roztworu roboczego środka dezynfekującego, ile należy użyć
Do dezynfekcji narzędzi stomatologicznych nie wolno stosować
Jakie zadanie realizowane jest w podstrefie I podczas pracy metodą czterech rąk?
Silikonowy odcisk czynnościowy wykonany na indywidualnej łyżce, przygotowany do przekazania technikowi dentystycznemu, powinien być przechowywany
Jakim kodem powinny być oznaczone odpady amalgamatu dentystycznego?
Podczas pakowania instrumentów do torebki papierowo-foliowej, należy zachować odstęp między zgrzewem a materiałem sterylizowanym, który wynosi
Należy usunąć pozostałości materiału światłoutwardzalnego z światłowodu lampy polimeryzacyjnej?
Jaki test jest stosowany do codziennego monitorowania sterylizatorów parowych przed rozpoczęciem ich standardowej działalności w celu sprawdzenia mechanicznej efektywności i szczelności urządzenia oraz możliwości penetracji pary wodnej w sterylizowanych materiałach?
Kleszcze ekstrakcyjne powinny być obsłużone zaraz po przyjęciu pacjenta w sposób
Która zasada aseptyki jest kluczowa podczas pracy w gabinecie stomatologicznym?
Określ właściwą sekwencję działań po zrealizowaniu wycisku dwufazowego?
Jakiego typu test stosuje się do weryfikacji skuteczności biologicznej procesu sterylizacji w autoklawie?
Jaką maksymalną objętość mogą mieć wypełnione narzędziami torebki papierowo-foliowe przed sterylizacją?
Który rysunek przestawia prawidłowe proporcje koncentratu i wody potrzebnych do przygotowania 1 litra 2% roztworu roboczego preparatu dezynfekcyjnego?

Amalgamat dentystyczny w postaci odpadów trzeba umieścić w żółtym pojemniku z kodem
Jak powinno się postępować z lampą polimeryzacyjną po zakończeniu jej użytkowania?
Biologiczna metoda kontrolowania procesu sterylizacji, realizowana cyklicznie, która potwierdza eliminację drobnoustrojów, to test
Odpady z amalgamatu stomatologicznego powinny być umieszczane w żółtym pojemniku z oznaczeniem kodu
Jakim testem weryfikującym skuteczne usunięcie powietrza oraz przenikanie pary wodnej w sterylizatorach parowych jest?
Ile mililitrów środka do dezynfekcji trzeba przygotować, aby uzyskać 3 litry 2% roztworu dezynfekującego?
Zasięg działania środka dezynfekcyjnego, oznaczonego na etykiecie symbolem Tbc, obejmuje
Jakie działania należy podjąć w odniesieniu do zużytego pojemnika separatora amalgamatu?
Aby oczyścić wnętrze kanałów piaskarki z pozostałości materiału ściernego, po opróżnieniu zbiornika i upewnieniu się, że jest on pusty, powinno się
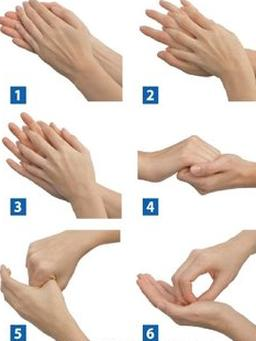
Ilustracja przedstawia etapy higienicznej dezynfekcji rąk według techniki Ayliffe’a. Wykonanie całej procedury powinno trwać
Zużyte ampułki z znieczuleniem powinny być umieszczane
Wybierz brakującą czynność wykonywaną w celu przygotowania końcówki turbiny do sterylizacji.