Pytanie 1
Limfografia to badanie kontrastowe
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
Limfografia to badanie kontrastowe
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
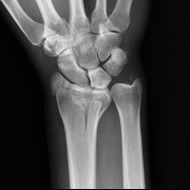
W badaniu MR nadgarstka w ułożeniu na supermana pacjent leży na
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
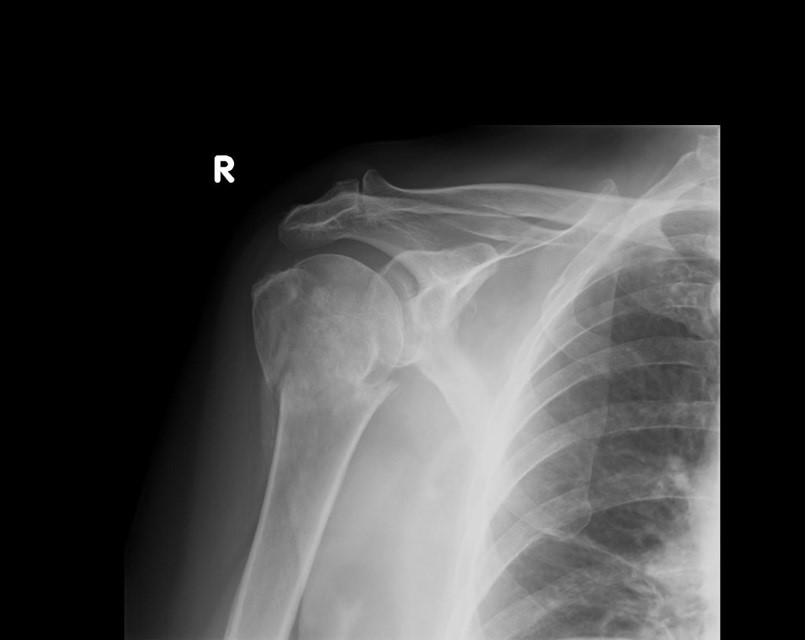
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
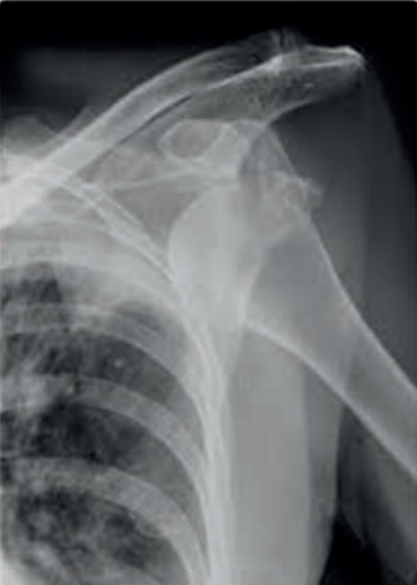
Cholangiografia to badanie radiologiczne
Zamieszczony obraz został wykonany metodą
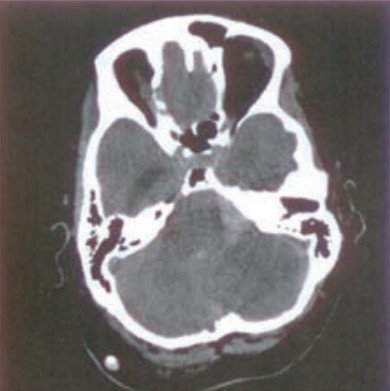
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
W radiografii mianem SID określa się
Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
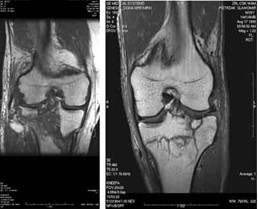
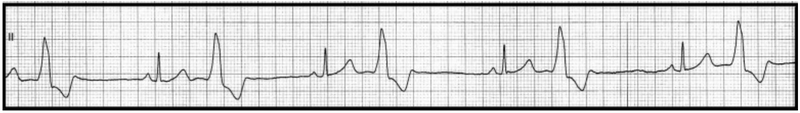
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
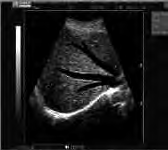
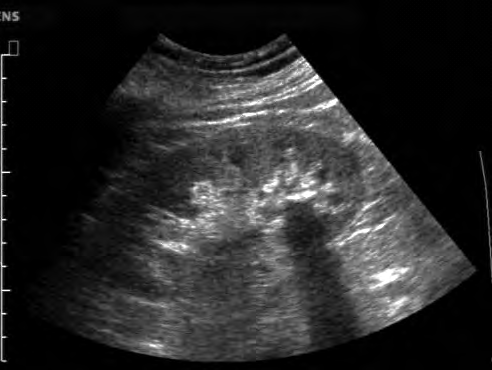
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
W obrazowaniu MR wykorzystuje się moment magnetyczny
Wyniosłość międzykłykciowa znajduje się na nasadzie
Cholangiografia to badanie radiologiczne
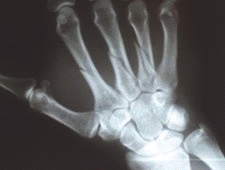
Na radiogramie uwidoczniono złamanie
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?
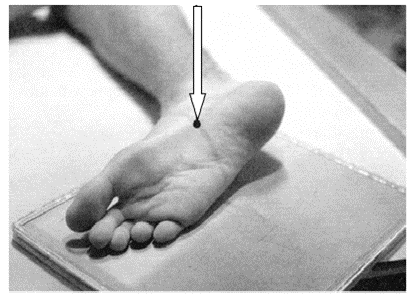
Na zamieszczonej ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
Bezwzględnym przeciwwskazaniem do wykonania badania rezonansem magnetycznym jest
„Ognisko zimne” w obrazie scyntygraficznym określa się jako
Ligand stosuje się
Jaki sposób frakcjonowania dawki jest stosowany w radioterapii konwencjonalnej?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
Na radiogramie uwidoczniono złamanie
Kolimator wielolistkowy w akceleratorze liniowym jest stosowany do
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
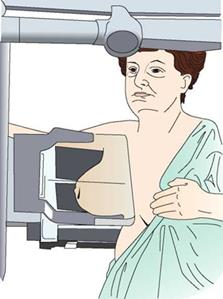
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
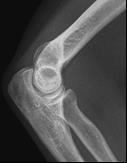
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
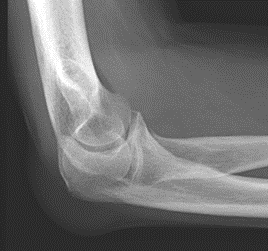
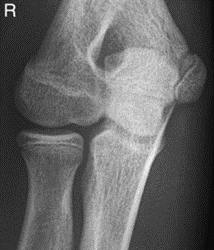
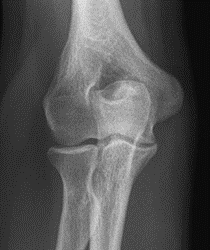
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
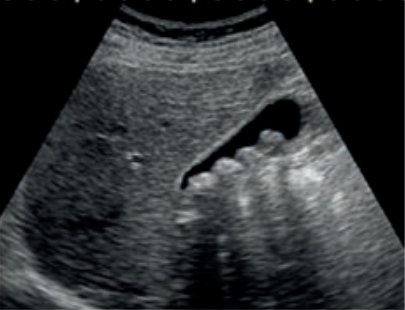
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
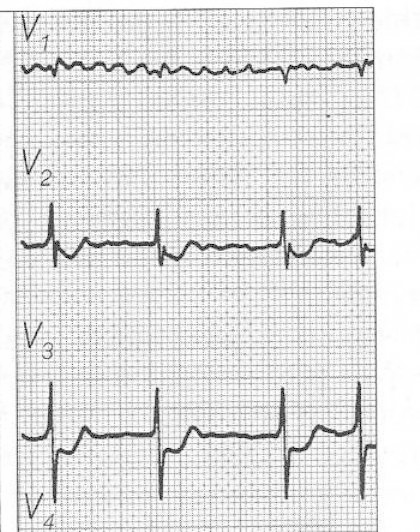
Zamieszczony elektrokardiogram przedstawia
Za wyrównanie ciśnienia między uchem środkowym a otoczeniem odpowiada
W leczeniu izotopowym tarczycy podaje się