Pytanie 1
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Pomiar densytometryczny BMD metodą DXA z kręgosłupa powinien obejmować kręgi
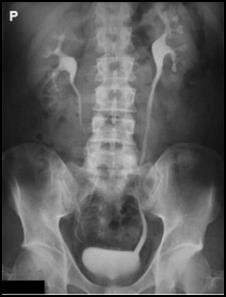
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
W obrazowaniu MR wykorzystuje się moment magnetyczny
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
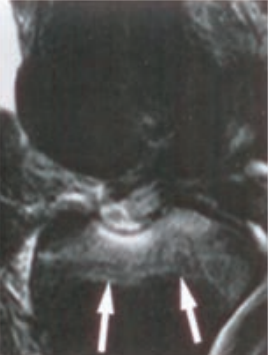
Obraz stawu kolanowego otrzymano metodą
Warstwa półchłonna (WP) służy do obliczania
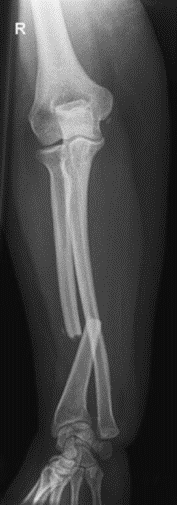
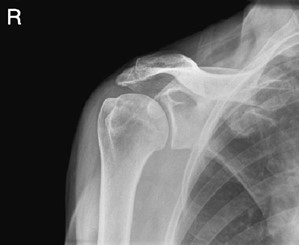
Na radiogramie uwidoczniono złamanie
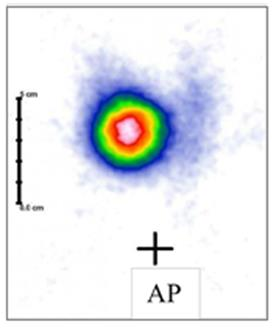
Na scyntygramie tarczycy uwidoczniono guzek
Jak przebiega promień centralny w projekcji AP czaszki?
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
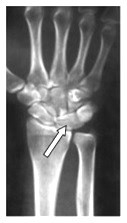
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
Czym charakteryzuje się późny odczyn popromienny?
Przy podejrzeniu ciała obcego w oczodole należy wykonać
DSA to cyfrowa
Który artefakt uwidoczniono na skanie RM głowy?
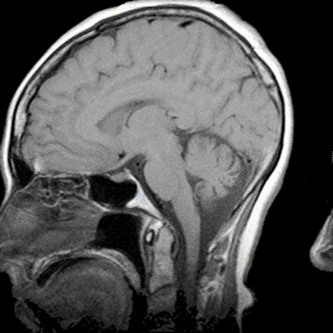
Na obrazie uwidoczniono
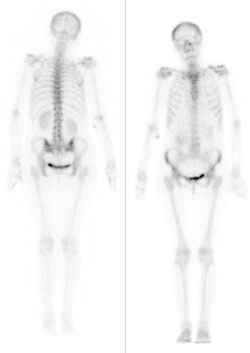
Proces chemicznego wywoływania radiogramów polega na
W badaniu MR nadgarstka w ułożeniu na supermana pacjent leży na
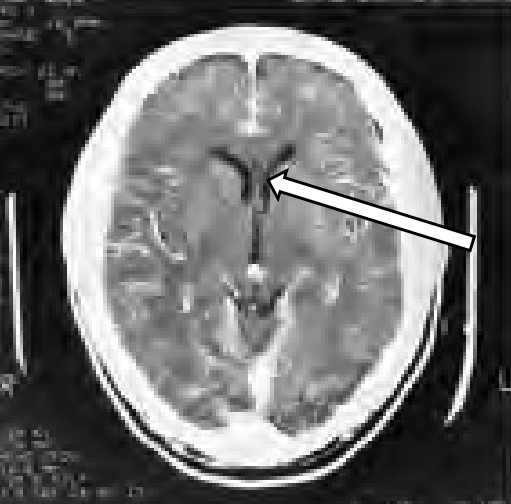
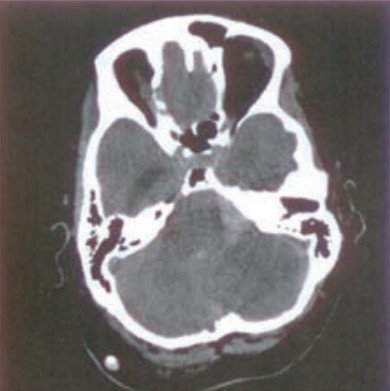
Którą strukturę anatomiczną oznaczono na skanie TK głowy?
W radiografii mianem SID określa się
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
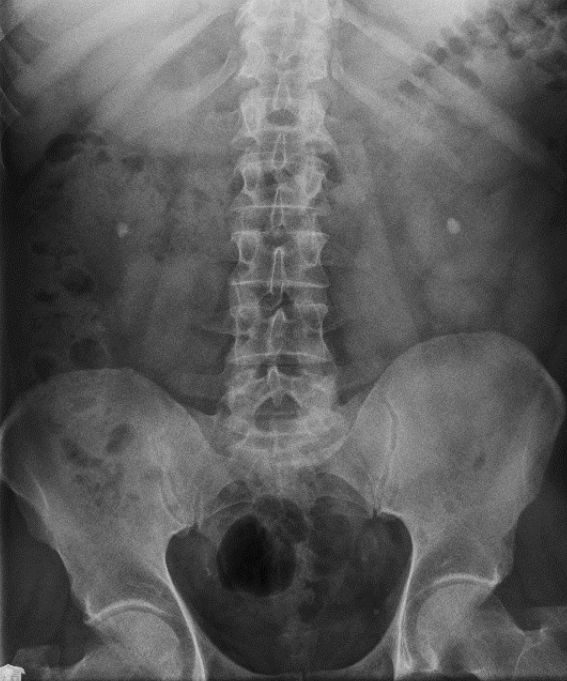
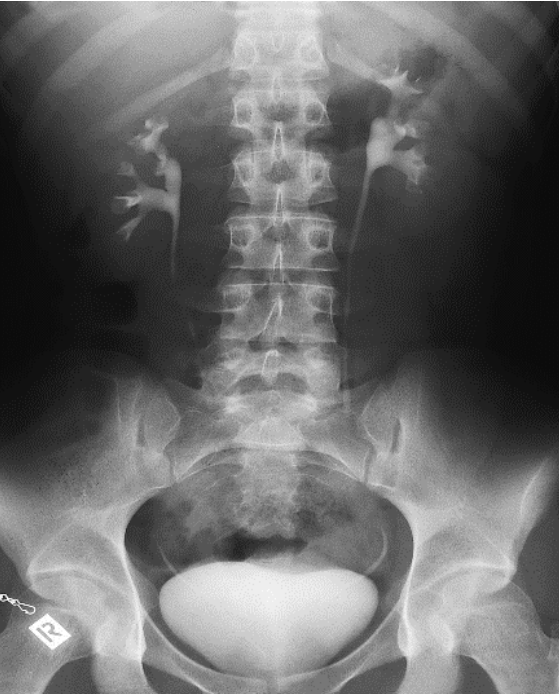
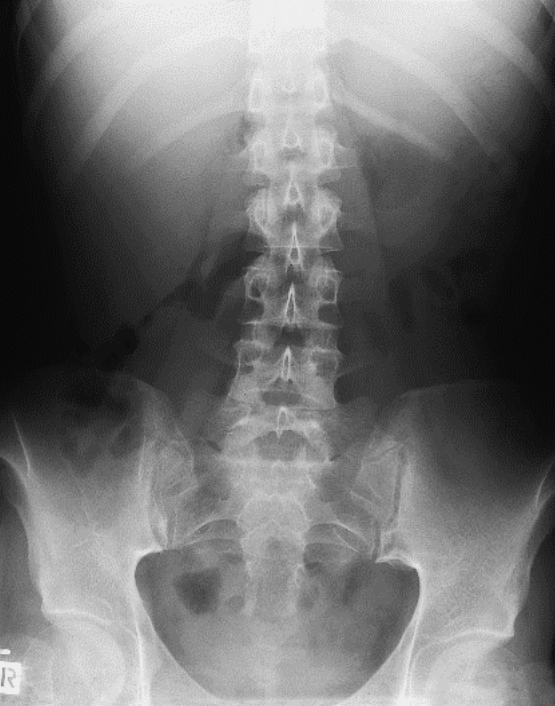
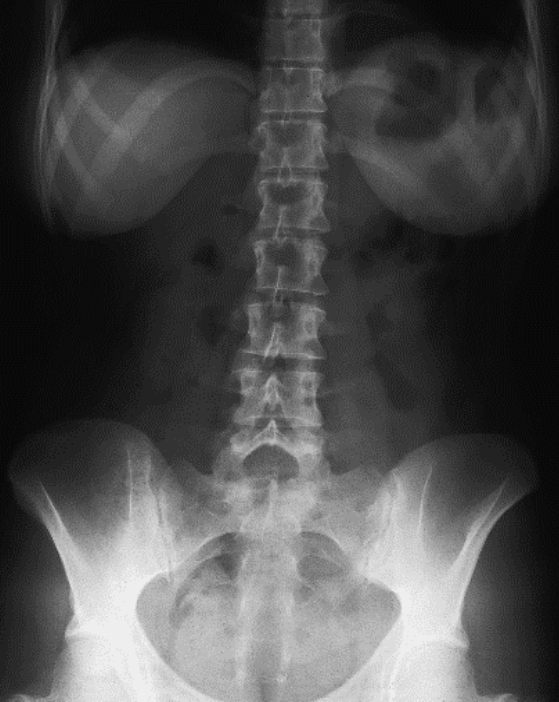
Na którym radiogramie uwidoczniona jest kamica nerkowa?
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
W badaniu cystografii wstępującej środek kontrastowy należy podać
Zamieszczony obraz został wykonany metodą
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Technikę bramkowania oddechowego stosuje się w badaniu MR
Fala głosowa rozchodzi się
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
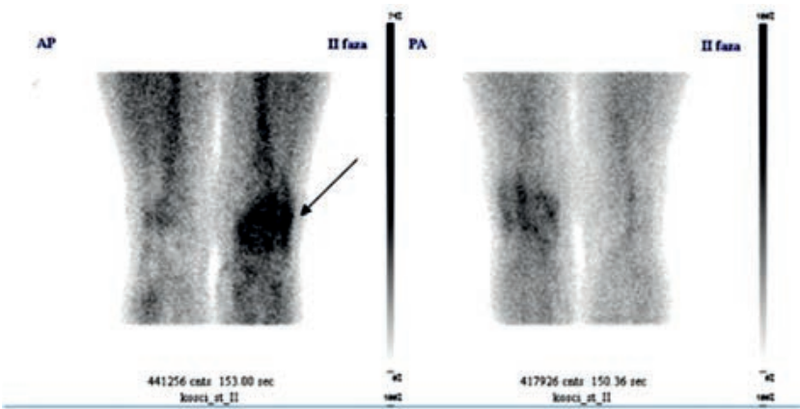
Na przedstawionym scyntygramie ukazano duży obszar
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
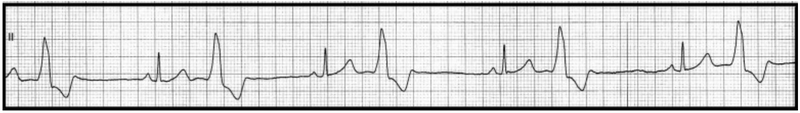
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
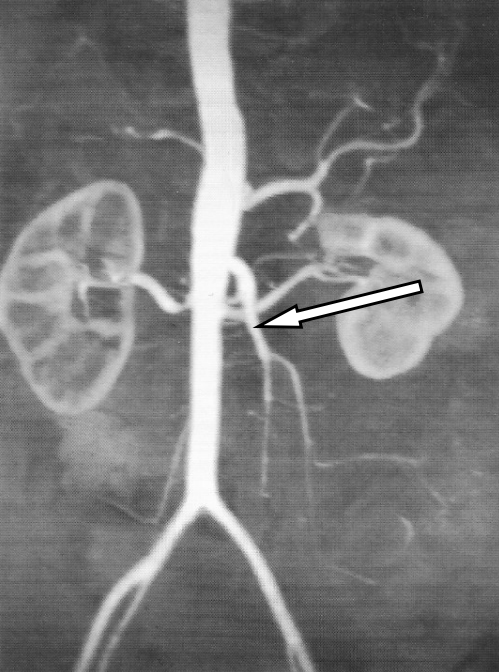
Którą tętnicę zaznaczono strzałką na obrazie MR?
Badanie gęstości mineralnej kości metodą DXA należy wykonać
Na radiogramie uwidoczniono
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?