Pytanie 1
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
W badaniu EKG elektrodę przedsercową V4 należy umocować
Ultrasonograficzne środki kontrastowe to
HRCT (high-resolution computed tomography) jest metodą obrazowania TK
Fala głosowa rozchodzi się
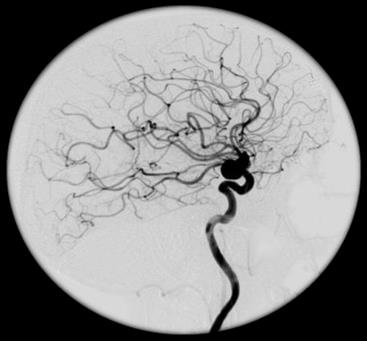
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
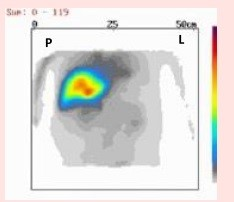
Który narząd został uwidoczniony na przedstawionym obrazie scyntygraficznym?
W scyntygrafii perfuzyjnej płuc pacjentowi podawany jest radioizotop
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
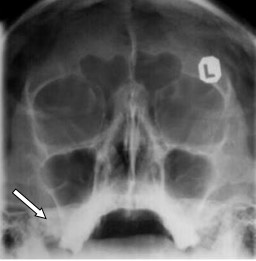
Na radiogramie czaszki strzałką zaznaczono
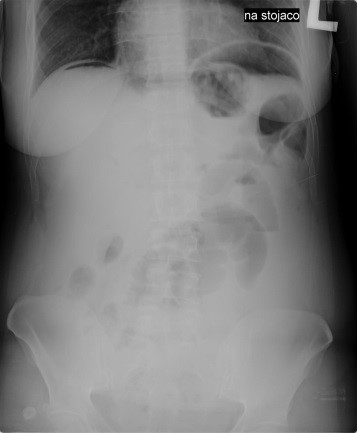
Radiogram jamy brzusznej uwidacznia
W scyntygrafii serca metoda bramkowanej akwizycji SPECT umożliwia między innymi ocenę frakcji wyrzutowej
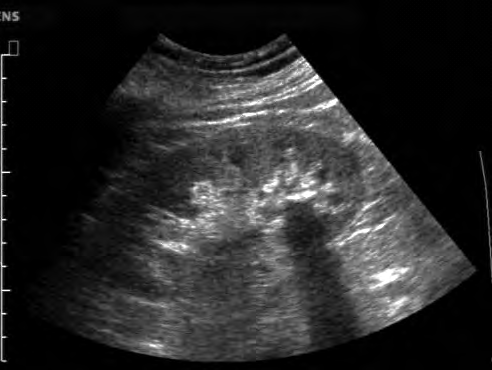
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
Który detektor w radiografii wymaga laserowego czytnika obrazu?
Teleterapia polega na napromienowaniu
W radiografii mianem SID określa się
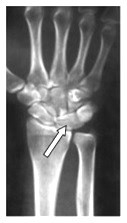
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
Badanie cewki moczowej polegające na wstecznym wprowadzeniu środka kontrastowego to
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
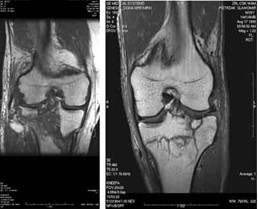
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
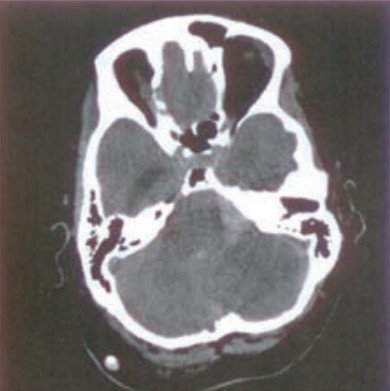
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
Zamieszczony obraz został wykonany metodą
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Celem radioterapii paliatywnej nie jest
Największa wartość energii promieniowania stosowanego w radioterapii jest generowana przy użyciu
Ligand stosuje się
W radioterapii hadronowej leczenie odbywa się przy użyciu
Na zamieszczonym rentgenogramie strzałką zaznaczono
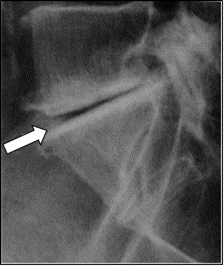
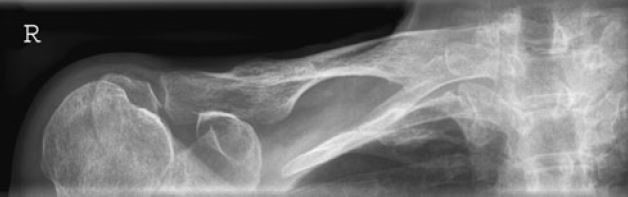
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
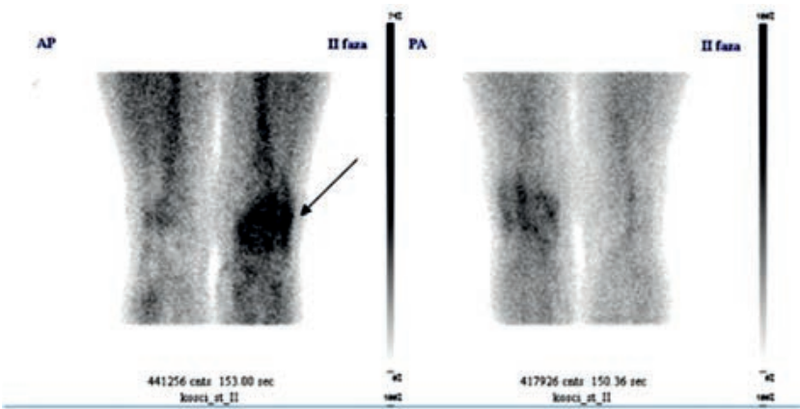
Na przedstawionym scyntygramie ukazano duży obszar
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Lordoza to fizjologiczna krzywizna kręgosłupa występująca
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Badanie przewodu pokarmowego metodą podwójnego kontrastu wiąże się z podaniem pacjentowi
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
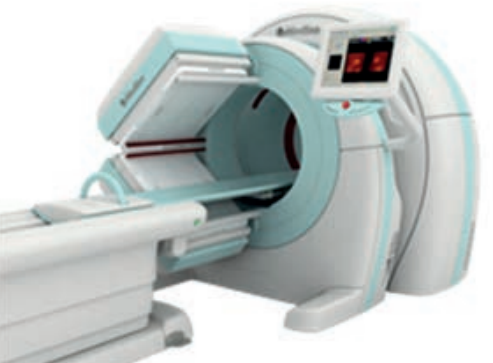
Które urządzenie zostało przedstawione na fotografii i w jakiej pracowni znajduje zastosowanie?