Pytanie 1
Związki lotne, które występują w wielu roślinach i mogą być wydobywane, np. poprzez destylację z parą wodną lub dzięki ciągłej ekstrakcji w aparacie Soxhleta, to
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
Związki lotne, które występują w wielu roślinach i mogą być wydobywane, np. poprzez destylację z parą wodną lub dzięki ciągłej ekstrakcji w aparacie Soxhleta, to
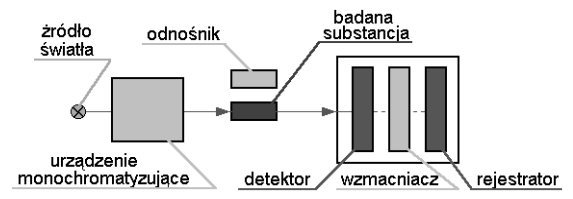
Schemat blokowy przedstawia
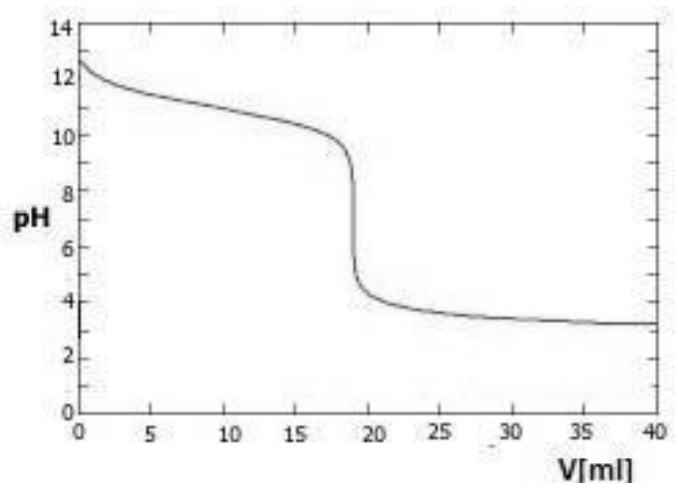
Na wykresie przedstawiono krzywą miareczkowania
Podczas elektrolizy wodnego roztworu kwasu solnego na katodzie zachodzi reakcja opisana równaniem
| A. | 2 H2O + 2e− → H2 + 2 OH− |
| B. | 2 H2O + 4e− → 4H+ + O2 |
| C. | 2 Cl− → Cl2 + 2e− |
| D. | 2 H+ + 2e− → H2 |
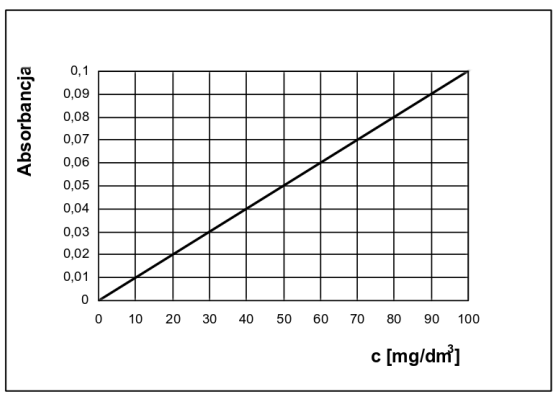
Korzystając z zamieszczonej na rysunku krzywej wzorcowej spektrofotometrycznego oznaczania kwasu salicylowego określ, ile miligramów tego kwasu znajduje się w 1 dm3 roztworu, jeżeli absorbancja badanej próbki wynosi 0,06.
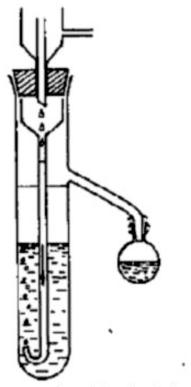
Ekstraktor przedstawiony na rysunku stosuje się do rozpuszczalników
W próbce wody pitnej o objętości 100 cm3 oznaczono zawartość azotanów 4 mg, chlorków 23 mg, manganu 0,006 mg i żelaza 0,01 mg. Korzystając z danych zawartych w tabeli, można stwierdzić, że badana woda
| Tabela. Wybrane parametry, jakim powinna odpowiadać woda do picia | ||
|---|---|---|
| Wskaźnik jakości wody | Jednostka | Najwyższe dopuszczalne stężenie lub zakres |
| Barwa | mgPt/l | 15 |
| Mętność | NTU | 1 |
| Zapach | - | akceptowalny |
| Odczyn | pH | 6,5 – 9,5 |
| Przewodność | μS/cm w 20°C | 2500 |
| Azotany | mg/l | 50 |
| Chlorki | mg/l | 250 |
| Chlor – wolny | mg/l | 0,1 – 0,3 |
| Mangan | mg/l | 0,05 |
| Twardość ogólna | mg CaCO₃/l | 60 - 500 |
| Twardość niewęglanowa | mval/l | - |
| Utlenialność | mgO₂/l | 5 |
| Żelazo | mg/l | 0,2 |
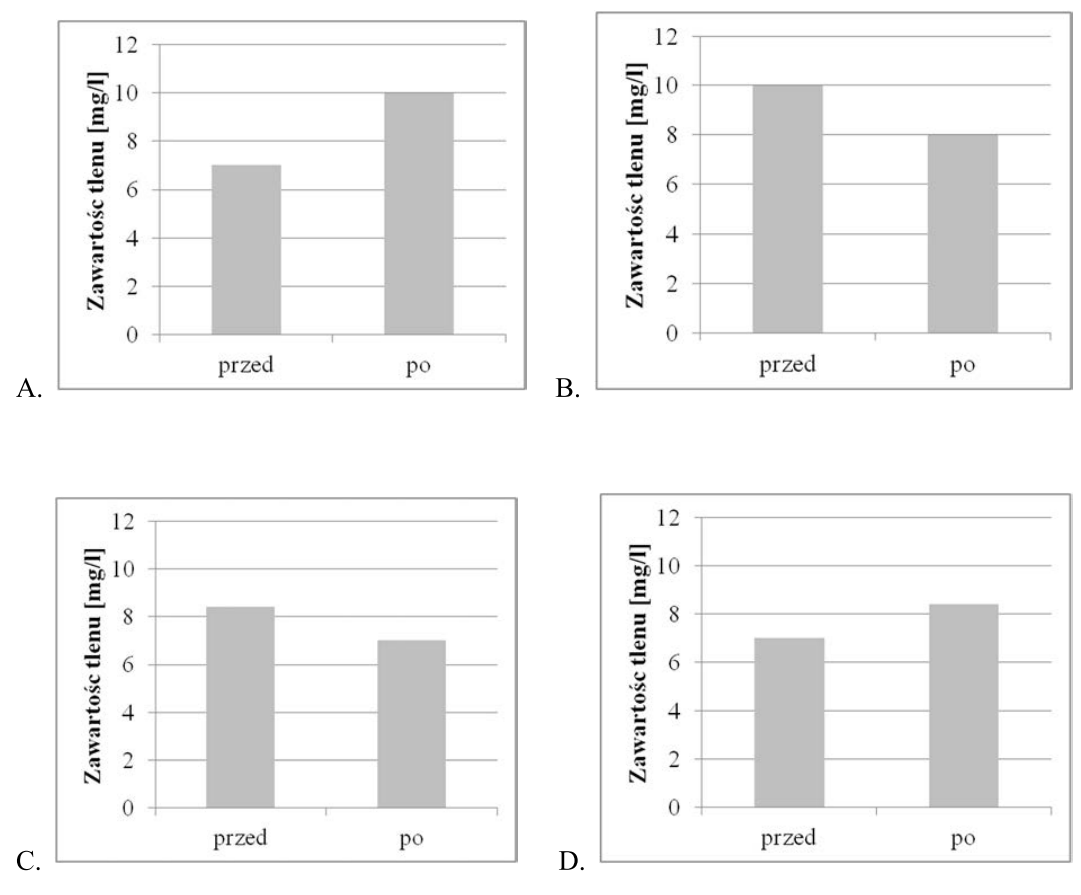
Badaniom poddano wodę z akwarium przed napowietrzaniem i po napowietrzaniu. Wiadomo, że zawartość tlenu w wodzie powinna wzrosnąć o 20%. Który z wykresów obrazuje wyniki tych badań?
W celu oceny jakości masła wykonano oznaczenie liczby kwasowej LK, liczby zmydlania LZ i liczby nadtlenkowej LOO. Wyniki zapisano w tabeli.
Wartość liczby estrowej LE w badanym maśle wynosi
| Liczba | Wartość zmierzona |
|---|---|
| LZ | 196,8 mg KOH/1g |
| LK | 1,2 mg KOH/1g |
| LE | ? |
| LOO | 4,25 milirównoważnika aktywnego tlenu/ kg |
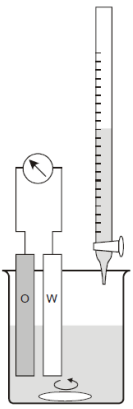
Na rysunku przedstawiono schemat układu do miareczkowania
O - elektroda odniesienia
W - elektroda wskaźnikowa
Reakcja ksantoproteinowa umożliwia identyfikację aminokwasu, który zawiera w swojej budowie
Zjawisko polegające na chemicznej modyfikacji substancji, które prowadzi do powstania innego związku, łatwiejszego do oznaczenia przy użyciu konkretnej metody, to
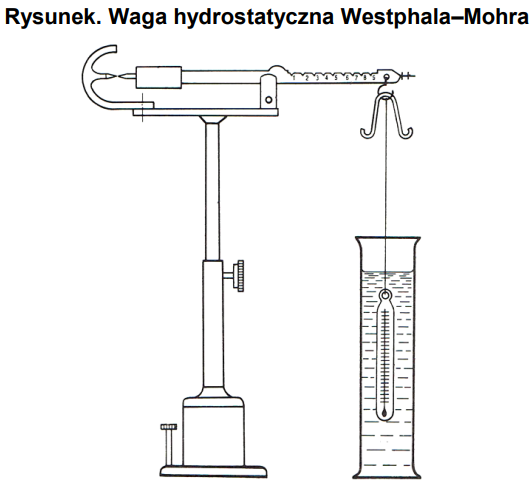
Którą właściwość fizyczną substancji można wyznaczyć za pomocą przyrządu przedstawionego na rysunku?
Na rysunku przedstawiono

Jaką metodę wykorzystuje się do wykrywania i pomiaru ilościowego substancji optycznie czynnych?
Uwzględniając zamieszczoną informację, dobierz metodę stosowaną do oznaczania azotanów(V) w wodzie.
| W środowisku stężonego kwasu siarkowego(VI) jony azotanowe(V) ulegają reakcji z salicylanem sodu, dając kwas nitrosalicylowy, który pod wpływem zasad przechodzi w formę zjonizowaną o żółtym zabarwieniu. |
Sprzyja tworzeniu osadów grubokrystalicznych w czystszej formie oraz umożliwiających łatwiejsze sączenie
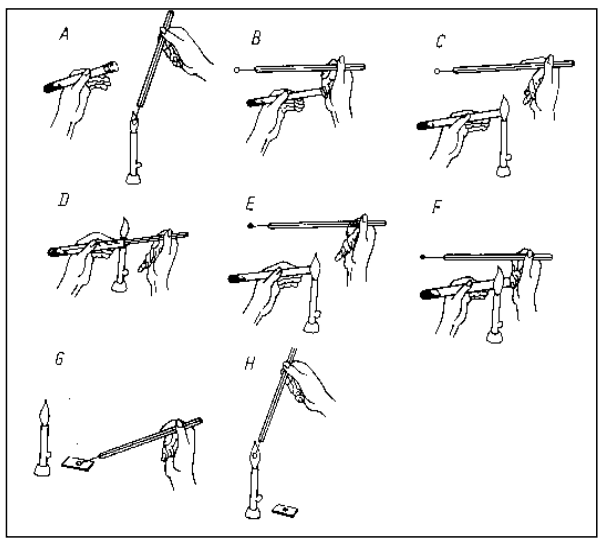
Na schemacie przedstawiającym sposób pobierania hodowli do badań ze skosu agarowego, literą A oznaczono
Związek chemiczny Ag2CrO4, który powstaje podczas analizy chlorków, charakteryzuje się kolorem
Na rysunku przedstawiono schemat

Która z wymienionych soli w roztworze wodnym ma charakter kwasowy?
Który nawóz, spośród wymienionych w tabeli, zawiera najwięcej azotu azotanowego?
| Tabela. Zawartość składnika czynnego w nawozach azotowych | |
|---|---|
| Nawóz | Zawartość składników, % |
| Saletra potasowa | N – 13,5% |
| Saletra magnezowa | N – 10,8% |
| Saletra amonowa | N – 34% (NH4+ – 17%, NO3- – 17%) |
| Saletra wapniowa | N – 14,5% |
| Siarczan amonu | N – 21% |
| Mocznik | N – 46% |
Jednym z kroków w procesie przygotowania preparatu mikrobiologicznego w stanie żywym jest
Jaką barwę ma oranż metylowy w środowisku o pH kwaśnym?
| Zawartość chlorowodoru w próbce można obliczyć wg wzoru: mB = CA · VA⁄1000 · pB⁄pA · MB w którym: mB – masa analizowanej substancji [g] CA – stężenie titranta [mol/dm3] VA – objętość titranta [cm3] pA i pB – współczynniki stechiometryczne reakcji, odpowiednio titranta i substancji oznaczanej MB – masa molowa substancji oznaczanej; 36,46 g/mol Do oznaczenia zużyto średnio 20,0 cm3 titranta, którego stężenie wynosiło 0,1000 mol/dm3. Obliczono masę próbki, która wyniosła 0,07292 g. |
| A. | HCl + NaOH → NaCl + H2O |
| B. | 3HCl + Al(OH)3 → AlCl3 + 3H2O |
| C. | 2HCl + Na2CO3 → 2NaCl + H2O + CO2 |
| D. | 2HCl + Na2B4O7 + 5H2O → 4H3BO3 + 2NaCl |
Na ilustracji przedstawiono schemat

Do czego używa się polarymetru?
Aby przygotować podłoże do badań mikrobiologicznych, należy
Jakiego koloru nabierają bakterie Gram—ujemne w trakcie stosowania metody Grama?
Rozpraszanie promieniowania świetlnego przez cząstki koloidalne, które mają wymiary mniejsze od długości fali światła, to zjawisko
Która z podanych metod analitycznych jest klasyfikowana jako technika łączona?
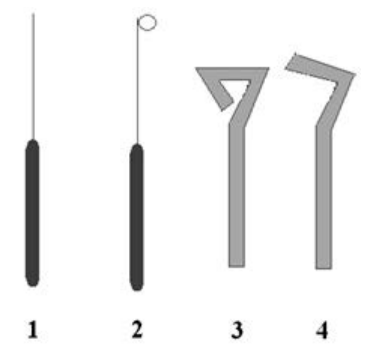
Schematyczny rysunek ezy, przyrządu używanego w laboratoriach mikrobiologicznych, został oznaczony na rysunku cyfrą
Jaką substancję oznacza się metodą Kjeldahla?
Jaką metodą oznacza się kwas solny w analizie miareczkowej?
Metalowe wskaźniki są wykorzystywane w analizach
W tabeli przedstawiono gęstość wodnych roztworów gliceryny w temperaturze 20°C w zależności od jej stężenia wyrażonego w % wagowych.
Z informacji zawartych w tabeli wynika, że stężenie gliceryny o gęstości 1,10 g/cm³ wynosi
| % wagowy gliceryny | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|
| [g/cm3] gęstość | 1,022 | 1,047 | 1,072 | 1,099 | 1,126 | 1,153 | 1,180 | 1,208 | 1,235 | 1,261 |
Woda obecna w cząsteczce Ca(OH)2 określana jest jako woda
Z jaką precyzją należy zważyć próbkę o masie 20 mg, aby błąd względny nie wynosił więcej niż 0,05%?
Substancją wskaźnikową w miareczkowaniu alkacymetrycznym nie jest
Reakcja jonu Ag+ z substancją pełniącą rolę odczynnika grupowego, 4g+ + Cl- —> AgCl ↓, jest typowa dla kationów z grupy