Pytanie 1
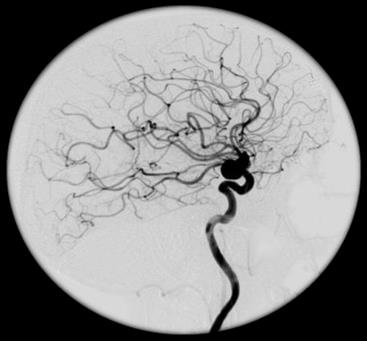
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono

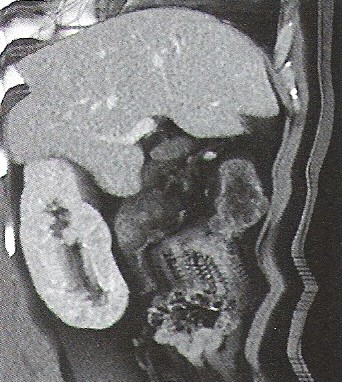
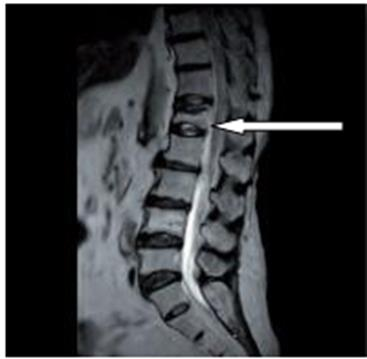
Na obrazie rezonansu magnetycznego strzałką oznaczono wyrostek kolczysty kręgu
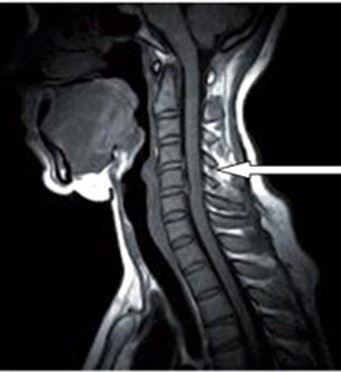
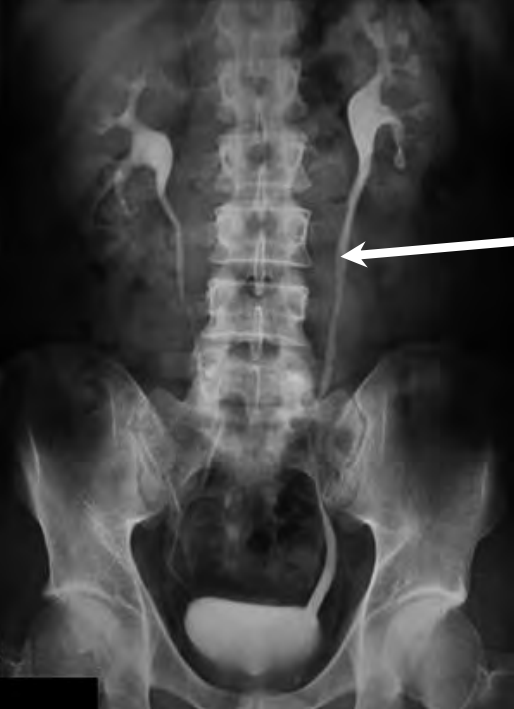
Pielografia zstępująca umożliwia diagnostykę
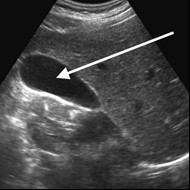
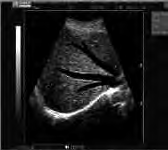
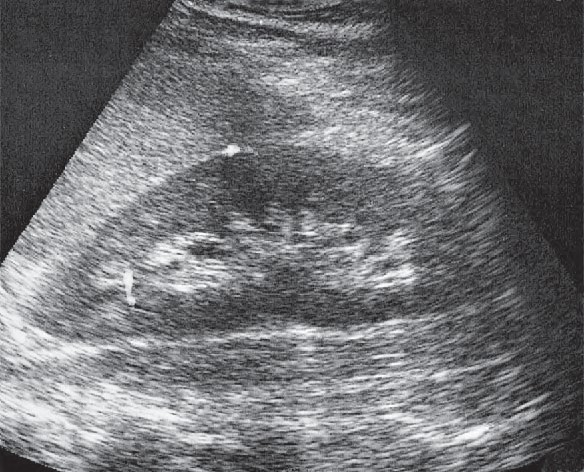
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
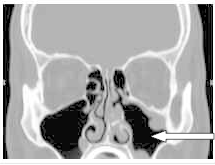
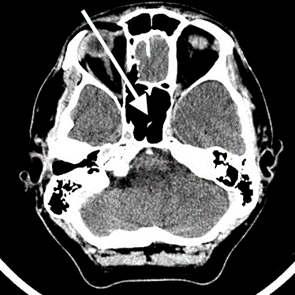
Na obrazie TK zaznaczono zatokę
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
Na prawidłowo wykonanym zdjęciu zatok w projekcji PA górny zarys piramid rzutuje się
W ultrasonografii występuje zależność:
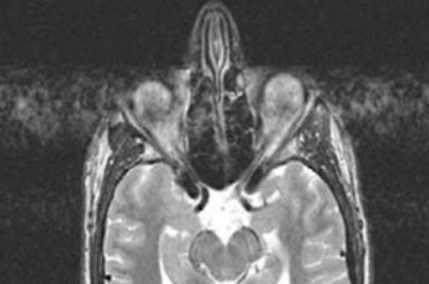
Co jest przyczyną artefaktu widocznego na obrazie MR?
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
W radiografii mianem SID określa się
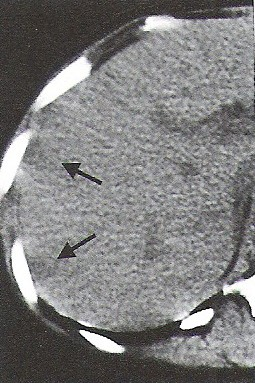
Na radiogramie TK głowy strzałką wskazano
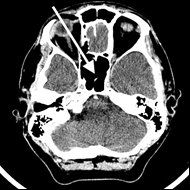
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?
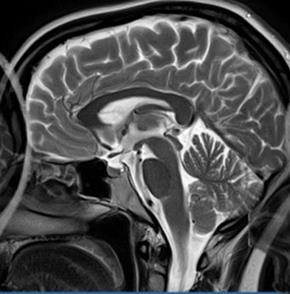
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
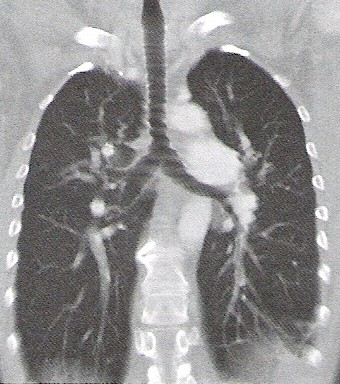
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
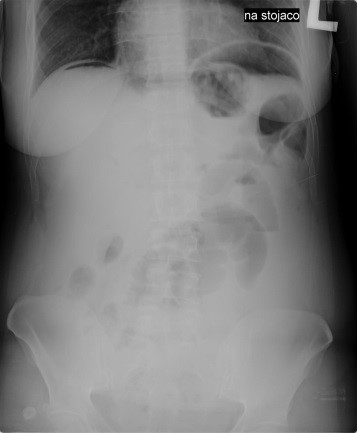
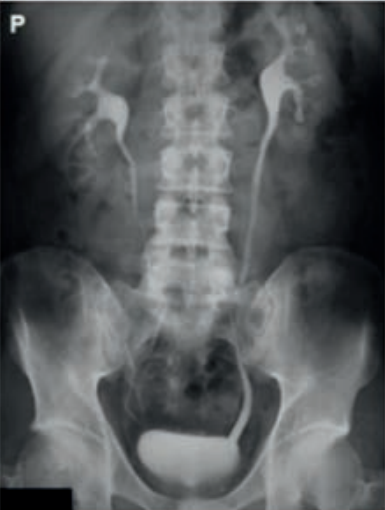
Radiogram jamy brzusznej uwidacznia
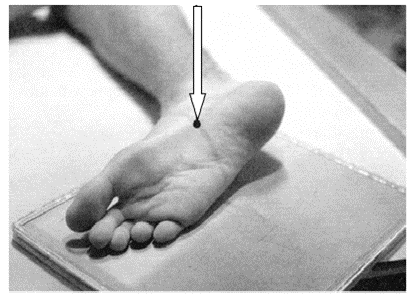
Na zamieszczonej ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
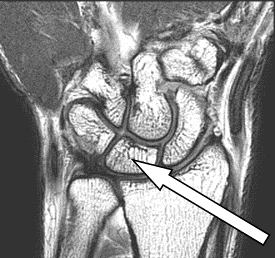
Na zamieszczonym obrazie RM nadgarstka lewego strzałką wskazano kość
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
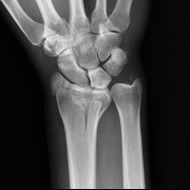
Na zamieszczonym rentgenogramie strzałką zaznaczono
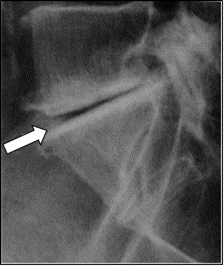
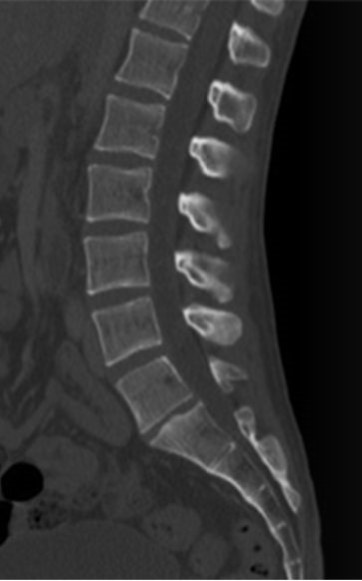
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
Który narząd widoczny jest na wydruku badania ultrasonograficznego?
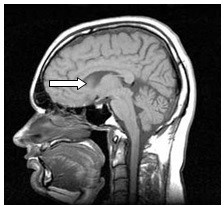
Zaznaczona strzałką struktura anatomiczna na obrazie rezonansu magnetycznego to
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
Standardowe badanie USG średniej wielkości piersi wykonuje się głowicą w zakresie częstotliwości
Którą metodą zostało wykonane badanie kręgosłupa zobrazowane na zdjęciu?
Na rentgenogramie uwidoczniono badanie
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Parametr SNR w obrazowaniu MR oznacza
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
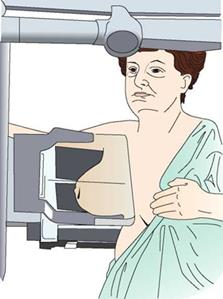
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
Więzka promieniowania X to