Pytanie 1
Nie należy podgrzewać cieczy w szczelnie zamkniętych pojemnikach, ponieważ
Wynik: 32/40 punktów (80,0%)
Wymagane minimum: 20 punktów (50%)
Nie należy podgrzewać cieczy w szczelnie zamkniętych pojemnikach, ponieważ
Jaką metodę wykorzystuje się w laboratorium do rozdzielenia osadu AgCl od cieczy macierzystej w probówkach?
Aby przeprowadzić syntezę substancji organicznej w temperaturze 150°C, należy zastosować łaźnię
Aby obliczyć gęstość cieczy przy użyciu metody hydrostatycznej, należy zastosować
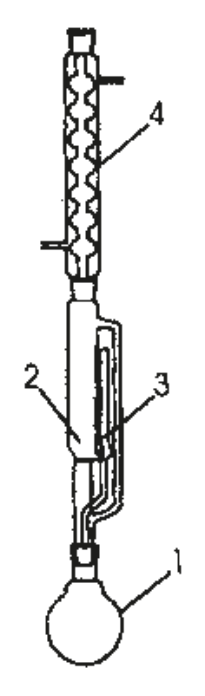
Na rysunku numerami 1 i 4 oznaczono:
Jak nazywa się naczynie o płaskim dnie, które wykorzystuje się do pozyskiwania substancji stałej poprzez stopniowe odparowanie rozpuszczalnika z roztworu?
W celu rozdrabniania niewielkich ilości bardzo twardego materiału wykorzystuje się moździerze
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Aby uzyskać drobnokrystaliczny osad BaSO4, należy wykonać poniższe kroki:
Do zlewki wlać 20 cm3 roztworu BaCl2, następnie dodać 100 cm3 wody destylowanej oraz kilka kropli roztworu HCl. Zawartość zlewki podgrzać na łaźni wodnej, a potem, ciągle mieszając, dodać 35 cm3 roztworu H2SO4.
Mieszaninę ogrzewać na łaźni wodnej przez 1 godzinę. Osad odsączyć i przepłukać kilkakrotnie gorącą wodą zakwaszoną kilkoma kroplami roztworu H2SO4.
Według przedstawionej procedury, do uzyskania osadu BaSO4 potrzebne są:
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Zgłębniki o konstrukcji przypominającej świder są wykorzystywane do pobierania próbek różnych materiałów
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Przedstawiony na rysunku sprzęt służy do

To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Rysunek przedstawia

Ilustracja przedstawia fragment szklanej pipety wielomiarowej

To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Zestaw do filtracji pod obniżonym ciśnieniem powinien obejmować między innymi
Wskaż prawidłowo dobrany sposób kalibracji i zastosowanie szkła miarowego.
| Nazwa naczynia | Sposób kalibracji | Zastosowanie | |
|---|---|---|---|
| A. | kolba miarowa | Ex | do sporządzania roztworów mianowanych o określonej objętości |
| B. | cylinder miarowy | Ex | do sporządzania roztworów mianowanych o określonej objętości |
| C. | pipeta Mohra | Ex | do odmierzania określonej objętości cieczy |
| D. | biureta | In | do odmierzania określonej objętości cieczy |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Wskaź zestaw reagentów oraz przyrządów wymaganych do przygotowania 0,5 dm3 roztworu HCl o stężeniu 0,2 mol/dm3?
Zdjęcie przedstawia palnik

Nie należy używać gorącej wody do mycia
Resztki szkła, osadników czy inne odpady stałe powstałe w laboratorium analitycznym powinny być umieszczone
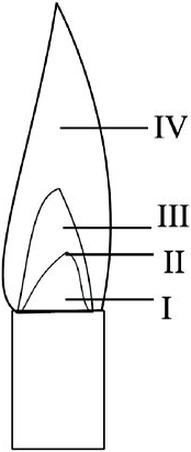
Na rysunku przedstawiającym płomień palnika gazowego najwyższa temperatura płomienia znajduje się w strefie
Zapis "20°C" umieszczony na pipecie oznacza, że

To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Przedstawiony na ilustracji zestaw służy do

Do przechowywania zamrożonych próbek wody stosuje się naczynia wykonane
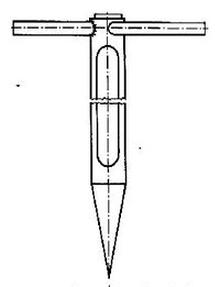
Przyrząd przedstawiony na rysunku służy do pobierania próbek substancji
Wskaź sprzęt konieczny do przeprowadzenia miareczkowania?
Oblicz, ile moli gazu można zebrać w pipecie gazowej o pojemności 500 cm3, jeśli gaz będzie gromadzony w warunkach normalnych. (W normalnych warunkach jeden mol gazu ma objętość 22,4 dm3)
Wagi laboratoryjne można klasyfikować według nośności oraz precyzji na
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Nie należy używać do czyszczenia szklanych naczyń laboratoryjnych
Sączków o najmniejszych średnicach, nazywanych "twardymi" i oznaczonych kolorem niebieskim, używa się do filtracji osadów?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakie oznaczenie znajduje się na naczyniach szklanych kalibrowanych do wlewu?