Pytanie 1
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
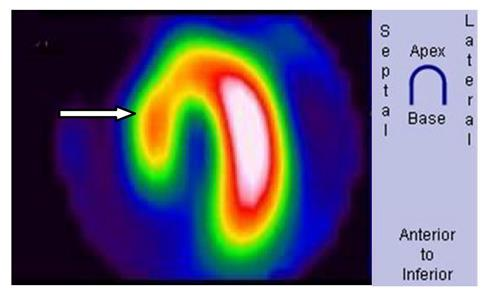
Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę

Promieniowanie rentgenowskie jest
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
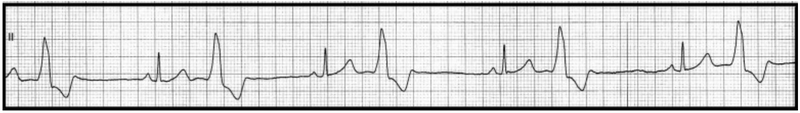
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
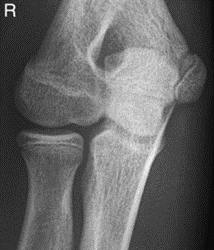
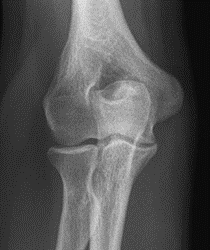
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
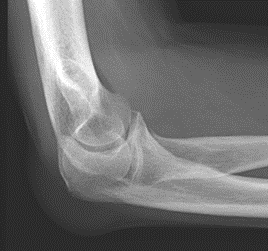
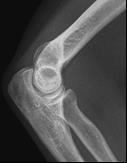
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Na obrazie uwidoczniono
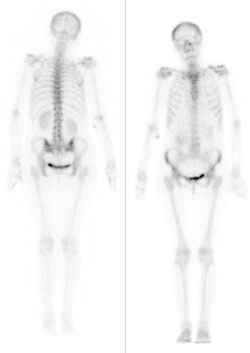
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
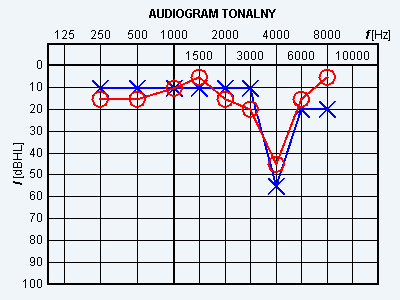
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
Co jest przyczyną artefaktu widocznego na obrazie MR?
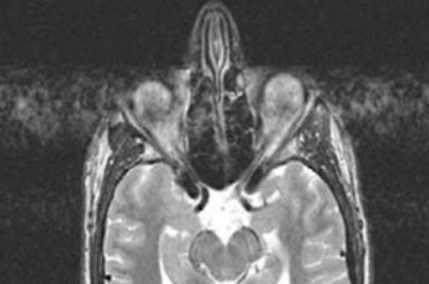
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W radioterapii hadronowej leczenie odbywa się przy użyciu
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
Na ilustracji przedstawiono przygotowanie pacjenta do badania
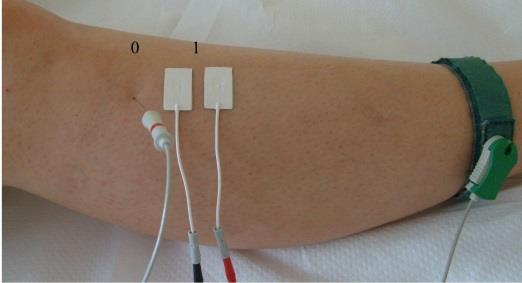
Rumień skóry pojawiający się podczas radioterapii jest objawem
Ligand stosuje się
Na radiogramie uwidoczniono złamanie
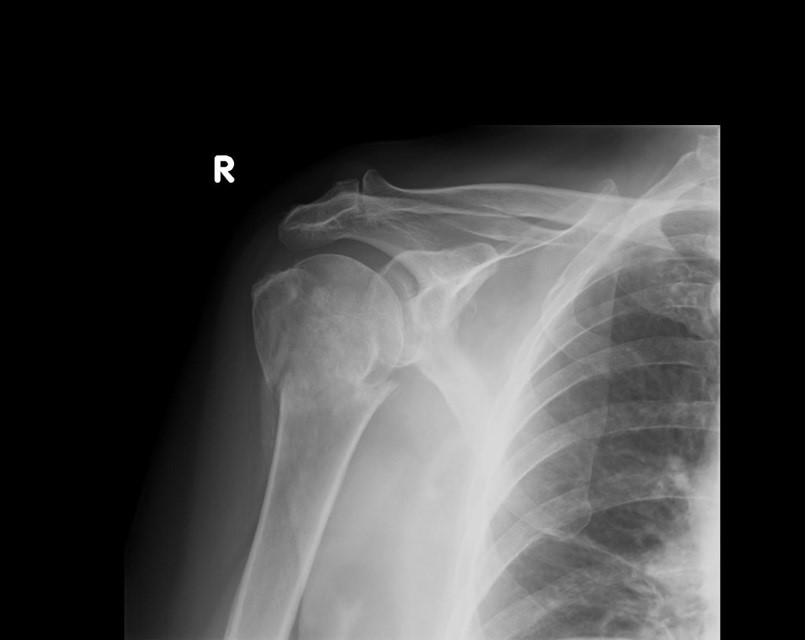
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
Po zakończeniu badania angiograficznego należy zapisać w dokumentacji medycznej pacjenta:
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Lordoza to fizjologiczna krzywizna kręgosłupa występująca
Na ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
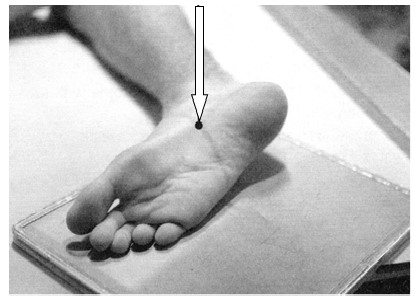
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
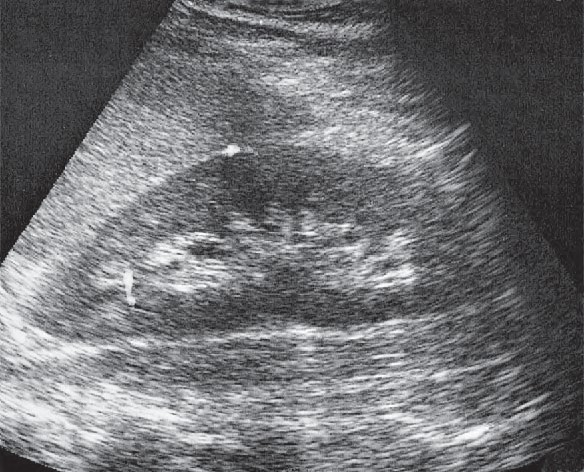
Który narząd widoczny jest na wydruku badania ultrasonograficznego?
Który z nowotworów jest hormonozależny?
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
Która właściwość promieniowania X pozwala na skierowanie promienia centralnego na wybrany punkt topograficzny podczas wykonywania badania radiologicznego?
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
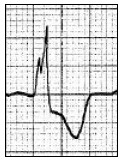
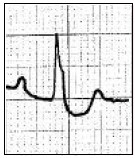
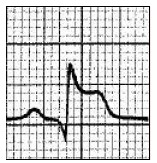
Który zapis EKG przedstawia falę Pardee'go?

W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
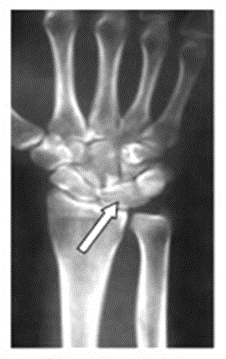
Na zamieszczonym obrazie radiologicznym nadgarstka strzałką wskazano kość
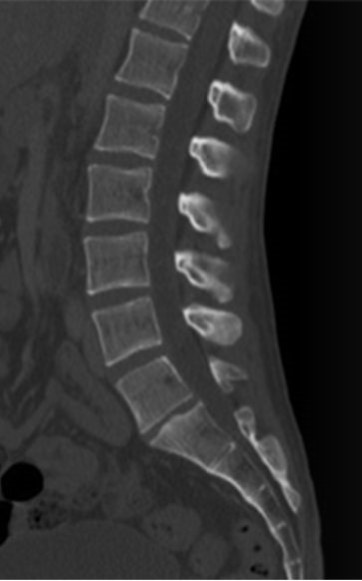
Którą metodą zostało wykonane badanie kręgosłupa zobrazowane na zdjęciu?
Podczas badania gammakamerą źródłem promieniowania jest