Pytanie 1
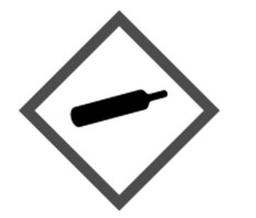
Zamieszczony piktogram odnosi się do substancji o klasie i kategorii zagrożenia:
Wynik: 38/40 punktów (95,0%)
Wymagane minimum: 20 punktów (50%)
Zamieszczony piktogram odnosi się do substancji o klasie i kategorii zagrożenia:

Jakie jest stężenie molowe kwasu siarkowego(VI) o zawartości 96% i gęstości 1,84 g/cm3?
Które z poniższych działań należy wykonać przed rozpoczęciem pracy z nowym szkłem laboratoryjnym?
Który z etapów przygotowania próbek do analizy opisano w ramce?
| Proces polegający na usuwaniu wody z zamrożonego materiału na drodze sublimacji lodu, tzn. bezpośredniego jego przejścia w stan pary z pominięciem stanu ciekłego. |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
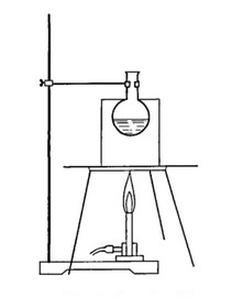
Na rysunku przedstawiono ogrzewanie kolby z cieczą w łaźni
Na podstawie danych w tabeli określ, dla oznaczania którego parametru zalecaną metodą jest chromatografia jonowa.
| Parametr | Metoda podstawowa |
|---|---|
| pH | metoda potencjometryczna, kalibracja przy zastosowaniu minimum dwóch wzorców o pH zależnym od wartości oczekiwanych w próbkach wody |
| azotany(V) | chromatografia jonowa |
| fosforany(V) | spektrofotometria |
| Na, K, Ca, Mg | AAS (spektrometria absorpcji atomowej) |
| zasadowość | miareczkowanie wobec fenoloftaleiny oraz oranżu metylowego |
| tlen rozpuszczony, BZT₅ | metoda potencjometryczna |
Z podanego wykazu wybierz sprzęt potrzebny do zmontowania zestawu do sączenia pod próżnią.
| 1 | 2 | 3 | 4 | 5 | 6 |
| pompka wodna | lejek z długą nóżką | kolba okrągłodenna | kolba ssawkowa | lejek sitowy | chłodnica powietrzna |
Podaj kolejność odczynników chemicznych według rosnącego stopnia czystości?
Ekstrakcję w trybie ciągłym przeprowadza się
Przy przygotowywaniu 100 cm3 roztworu o określonym stężeniu procentowym (m/V) konieczne jest odważenie wyliczonej ilości substancji, a następnie przeniesienie jej do
Masa molowa kwasu azotowego(V) wynosi 63,0 g/mol. Jakie jest stężenie molowe 20% roztworu tego kwasu o gęstości 1,1 g/cm3?
Do przechowywania stężonego kwasu azotowego(V) w laboratorium należy stosować:
W celu uzyskania czystej substancji próbkę zawierającą nitroanilinę poddano krystalizacji. Oblicz masę odważki nitroaniliny, pobranej do krystalizacji, jeśli uzyskano 1,5 g czystego związku, a wydajność krystalizacji wynosiła 75%.
Temperatura topnienia mocznika wynosi 133 °C. W celu określenia czystości preparatów tej substancji, przeprowadzono badania temperatury ich topnienia, uzyskując wyniki przedstawione w tabeli. Wskaż preparat o najmniejszym stopniu czystości.
| Preparat | A | B | C | D |
|---|---|---|---|---|
| Zakres temperatury topnienia [°C] | 132-133 | 130-133 | 125-133 | 128-133 |
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakim kolorem zazwyczaj oznacza się przewody w instalacji gazowej w laboratorium?
Czy odpady laboratoryjne zawierające jony metali ciężkich powinny zostać poddane obróbce przed umieszczeniem ich w odpowiednio oznaczonej pojemności?
Jakim narzędziem dokonuje się poboru próbki wody?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Na rysunku przedstawiono urządzenie służące do poboru próbek

Roztwór amoniaku o stężeniu 25% nie powinien być trzymany
Jakie środki stosuje się do czyszczenia szkła miarowego, które zostało zanieczyszczone substancjami tłustymi?
Jakie jest stężenie procentowe roztworu HCl (M=36,46 g/mol) o gęstości 1,19 g/cm3 oraz stężeniu molowym 12 mol/dm3?
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Którą substancję można bezpośrednio wyrzucić do odpadów komunalnych?
W laboratoriach roztwór potasu dichromianu(VI) w stężonym kwasie siarkowym(VI) wykorzystuje się do
Pierwotna próbka jest zbierana
Ropa naftowa stanowi mieszankę węglowodorów. Jaką metodę wykorzystuje się do jej rozdzielania na składniki?
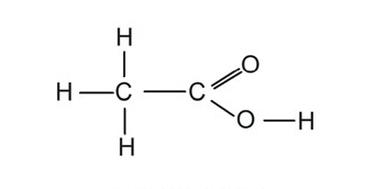
Związek o podanym wzorze to kwas
Na podstawie danych w tabeli określ, jaką masę próbki należy pobrać, jeżeli wielkość ziarna wynosi 1·10-5 m.
| Wielkość ziaren lub kawałków [mm] | Poniżej 1 | 1-10 | 11-50 | Ponad 50 |
|---|---|---|---|---|
| Pierwotna próbka (minimum) [g] | 100 | 200 | 1000 | 2500 |
Odczynnik chemiczny, w którym zawartość domieszek wynosi od 1 do 10%, jest nazywany odczynnikiem
Roztwór zawierający 16,00 g siarczanu(VI) miedzi(II) nasycono siarkowodorem. Masa wytrąconego siarczku miedzi(II), po odsączeniu i wysuszeniu, wynosiła 8,64 g. Oblicz procentową wydajność tej reakcji.
Równanie reakcji:
\( \text{CuSO}_4 + \text{H}_2\text{S} \rightarrow \text{CuS} + \text{H}_2\text{SO}_4 \)
\( \text{M CuSO}_4 = 160 \, \text{g/mol} \)
\( \text{M CuS} = 96 \, \text{g/mol} \)
Metoda przygotowania próbki do badania, która nie jest
Wody pobrane ze studni powinny być przewożone w szczelnie zamkniętych butelkach z przezroczystego materiału
Które z wymienionych reakcji chemicznych stanowi reakcję redoks?
Na ilustracji zobrazowano urządzenie do
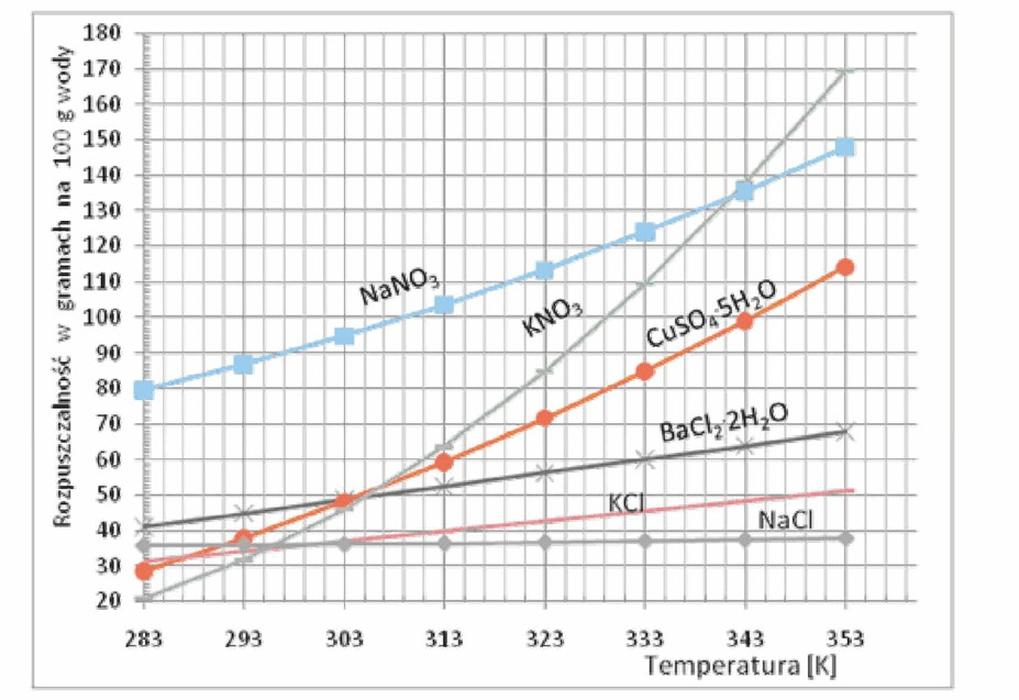
Korzystając z wykresu określ, w jakiej temperaturze należy rozpuszczać azotan(V) potasu, aby całkowicie rozpuścić 110 g soli w 100 g wody.
Na skutek krystalizacji 18 g kwasu benzoesowego uzyskano 8 g czystego produktu. Jaką wydajność miała ta krystalizacja?