Pytanie 1
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Wynik: 40/40 punktów (100,0%)
Wymagane minimum: 20 punktów (50%)
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
W którym miejscu, zgodnie z zasadami wykonywania badania EKG, należy umocować żółtą elektrodę przedsercową V2?
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Do pomiaru dawek indywidualnych u osób narażonych zawodowo na promieniowanie rentgenowskie są stosowane
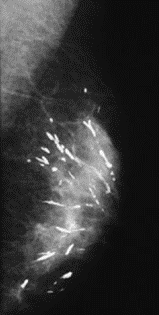
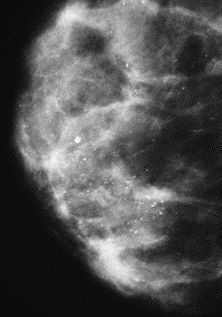
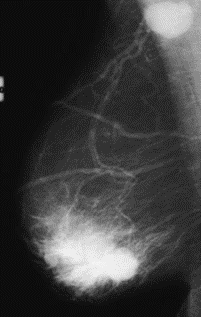
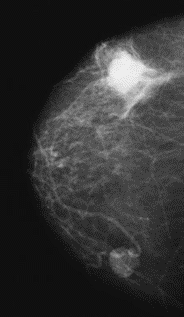
Na którym obrazie rentgenowskim sutka uwidoczniono zmianę patologiczną w obrębie węzłów chłonnych?
Na wykresie EKG zaznaczono
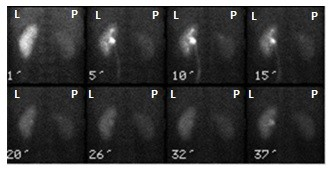
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Więzka promieniowania X to
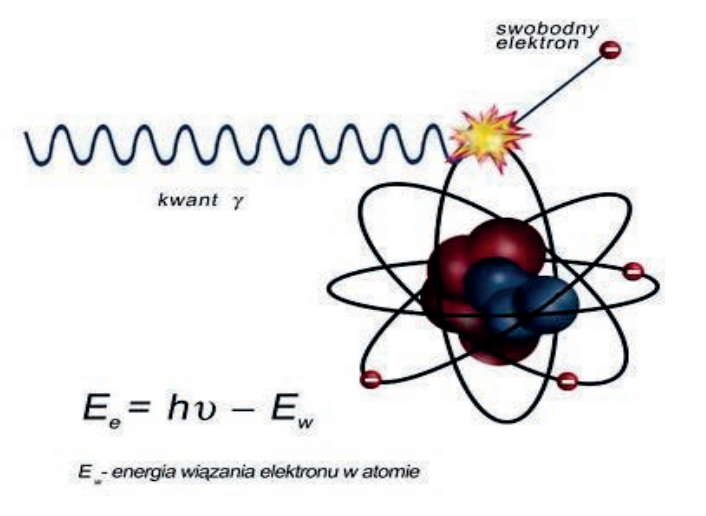
Na schemacie oznaczono
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
Który radioizotop jest emiterem promieniowania alfa?
Który system informatyczny jest wykorzystywany do archiwizowania i przesyłania obrazów na stacje diagnostyczne w standardzie DICOM?
Który załamek odzwierciedla szybką repolaryzację komór w zapisie EKG?
Na zamieszczonej rycinie przedstawiono
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
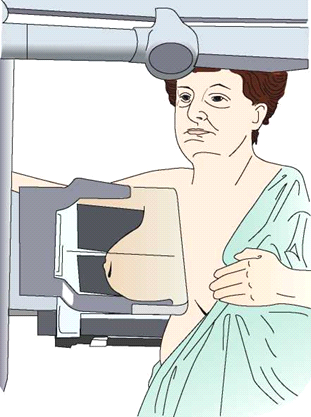
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
Które informacje należy zamieścić na strzykawce z radiofarmaceutykiem przygotowanym przez technika elektroradiologa?
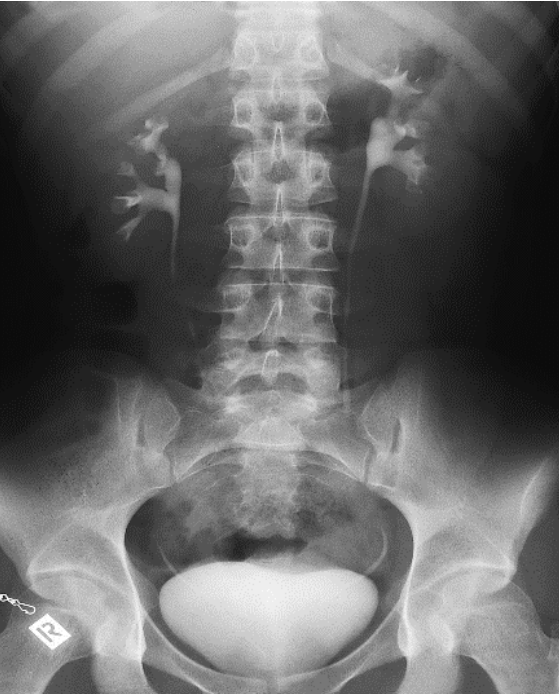
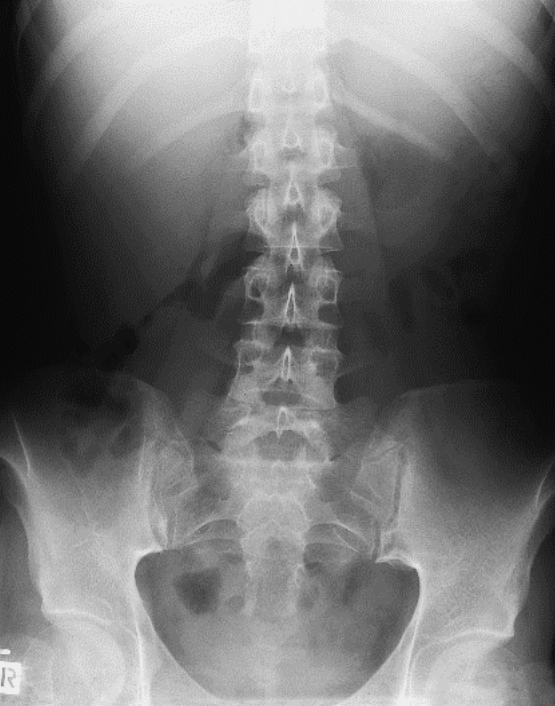
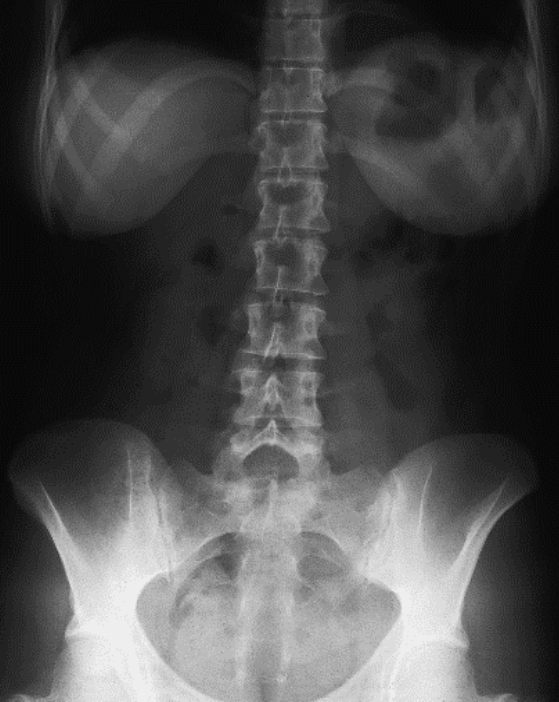
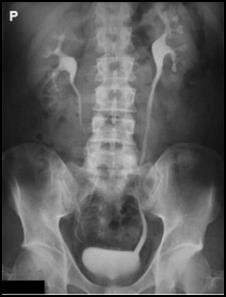
Na którym radiogramie uwidoczniona jest kamica nerkowa?
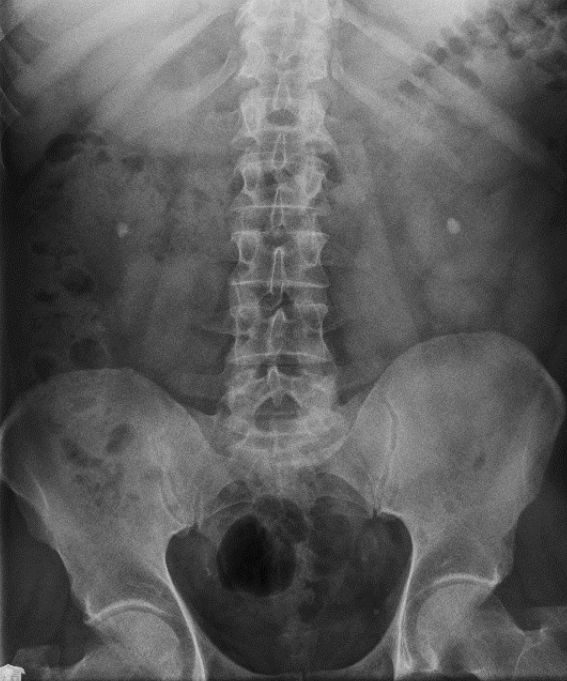
Planowany obszar napromieniania PTV obejmuje
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
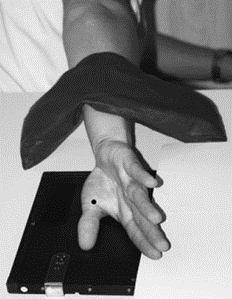
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Który program wtórnej rekonstrukcji obrazów TK pozwala na odwzorowanie wnętrza jelita grubego, tchawicy i oskrzeli?
Na przedstawionym radiogramie TK głowy strzałką zaznaczono
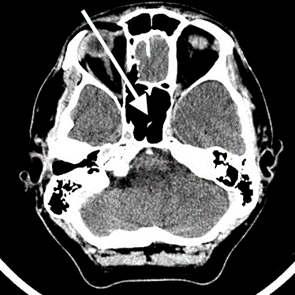
Strzałką na schemacie oznaczono
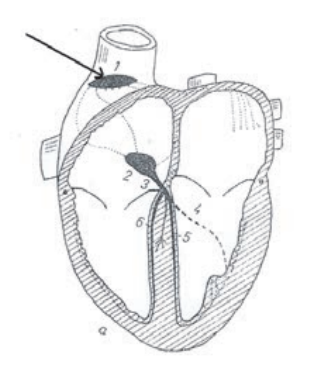
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
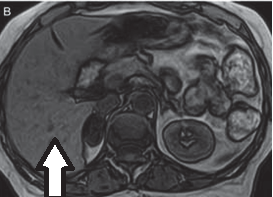
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
Jaki sposób frakcjonowania dawki jest stosowany w radioterapii konwencjonalnej?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Wskazaniem do wykonania badania spirometrycznego jest
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
Badanie polegające na wprowadzeniu cewnika przez pęcherz moczowy do moczowodu i miedniczki nerkowej i podaniu środka kontrastującego to
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
W leczeniu izotopowym tarczycy należy podać
Na ilustracji przedstawiono ułożenie pacjenta do zdjęcia rentgenowskiego
Standardowe badanie USG średniej wielkości piersi wykonuje się głowicą w zakresie częstotliwości
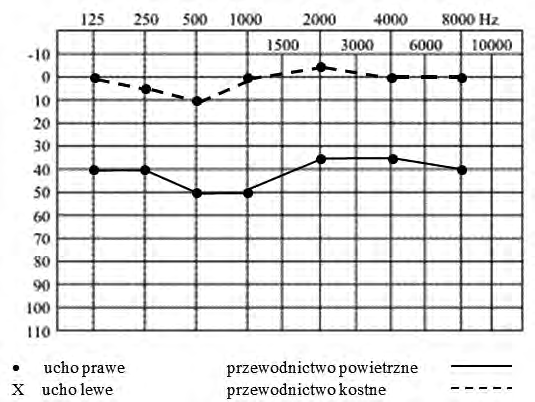
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez