Pytanie 1
Zwiększenie efektu toksycznego jednej substancji chemicznej poprzez inną substancję, która jest jednocześnie dostarczana do organizmu, nazywa się działaniem
Wynik: 21/40 punktów (52,5%)
Wymagane minimum: 20 punktów (50%)
Zwiększenie efektu toksycznego jednej substancji chemicznej poprzez inną substancję, która jest jednocześnie dostarczana do organizmu, nazywa się działaniem
Zgodnie z informacją zawartą w ramce zawartość jonów chlorkowych i jodkowych w roztworze można oznaczyć
Zasada oznaczenia zawartości jonów chlorkowych i jodkowych w roztworze. Podstawą metody jest reakcja strąceniowa zachodząca między jonami Cl- i I- a jonami Ag+. Oznaczenie polega na badaniu zmian potencjału elektrody wskaźnikowej podczas dodawania do analizowanego roztworu, mianowanego roztworu AgNO3. |
Woda obecna w cząsteczce Ca(OH)2 określana jest jako woda
Zamieszczony opis definiuje wskaźniki stosowane w miareczkowaniu
| Substancje te zmieniają zabarwienie w zależności od zmiany stężenia jonów wodorowych w roztworze. Są to słabe kwasy lub zasady organiczne, których barwa niezdysocjowanej cząsteczki w roztworze wodnym różni się od barwy jonów. |
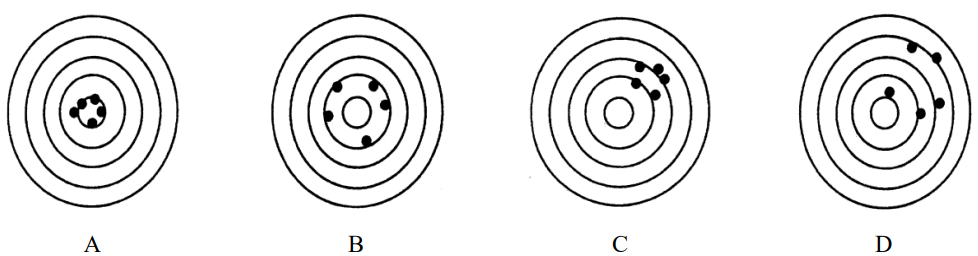
Na rysunkach przedstawiono serie pomiarów o różnej dokładności i precyzji (środek najmniejszego okręgu oznacza wartość prawdziwą). Serię pomiarów nieprecyzyjnych, ale dokładnych, przedstawiono na rysunku
Zielonkawo lub żółtozielono zabarwiony płomień palnika sygnalizuje obecność jonów
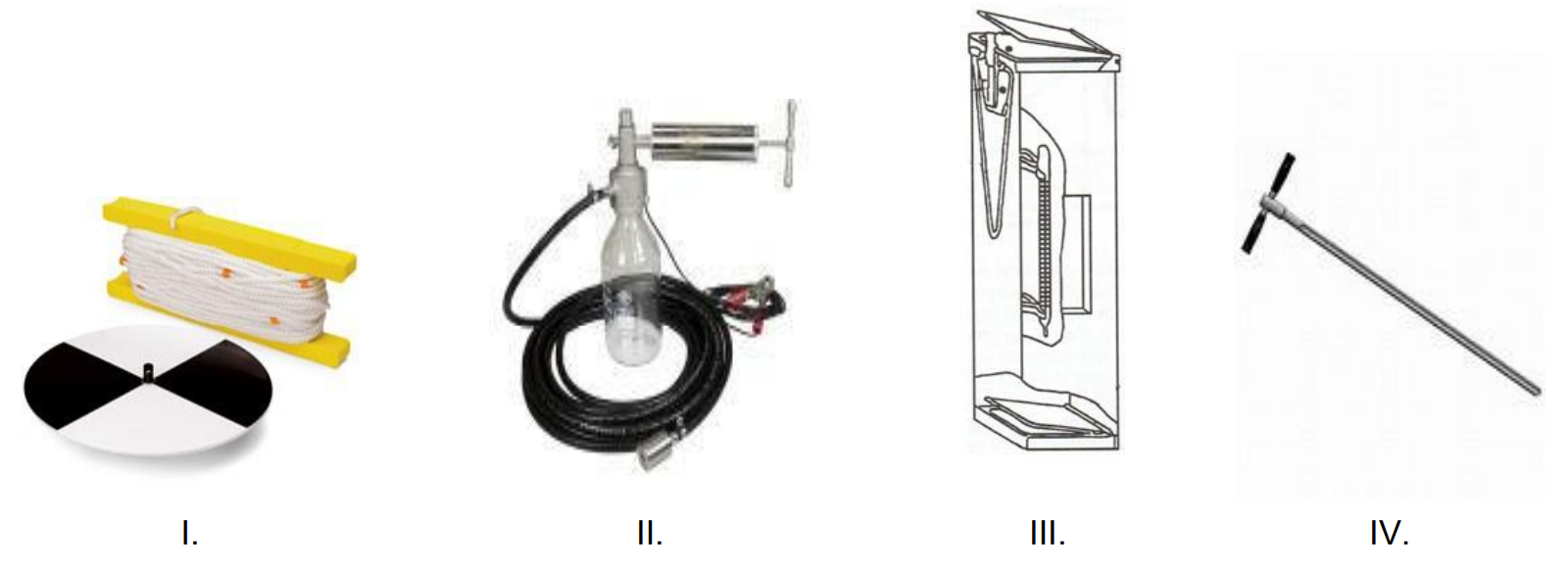
Na którym rysunku przedstawiono sprzęt stosowany do pomiaru mętności wody?
Aby określić wartość absorbancji substancji X, zmierzono, przy tych samych długościach fali, absorbancję mieszaniny X i Y oraz osobno substancji Y.
Jeśli AX+Y = 0,84, a AY = 0,56, to jaka jest wartość AX?
Aby zniwelować oddziaływanie wody obecnej w próbce materiału sypkiego na rezultat analizy składu, próbkę należy poddać
W celu identyfikacji cukru przeprowadzono następujące doświadczenia:
Identyfikowanym cukrem jest
| Doświadczenie | Wynik doświadczenia |
|---|---|
| Próba Trommera | pozytywna |
| Próba Tollensa | pozytywna |
| Hydroliza | nie zachodzi |
Jaką metodę kontroli stanu mikrobiologicznego powietrza opisano w ramce?
| Otwarte płytki Petriego z podłożem stałym pozostawiono na 30 minut na wysokości 1 metra od podłogi, a następnie inkubowano przez 48 godzin w temperaturze 37°C. Po tym czasie wyhodowane kolonie zliczono i zidentyfikowano ich szczepy. |
W temperaturze 20°C wyznaczono gęstość i współczynnik załamania światła kwasu butanowego. Wyniki zestawiono w tabeli:
| Gęstość | Współczynnik załamania światła |
|---|---|
| 0,960 g/cm³ | 1,398 |
RM = (n² − 1) · M
(n² + 2) · d
RM – refrakcja molowa, cm³/mol
n – współczynnik załamania światła
d – gęstość, g/cm³
M – masa molowa, 88 g/mol
Zgodnie z klasyfikacją Bunsena, aniony przypisywane są do jednej z 7 grup analitycznych na podstawie różnic w ich zachowaniu względem jonów
Opisana metoda miareczkowania zaliczana jest do
| Ilościowe oznaczenie cukrów polega na redukcji soli miedzi(II) roztworem cukru, a następnie dodaniu do próbki roztworu KI i odmiareczkowaniu wydzielonego jodu mianowanym roztworem tiosiarczanu sodu |
Równanie przedstawia reakcję zachodzącą podczas oznaczania żelaza metodą miareczkowania
| 5Fe2+ + MnO4- + 8H+ ⇆ 5Fe3+ + Mn2+ + 4H2O |
Na podstawie danych w tabeli określ, który odczynnik należy dobrać, aby wykryć fenyloalaninę metodą chromatografii bibułowej i cienkowarstwowej.
| Substancje wykrywane | Odczynnik | Skład | Efekt barwny |
|---|---|---|---|
| Kwasy karboksylowe | Zieleń bromokrezolowa | 3% roztwór w metanolu z dodatkiem NaOH | Żółte plamy na zielonym tle |
| Aminokwasy | Ninhydryna | 1-2% roztwór w acetonie | Ogrzanie do temp. 110°C charakterystyczne zabarwienie |
| Lipidy | Błękit bromotymolowy | 0,04% roztwór w NaOH o stęż. 0,01 mol/dm3 | Żółte plamy na zielonym tle |
| Barbiturany | Azotan(V) rtęci(II) | 1% roztwór wodny | Czarne lub białe plamy na szarym tle |
W naczyniu rozdzielającym umieszczono wodę oraz eter etylowy (d20 = 0,7138 g/cm3) i dokładnie je wymieszano.
Po chwili można zauważyć
Zjawisko opisane w ramce to
| Jeżeli w wodzie zostanie rozpuszczona α-D-glukopiranoza, to roztwór tuż po rozpuszczeniu wykazuje skręcalność właściwą [α]D= +112,2°, lecz w miarę upływu czasu skręcalność ta stopniowo spada do wartości charakterystycznej w stanie równowagi, mianowicie [α]D= +52,7° |
Jakiego rodzaju proces uzdatniania wody ilustrują podane równania reakcji chemicznych?
CO2 + Ca(OH)2 → CaCO3 + H2O Ca(HCO3)2 + Ca(OH)2 → 2CaCO3 + 2H2O
Drobnoustroje posiadające zdolność do rozkładu białek oraz peptydów charakteryzują się właściwościami
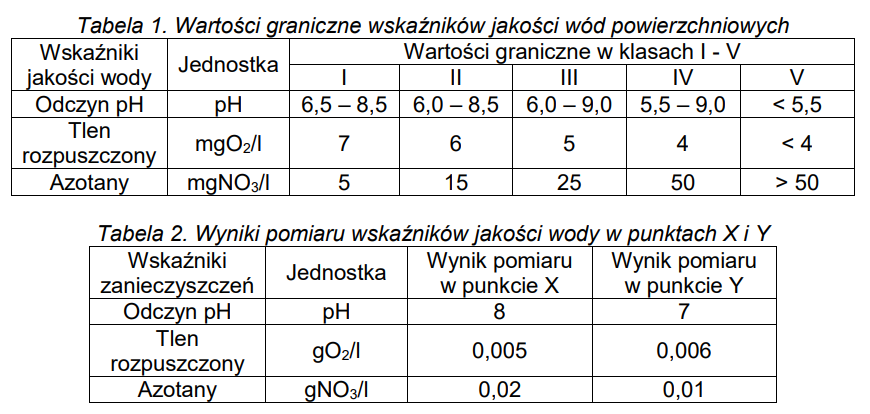
Na podstawie danych w tabelach 1-2 zawierających wartości graniczne wskaźników jakości wody i uzyskane wyniki pomiarowe oceń jakość wody w punktach pomiarowych X i Y, określając jej klasę.
Gęstość wody w temperaturze 25oC wynosi
| T [K] | ||
|---|---|---|
| T [K] | d [g/cm³] | η [cP] |
| 293 | 0,99823 | 1,0050 |
| 298 | 0,99707 | 0,8937 |
| 303 | 0,99567 | 0,8007 |
| 308 | 0,99406 | 0,7225 |
| 313 | 0,99222 | 0,6560 |
| 318 | 0,99025 | 0,5988 |
| 323 | 0,98807 | 0,5494 |
| 328 | 0,98573 | 0,5064 |
| 333 | 0,98324 | 0,4688 |
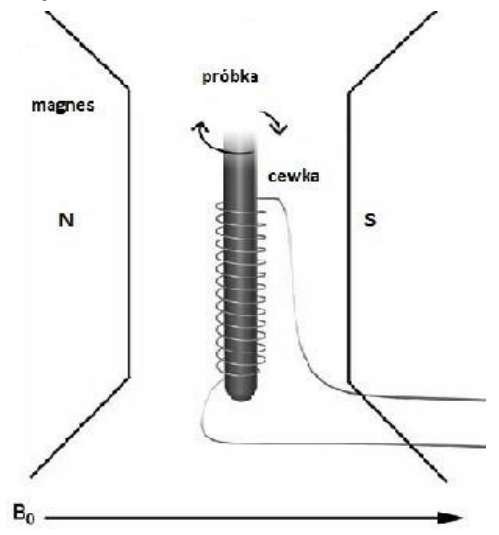
Na rysunku przedstawiono schemat aparatury do
W obecności anionów siarczanowych SO42- w roztworze wodnym, ich obecność można zweryfikować, dodając roztwór
Zjawisko, w którym obce jony są mechanicznie zatrzymywane przez szybko rosnący kryształ, określane jest mianem
W badaniach dotyczących kinetyki hydrolizy sacharozy wykorzystuje się mierzenie aktywności optycznej cukrów, które określa się
Jakie składniki odżywcze w żywności są identyfikowane za pomocą odczynników Fehlinga I i II?
Na rysunku przedstawiono schemat blokowy
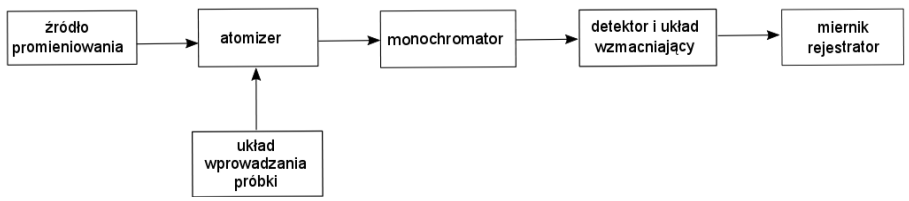
Na diagramie słupkowym przedstawiono wyniki analizy sitowej surowca w formie proszkowej. W jakiej kolejności zamontowano sita w wytrząsarce, licząc je od naczynia zbierającego?
W tabeli przedstawiono gęstość wodnych roztworów gliceryny w temperaturze 20°C w zależności od jej stężenia wyrażonego w % wagowych.
Z informacji zawartych w tabeli wynika, że stężenie gliceryny o gęstości 1,10 g/cm³ wynosi
| % wagowy gliceryny | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
|---|---|---|---|---|---|---|---|---|---|---|
| [g/cm3] gęstość | 1,022 | 1,047 | 1,072 | 1,099 | 1,126 | 1,153 | 1,180 | 1,208 | 1,235 | 1,261 |
Na rysunkach przedstawiono serie pomiarów o różnej dokładności i precyzji (środek najmniejszego okręgu oznacza wartość prawdziwą). Serię pomiarów precyzyjnych, ale niedokładnych przedstawiono na rysunku
Jaką substancję podstawową powinno się użyć do ustalania miana roztworu wodorotlenku sodu?
Na ilustracji przedstawiono

Na rysunku przedstawiono aparat służący do badania zawartości wody w surowcach metodą
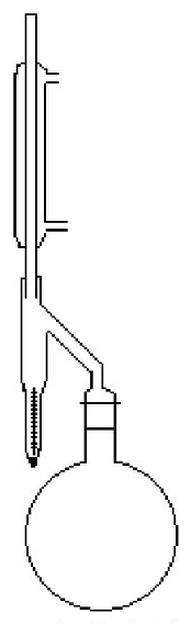
Której z metod nie wykorzystuje się do pomiaru stężenia soli w solankach?
Wskaż grupę związków chemicznych powodujących twardość niewęglanową wody.
| A. | CaSO4, MgCl2, Ca(NO3)2, MgSO4 |
| B. | CaCl2, Ca(HCO3)2, MgCl2, MnSO4 |
| C. | Ca(NO3)2, Ca(HCO3)2, MgCl2, MnSO4 |
| D. | CaCO3, Mg(HCO3)2, MgSO4, Ca(NO3)2 |
Podłoże, które jest wykorzystywane do uzyskiwania hodowli z wysoką liczbą drobnoustrojów danego szczepu, nazywamy
W jakim oznaczeniu wskaźnik reaguje z titrantem, prowadząc do powstania barwnego osadu?
Wskaź kationy, które są możliwe do wykrycia poprzez próbę płomieniową?
Jakim odczynnikiem grupowym IV grupy analitycznej kationów jest?