Pytanie 1
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
Wynik: 30/40 punktów (75,0%)
Wymagane minimum: 20 punktów (50%)
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
Diagnozowanie metodą PET oparte jest na zjawisku
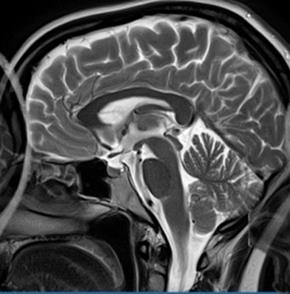
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
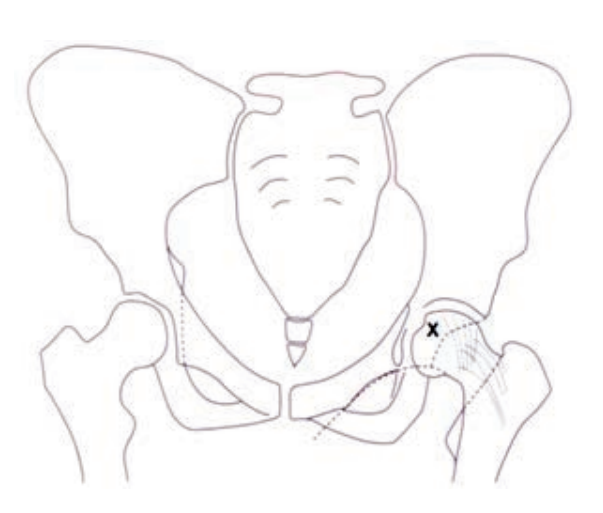
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
Bezwzględnym przeciwwskazaniem do badania spirometrycznego jest
Do badania MR nadgarstka pacjenta należy ułożyć
Standardowe badanie USG średniej wielkości piersi wykonuje się głowicą w zakresie częstotliwości
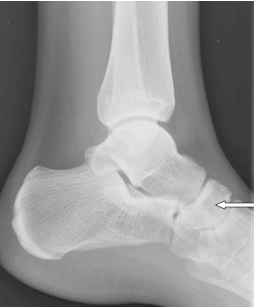
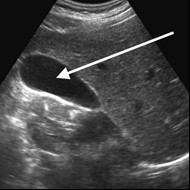
Na radiogramie strzałką oznaczono
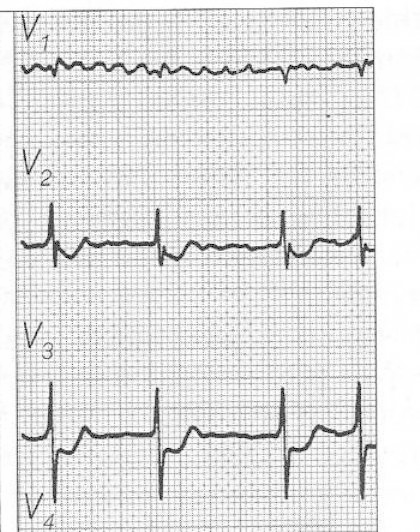
Zamieszczony elektrokardiogram przedstawia
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Które badanie, zgodnie z zakresem kompetencji, może samodzielnie wykonać technik elektroradiolog?
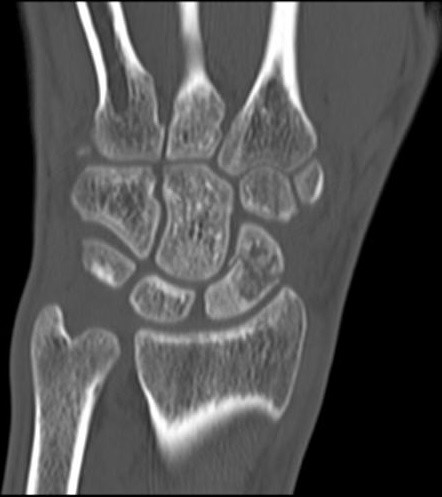
Na obrazie TK nadgarstka uwidocznione jest złamanie kości
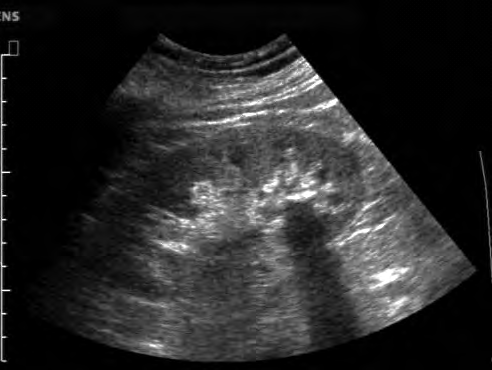
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
Który system informatyczny jest wykorzystywany do archiwizowania i przesyłania obrazów na stacje diagnostyczne w standardzie DICOM?
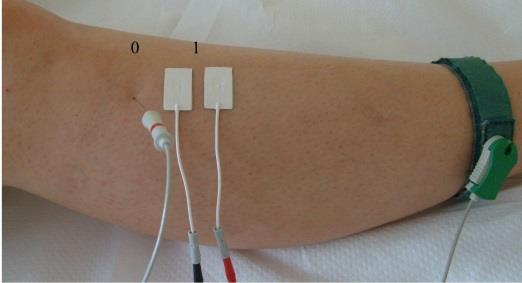
Na ilustracji przedstawiono przygotowanie pacjenta do badania
Który wynik badania tympanometrycznego potwierdza, że słuch badanego pacjenta jest w granicach normy?
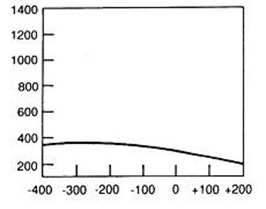
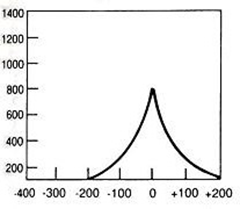
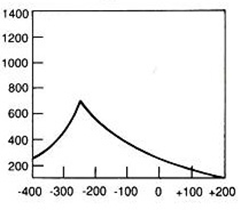
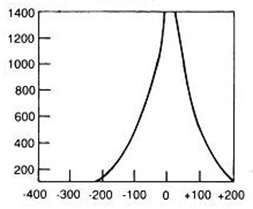
Przy podejrzeniu ciała obcego w oczodole należy wykonać
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
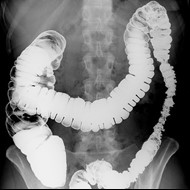
Przedstawiony obraz radiologiczny został zarejestrowany podczas badania jelita
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
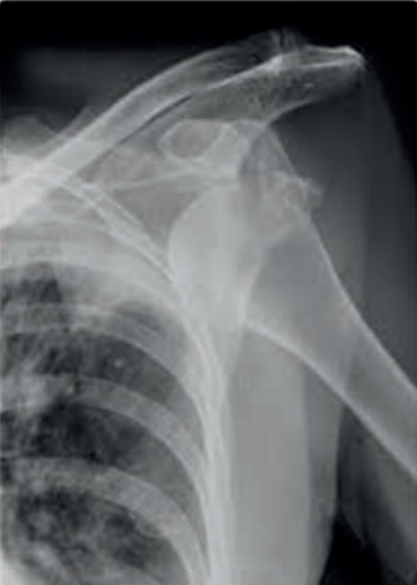
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
Jaki sposób frakcjonowania dawki jest stosowany w radioterapii konwencjonalnej?
Zdjęcie zatok przynosowych wykonuje się w pozycji
Parametr SNR w obrazowaniu MR oznacza
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
W badaniu cystografii wstępującej środek kontrastowy należy podać
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
Wskazaniem do wykonania badania spirometrycznego jest
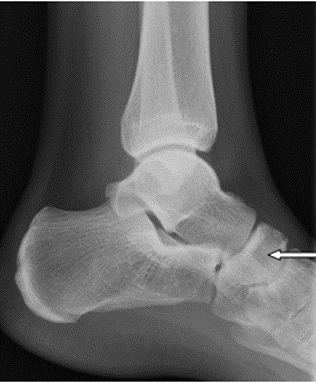
Na zamieszczonym radiogramie strzałką oznaczono kość
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
W obrazowaniu MR wykorzystuje się moment magnetyczny
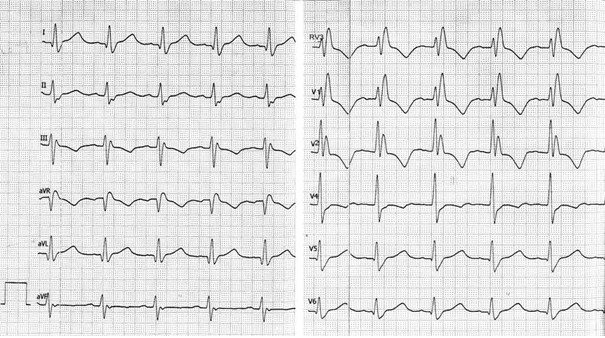
Przedstawiony zapis elektrokardiograficzny może wskazywać na
Który radioizotop jest emiterem promieniowania alfa?
Rutynowe badanie koronarografii prawej tętnicy wieńcowej wykonywane jest w rzucie skośnym przednim
W badaniu EKG elektrodę przedsercową V4 należy umocować