Pytanie 1
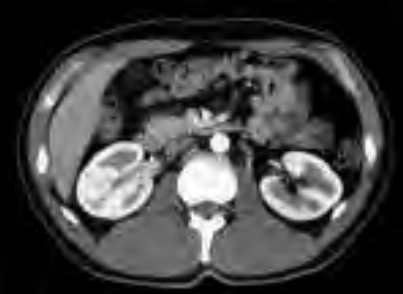
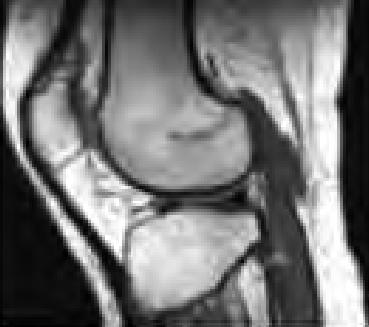
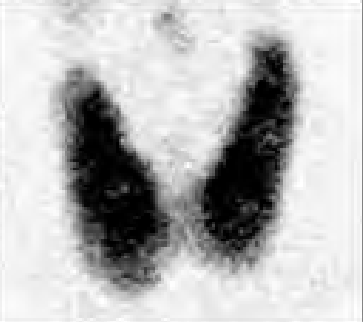
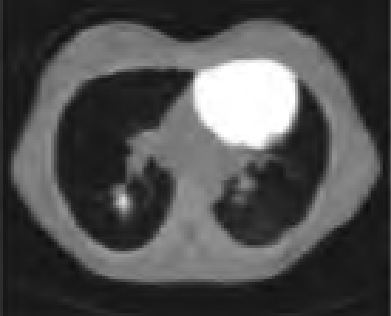
Na którym obrazie zarejestrowano badanie scyntygraficzne?
Wynik: 35/40 punktów (87,5%)
Wymagane minimum: 20 punktów (50%)
Na którym obrazie zarejestrowano badanie scyntygraficzne?




Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
W przypadku migotania komór w zapisie EKG występuje
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
W celu wykonania badania scyntygraficznego układu kostnego radiofarmaceutyk należy podać pacjentowi
Na zamieszczonym obrazie RM nadgarstka lewego strzałką wskazano kość
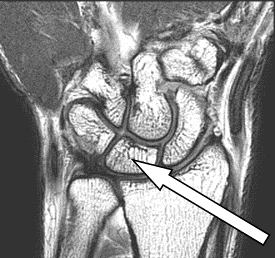
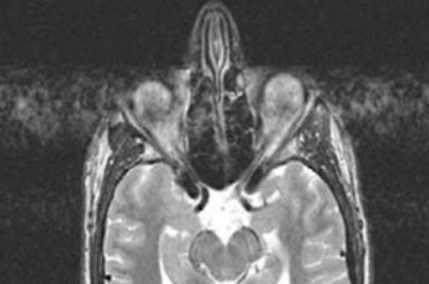
Co jest przyczyną artefaktu widocznego na obrazie MR?
Który radioizotop jest emiterem promieniowania alfa?
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
Teleterapia polega na napromienowaniu
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
Które badanie, zgodnie z zakresem kompetencji, może samodzielnie wykonać technik elektroradiolog?
Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Pomiar densytometryczny BMD metodą DXA z kręgosłupa powinien obejmować kręgi
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
W medycynie nuklearnej wykorzystuje się:
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
W której technice obrazowania zostają zarejestrowane jednocześnie dwa przeciwbieżne kwanty promieniowania gamma o równej energii 511 keV?
W celu unieruchomienia okolicy badanej podczas wykonywania zdjęcia nadgarstka u osoby dorosłej należy zastosować
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
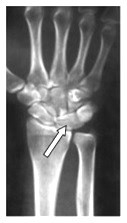
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
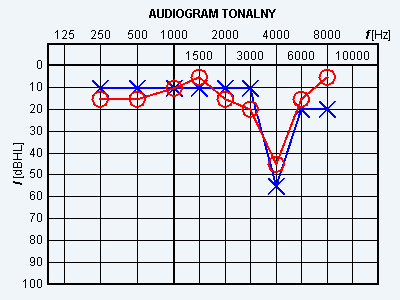
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
Przy podejrzeniu ciała obcego w oczodole należy wykonać
Obrazy DDR są tworzone w trakcie
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm × 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Zdjęcie zatok przynosowych wykonuje się w pozycji
Wskazaniem do zastosowania brachyterapii w leczeniu radykalnym jest rak
Który detektor w radiografii wymaga laserowego czytnika obrazu?
Największa wartość energii promieniowania stosowanego w radioterapii jest generowana przy użyciu
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Pielografia to badanie układu
W badaniu audiometrycznym do oceny przewodnictwa kostnego wybranego ucha słuchawkę kostną należy przyłożyć do
Na obrazie MR kręgosłupa lędźwiowego strzałką wskazano