Pytanie 1
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Wynik: 39/40 punktów (97,5%)
Wymagane minimum: 20 punktów (50%)
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

W badaniu EEG w systemie „10-20” elektrody w okolicy skroniowej oznaczone są literą
Które czynności wykonuje technik elektroradiolog w pracowni „gorącej”?
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Limfografia to badanie kontrastowe
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
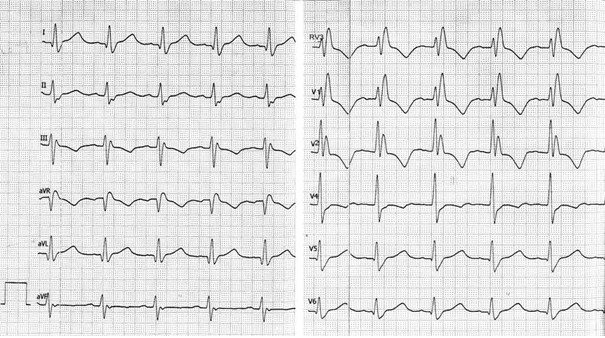
W zapisie EKG prawidłowego rytmu zatokowego wszystkie załamki P są
Promieniowanie jonizujące pośrednio to
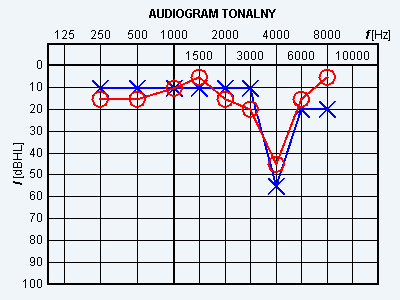
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
W radiologii stomatologicznej ząb o numerze 23 to kieł
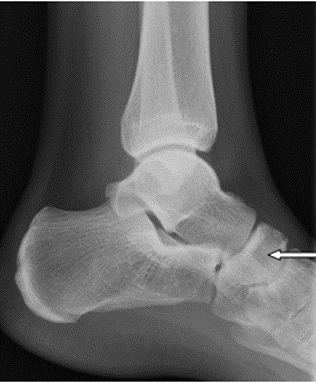
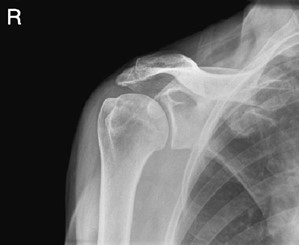
Na zamieszczonym radiogramie strzałką oznaczono kość
„Ognisko zimne” w obrazie scyntygraficznym oznacza
W której pozycji wykonuje się zdjęcie jamy brzusznej u pacjenta z podejrzeniem perforacji żołądka?
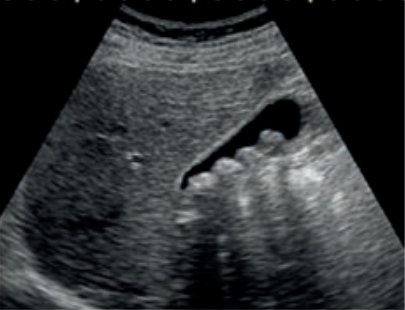
Jakie struktury anatomiczne uwidoczniono na obrazie USG?
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
Na radiogramie uwidoczniono
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
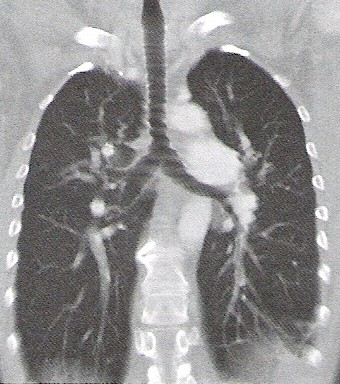
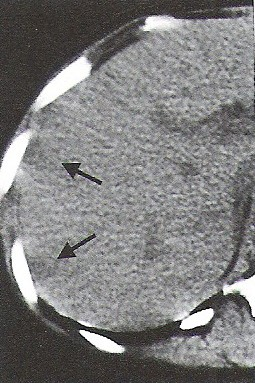
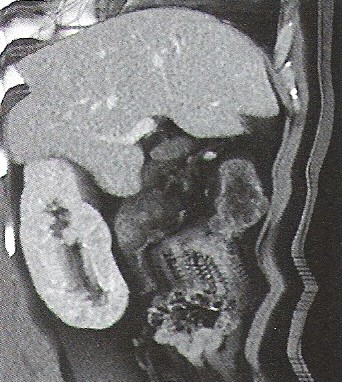
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
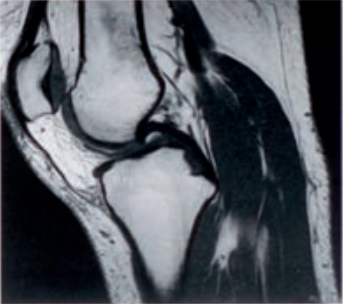
Którą metodę badania zastosowano w obrazowaniu stawu kolanowego?
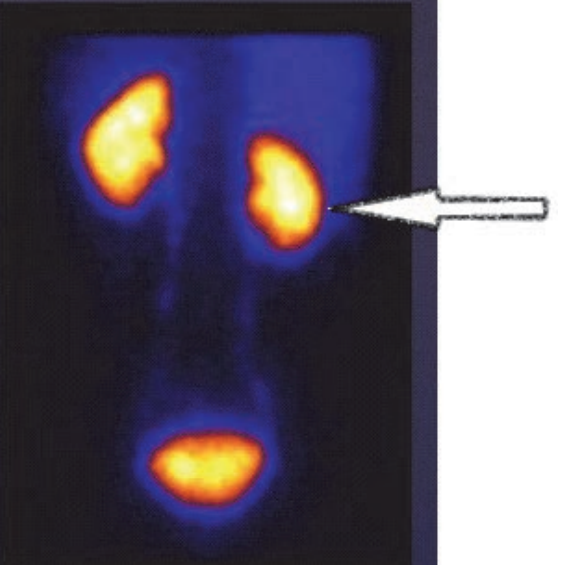
Na scyntygramie strzałką oznaczono
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
W radioterapii hadronowej leczenie odbywa się przy użyciu
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
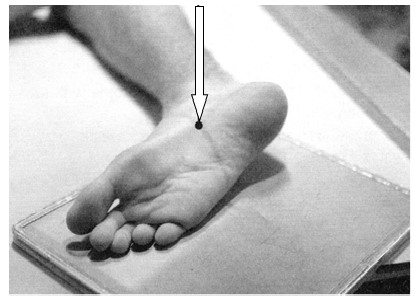
Na ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
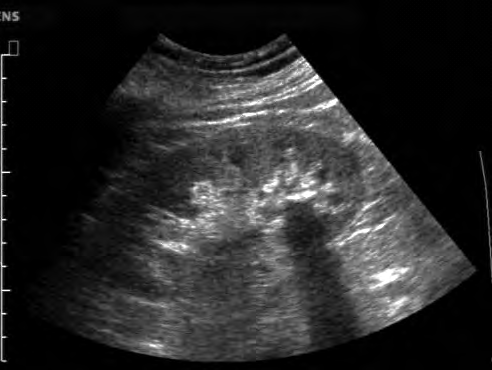
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono
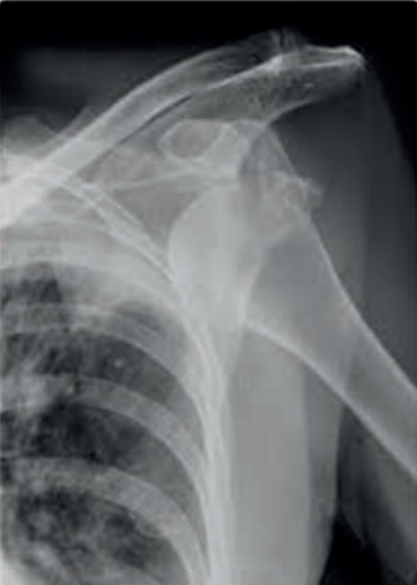
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
Przedstawiony zapis elektrokardiograficzny może wskazywać na