Pytanie 1
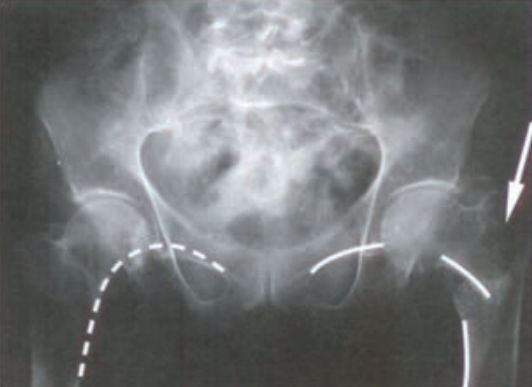
Radiogram przedstawia
Wynik: 26/40 punktów (65,0%)
Wymagane minimum: 20 punktów (50%)
Radiogram przedstawia

Na zamieszczonej rycinie przedstawiono
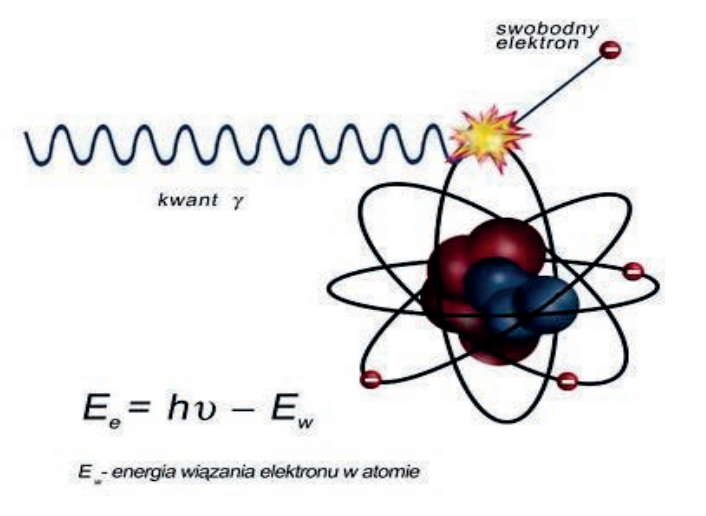
W ultrasonografii występuje zależność:
Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
Na elektrokardiogramie strzałki wskazują załamki
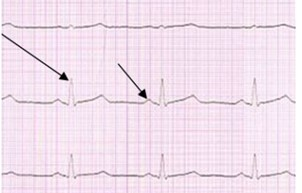
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
Proces chemicznego wywoływania radiogramów polega na
Na scyntygramie kości strzałkami oznaczono ogniska
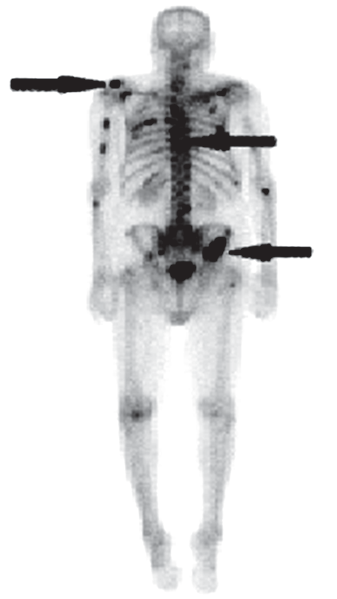
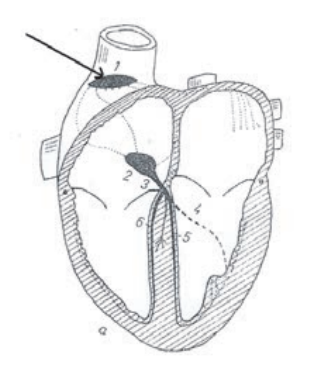
Strzałką na schemacie oznaczono
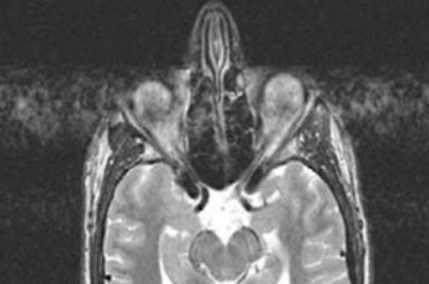
Co jest przyczyną artefaktu widocznego na obrazie MR?
W brachyterapii MDR stosowane są dawki promieniowania
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
Dawka graniczna wyrażona jako dawka skuteczna (efektywna), dla osób zawodowo narażonych na działanie promieniowania jonizującego wynosi w ciągu roku kalendarzowego
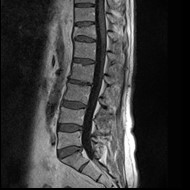
Na obrazie uwidoczniono złamanie kompresyjne kręgu
Objawem późnego odczynu popromiennego po teleradioterapii jest
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
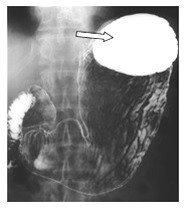
Który element żołądka zaznaczono strzałką na zdjęciu rentgenowskim?
W medycynie nuklearnej wykorzystuje się:
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
Obrazowanie portalowe w radioterapii służy do
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
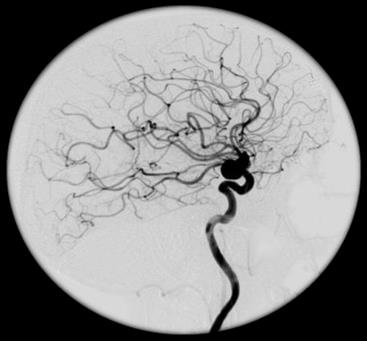
W obrazowaniu MR do uwidocznienia naczyń krwionośnych jest stosowana sekwencja
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?
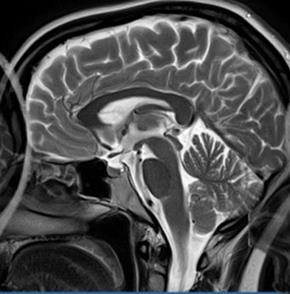
W technice napromieniania SSD mierzona jest odległość źródła promieniowania od
Na zamieszczonym radiogramie strzałką oznaczono kość
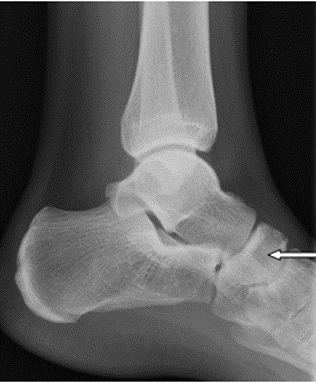
Przedstawiony obraz został zarejestrowany podczas wykonania
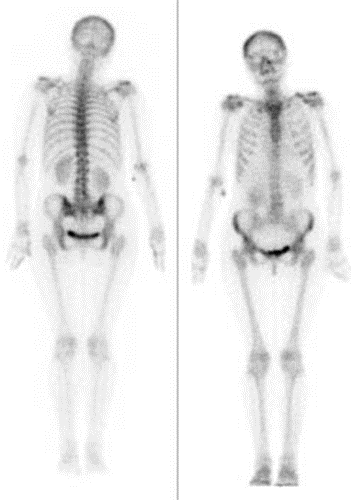
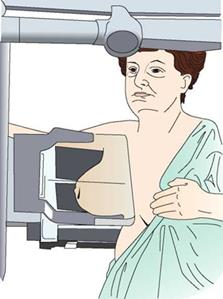
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
Rytm alfa i beta rejestruje się podczas badania
W radiologii stomatologicznej ząb o numerze 23 to kieł
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
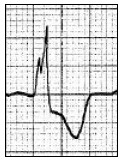
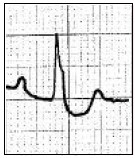
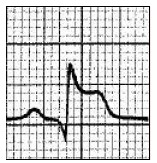
Który zapis EKG przedstawia falę Pardee'go?

Badanie metodą Dopplera umożliwia
Świeżo wynaczyniona krew na obrazach TK głowy bez podania środka kontrastowego ukazuje się jako obszar
Do badania MR nadgarstka pacjenta należy ułożyć
W radioterapii hadronowej leczenie odbywa się przy użyciu
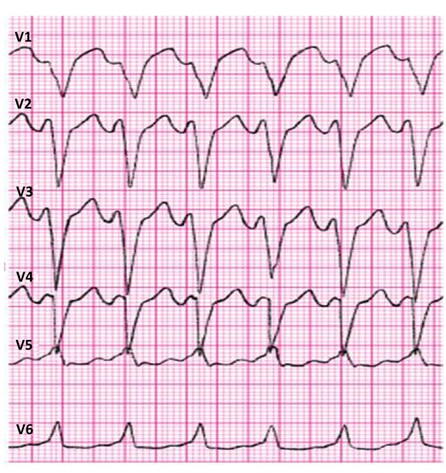
Które zaburzenie rytmu serca zarejestrowano na elektrokardiogramie?
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
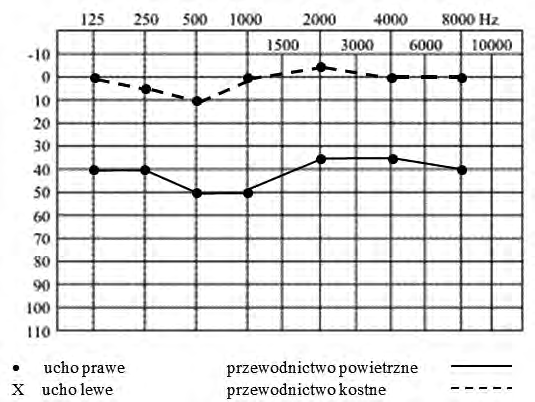
W której próbie stroikowej przystawia się stroik do czoła (u podstawy nosa) lub na szczycie głowy i porównuje się przewodnictwo kostne ucha prawego i lewego?