Pytanie 1
Promieniowanie rentgenowskie jest
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Promieniowanie rentgenowskie jest
W przypadku migotania komór w zapisie EKG występuje
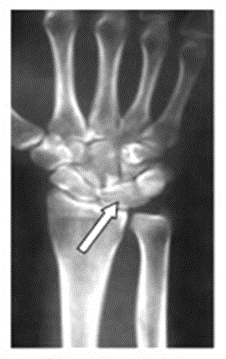
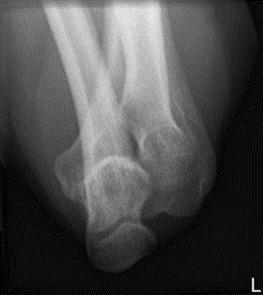
Na zamieszczonym obrazie radiologicznym nadgarstka strzałką wskazano kość
Planowany obszar napromieniania PTV obejmuje
Badanie metodą Dopplera umożliwia
W metodzie RM (rezonansu magnetycznego) po umieszczeniu pacjenta w silnym, stałym polu magnetycznym dochodzi do oddziaływania
Obraz stawu kolanowego otrzymano metodą
W systemie międzynarodowym czwarty górny ząb mleczny po stronie prawej oznacza się symbolem
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
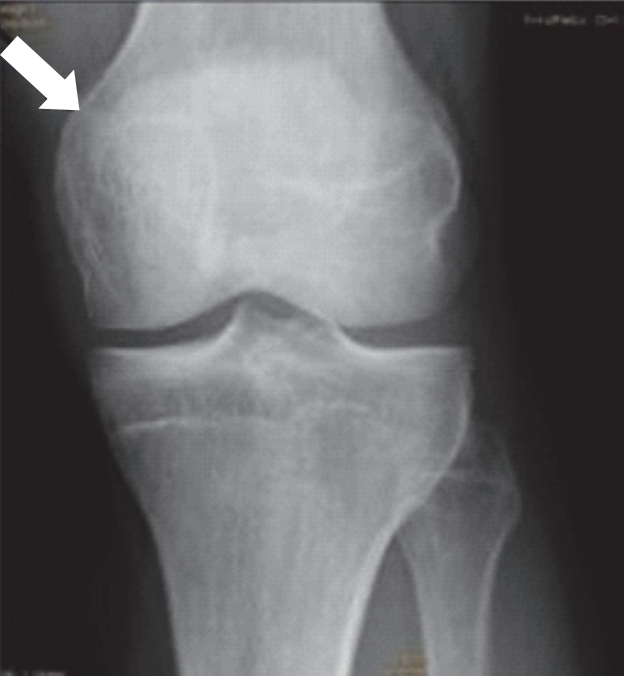
Którą strukturę anatomiczną zaznaczono na radiogramie stawu kolanowego?
Do wykonania stomatologicznego zdjęcia rentgenowskiego techniką kąta prostego promień centralny należy ustawić prostopadle do
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
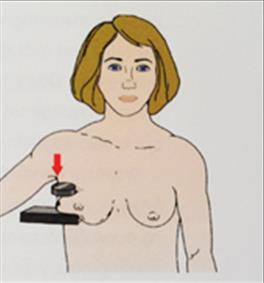
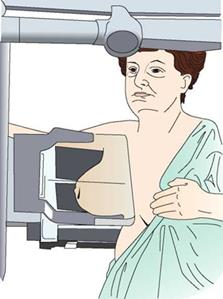
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
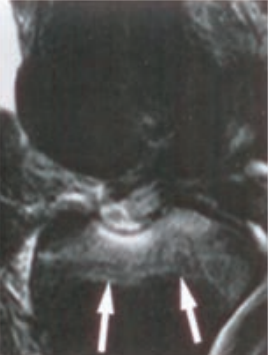
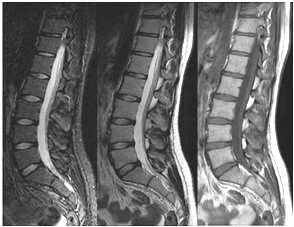
Które kolejne sekwencje badania kręgosłupa lędźwiowego uwidoczniono na przedstawionych obrazach?
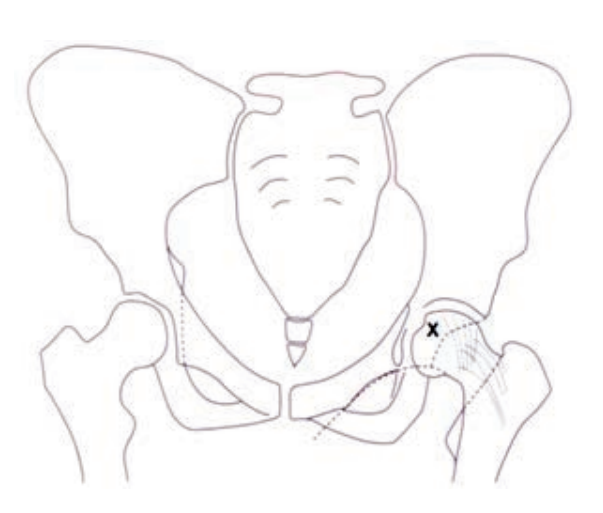
Na rycinie rentgenogramu w projekcji AP symbolem X oznaczono
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Który radioizotop stosuje się do badania scyntygraficznego kości?
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
W standardowym badaniu EEG elektrody P3, P4 i Pz umieszcza się na skórze głowy pacjenta nad płatami
W badaniu EKG punktem przyłożenia odprowadzenia przedsercowego C2 jest
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
Która składowa prawidłowej krzywej EKG odpowiada powolnej repolaryzacji komór mięśnia sercowego?
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
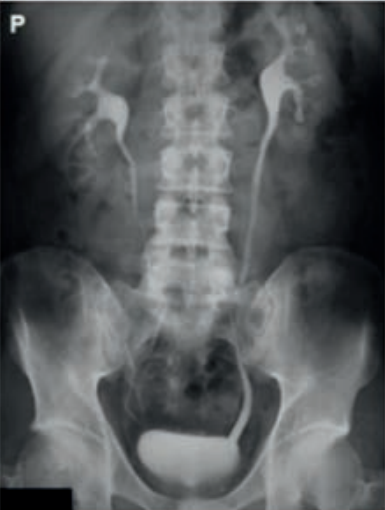
Na rentgenogramie uwidoczniono badanie
Który radiofarmaceutyk może zostać podany pacjentowi w scyntygrafii perfuzyjnej mózgu?
Podczas badania EEG w systemie „10-20” literą A oznacza się elektrody
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Na obrazie uwidoczniono
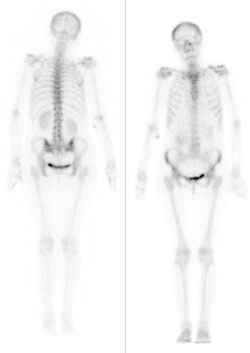
Która metoda diagnostyczna służy do określenia gęstości minerału kostnego w ujęciu objętościowym g/cm³?
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
Technikę bramkowania oddechowego stosuje się w badaniu MR
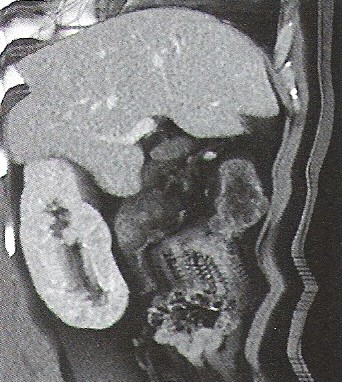
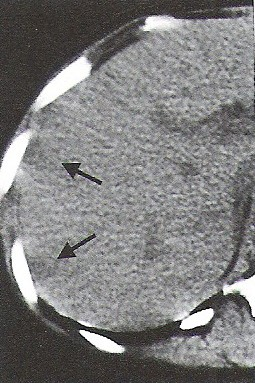
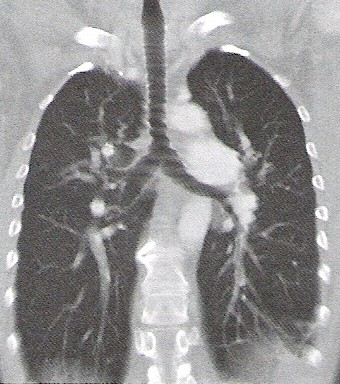
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
Koronarografia jest radiologicznym zabiegiem diagnostycznym pozwalającym ocenić drożność
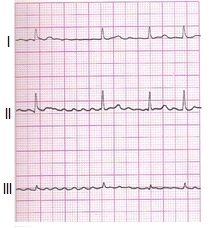
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
Do wczesnych odczynów popromiennych po radioterapii zalicza się