Pytanie 1
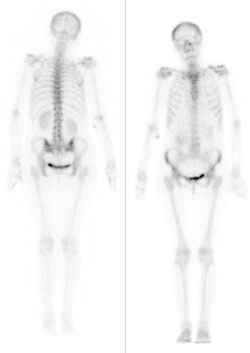
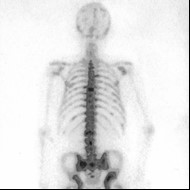
SPECT to
Brak odpowiedzi na to pytanie.
Prawidłowo, SPECT to tomografia emisyjna pojedynczego fotonu (Single Photon Emission Computed Tomography). Jest to klasyczne badanie medycyny nuklearnej, gdzie pacjentowi podaje się radiofarmaceutyk emitujący promieniowanie gamma, a następnie gammakamera obraca się wokół ciała i rejestruje pojedyncze fotony wychodzące z organizmu. Z tych sygnałów komputer rekonstruuje przekrojowe obrazy 3D rozkładu znacznika w tkankach. W praktyce klinicznej SPECT wykorzystuje się np. w kardiologii do oceny perfuzji mięśnia sercowego (badania obciążeniowe, niedokrwienie, przebyte zawały), w neurologii do oceny ukrwienia mózgu, w ortopedii i onkologii do scyntygrafii kości czy lokalizacji ognisk zapalnych. Moim zdaniem ważne jest, żeby kojarzyć, że SPECT pokazuje przede wszystkim funkcję i metabolizm tkanek, a nie tylko ich budowę anatomiczną, jak klasyczna TK. Standardowo stosuje się radiofarmaceutyki oparte o technet-99m, które mają dobre parametry energetyczne i krótki czas półtrwania, co jest zgodne z zasadą ALARA i dobrą praktyką ochrony radiologicznej. Obrazy SPECT często łączy się z TK w jednym urządzeniu (SPECT/CT), co pozwala na precyzyjną lokalizację zmian w anatomii pacjenta – to jest obecnie złoty standard w wielu pracowniach medycyny nuklearnej. W technice ważne jest też prawidłowe pozycjonowanie pacjenta, odpowiedni czas akwizycji i korekcja osłabienia, żeby uzyskać obrazy dobrej jakości diagnostycznej. Warto zapamiętać: pojedynczy foton = SPECT, pozytony = PET, a brak emisji = klasyczna radiologia projekcyjna lub TK.