Pytanie 1
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

Wynik: 16/40 punktów (40,0%)
Wymagane minimum: 20 punktów (50%)
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

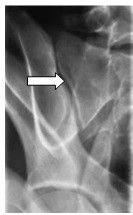
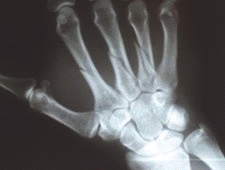
Którą strukturę anatomiczną zaznaczono strzałką na rentgenogramie?
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Jak przebiega promień centralny w projekcji AP czaszki?
Po wykonanej radioterapii do dokumentacji pacjenta należy wpisać dawkę promieniowania w jednostce
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
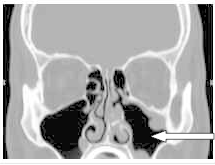
Na obrazie TK zaznaczono zatokę
Do badania MR nadgarstka pacjenta należy ułożyć
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
W medycynie nuklearnej wykorzystuje się:
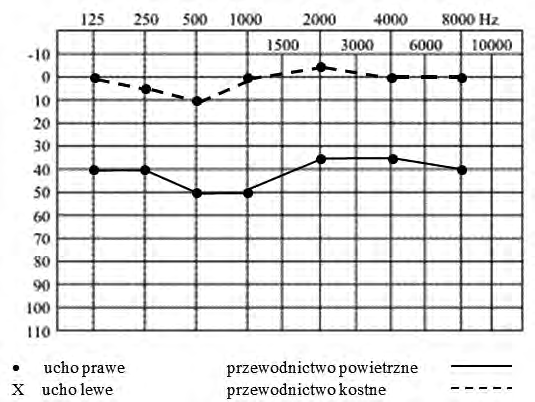
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
Podczas wykonywania zdjęcia rentgenowskiego lewobocznego czaszki promień centralny powinien przebiegać
W scyntygrafii perfuzyjnej płuc pacjentowi podawany jest radioizotop
Teleterapia polega na napromienowaniu
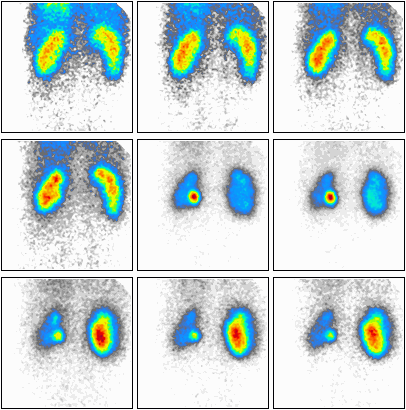
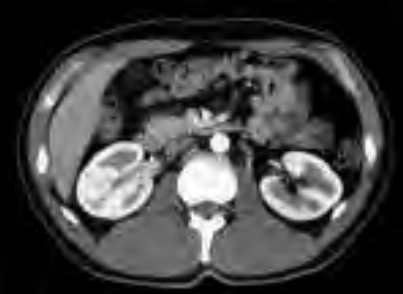
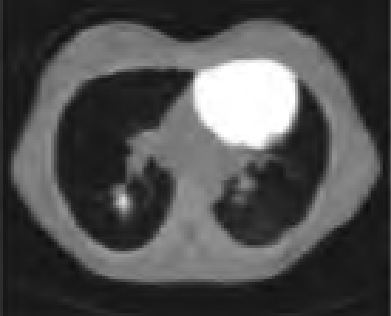
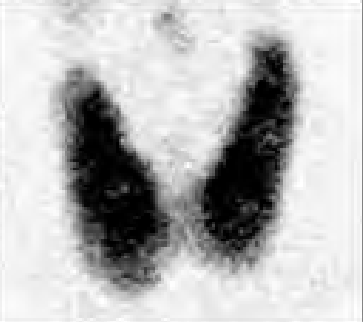
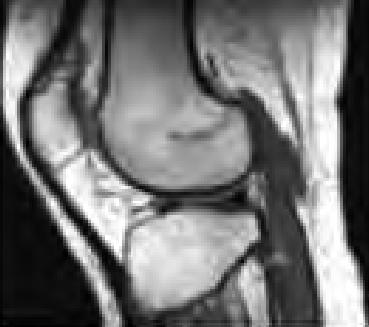
Podczas którego badania zostały zarejestrowane przedstawione obrazy?
Źródłem promieniowania protonowego stosowanego w radioterapii jest
Na którym obrazie zarejestrowano badanie scyntygraficzne?
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
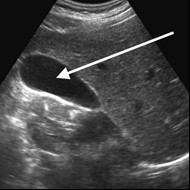
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Którą kasetę należy wykorzystać do wykonania rentgenogramu klatki piersiowej w projekcji bocznej u 35-letniej pacjentki o wzroście 165 cm i wadze 54 kg?
Objawem późnego odczynu popromiennego po teleradioterapii jest
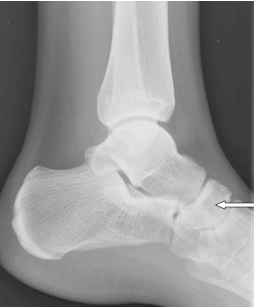
Na radiogramie uwidoczniono złamanie
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
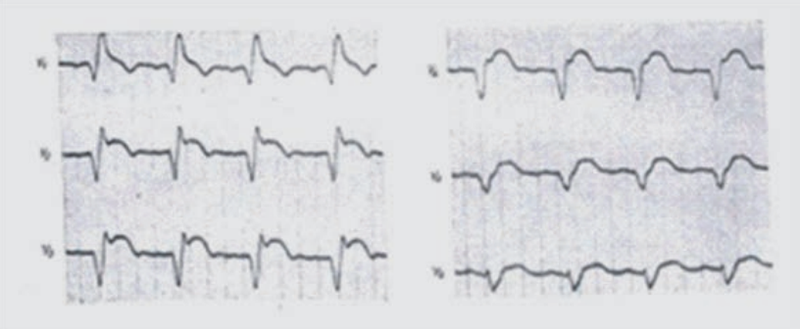
Na elektrokardiogramie zarejestrowano
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
W jakich jednostkach mierzy się natężenie dźwięku?
Obrazowanie portalowe w radioterapii służy do
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Którym skrótem w badaniu spirometrycznym oznaczana jest pojemność życiowa płuc?
Na radiogramie strzałką oznaczono
Brachyterapia wewnątrzprzewodowa jest stosowana w leczeniu
Celiakografia jest badaniem kontrastowym
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
W radioterapii hadronowej leczenie odbywa się przy użyciu
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową