Pytanie 1
Który radioizotop jest emiterem promieniowania alfa?
Wynik: 8/40 punktów (20,0%)
Wymagane minimum: 20 punktów (50%)
Który radioizotop jest emiterem promieniowania alfa?
Centratory laserowe zamontowane w kabinie aparatu terapeutycznego służą do
Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
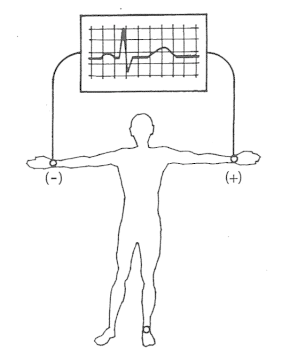
Które odprowadzenie elektrokardiograficzne przedstawiono na ilustracji?
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Rozpoczęcie badania TK nerek po 20-30 sekundach od początku podania środka kontrastowego umożliwia diagnostykę
Który materiał światłoczuły należy zastosować w rentgenodiagnostyce analogowej, by zminimalizować dawkę promieniowania jonizującego otrzymaną przez pacjenta?
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
Która struktura może być oknem akustycznym w badaniu ultrasonograficznym?
Osłony na gonady dla osób dorosłych powinny posiadać równoważnik osłabienia promieniowania nie mniejszy niż
Pojawienie się w zapisie EKG patologicznego załamka Q lub QS może wskazywać na
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Skrótem CTV w radioterapii oznacza się
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Brak odpowiedzi na to pytanie.
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
Brak odpowiedzi na to pytanie.
Obrazy DDR są tworzone w trakcie
Brak odpowiedzi na to pytanie.
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
Brak odpowiedzi na to pytanie.
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy
Brak odpowiedzi na to pytanie.
Który narząd widoczny jest na wydruku badania ultrasonograficznego?
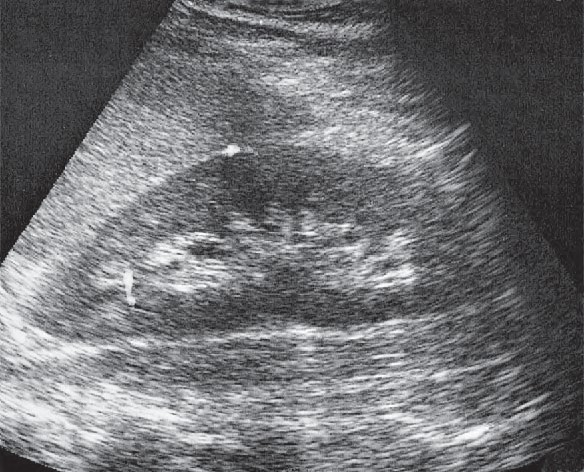
Brak odpowiedzi na to pytanie.
Który elektrokardiogram jest poprawny technicznie?
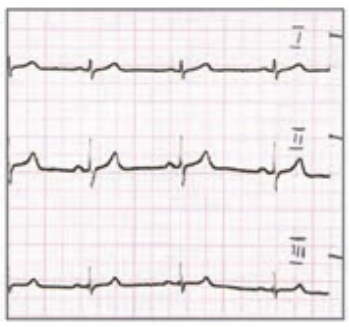
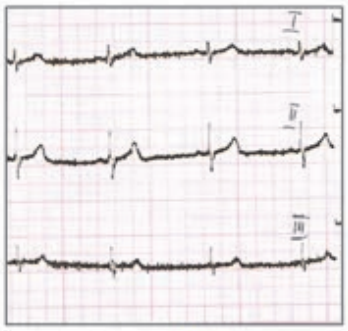
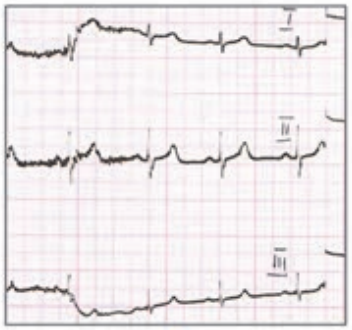
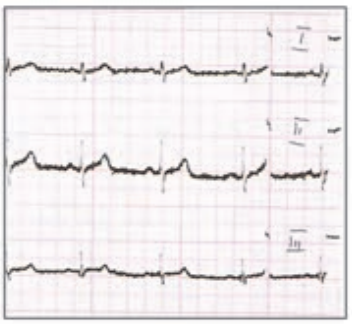
Brak odpowiedzi na to pytanie.
Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
Brak odpowiedzi na to pytanie.
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
Brak odpowiedzi na to pytanie.
W badaniu EKG elektrodę przedsercową V4 należy umocować
Brak odpowiedzi na to pytanie.
Technikę bramkowania oddechowego stosuje się w badaniu MR
Brak odpowiedzi na to pytanie.
Który środek ochrony radiologicznej pacjenta należy zastosować podczas wykonywania zdjęcia bocznego kręgosłupa szyjnego?
Brak odpowiedzi na to pytanie.
Który narząd został uwidoczniony na przedstawionym obrazie scyntygraficznym?
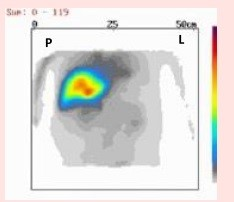
Brak odpowiedzi na to pytanie.
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Brak odpowiedzi na to pytanie.
Rozpraszanie promieniowania X, w wyniku którego następuje zwiększenie długości fali promieniowania, to zjawisko
Brak odpowiedzi na to pytanie.
Który zestaw zdjęć narządów klatki piersiowej należy wykonać u pacjenta z podejrzeniem lewostronnego zapalenia płuc?
Brak odpowiedzi na to pytanie.
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
Brak odpowiedzi na to pytanie.
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Brak odpowiedzi na to pytanie.
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Brak odpowiedzi na to pytanie.
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?
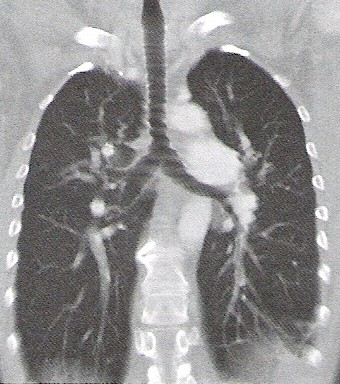
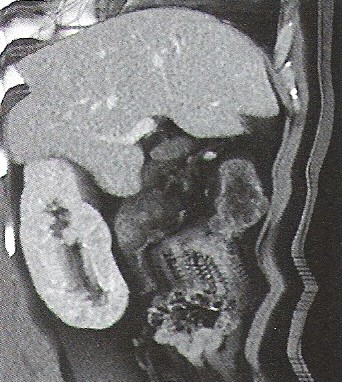
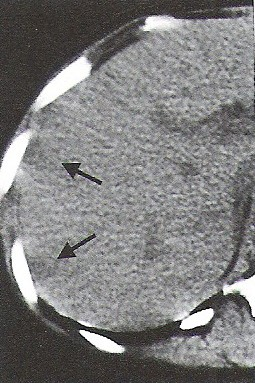

Brak odpowiedzi na to pytanie.
Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje
Brak odpowiedzi na to pytanie.
Pielografia zstępująca umożliwia diagnostykę
Brak odpowiedzi na to pytanie.
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Brak odpowiedzi na to pytanie.
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
Brak odpowiedzi na to pytanie.
Standardowe badanie urografii polega na podaniu pacjentowi środka kontrastującego
Brak odpowiedzi na to pytanie.
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
Brak odpowiedzi na to pytanie.