Pytanie 1
Zamieszczony elektrokardiogram przedstawia
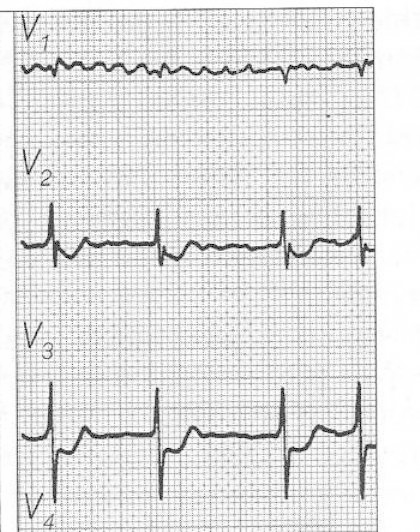
Wynik: 34/40 punktów (85,0%)
Wymagane minimum: 20 punktów (50%)
Zamieszczony elektrokardiogram przedstawia

Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
Przy ułożeniu do zdjęcia AP czaszki płaszczyzna
Na zarejestrowanych obrazach badania renoscyntygraficznego widać, że prawa nerka pacjenta
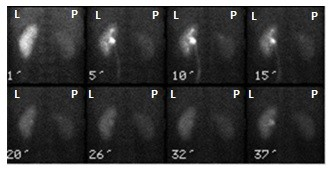
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
Do planowego badania TK klatki piersiowej z użyciem środka cieniującego pacjent powinien zgłosić się
Podczas badania gammakamerą źródłem promieniowania jest
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
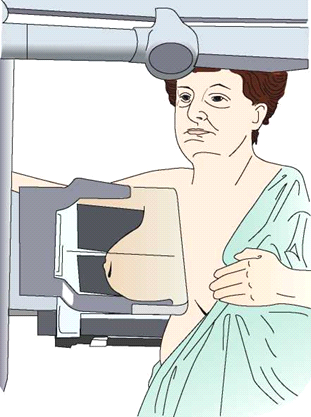
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie
Jaki czas należy ustawić do wykonania zdjęcia rentgenowskiego dwójki górnej lewej?
| Tabela ekspozycji | |||
|---|---|---|---|
| wartości | czasu (s) | napięcia (kV) | natężenia (mA) |
| zęby przedtrzonowe i kły | 0,160 | 60 | 8 |
| siekacze | 0,120 | 60 | 8 |
| zęby trzonowe | 0,200 | 60 | 8 |
| ekspozycja zgryzowo-skrzydełkowa | 0,180 | 66 | 6 |
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
Powierzchnia gabinetu rentgenowskiego, w którym zainstalowany jest aparat rentgenowski wyposażony w oddzielną lampę, nie może być mniejsza niż
Planowany obszar napromieniania PTV obejmuje
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
Ilustracja przedstawia pozycjonowanie pacjentki do badania mammograficznego w projekcji
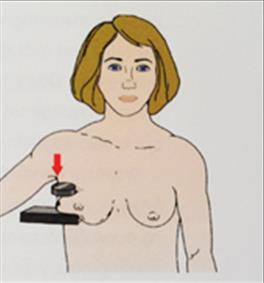
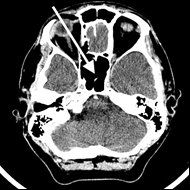
Na radiogramie TK głowy strzałką wskazano
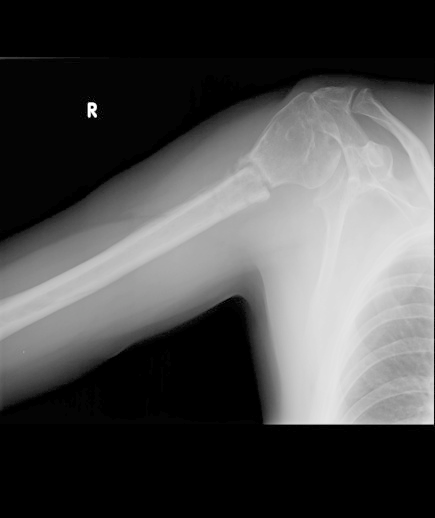
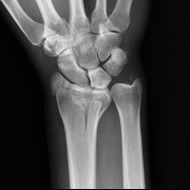
Na radiogramie uwidoczniono złamanie
Promieniowanie rentgenowskie jest
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Po podaniu kontrastu obraz zmian nowotworowych w badaniu MR najlepiej uwidacznia się w sekwencji
Obrazowanie w sekwencjach STIR, FLAIR, SE wykonywane jest w badaniu
Do wczesnych odczynów popromiennych po radioterapii zalicza się
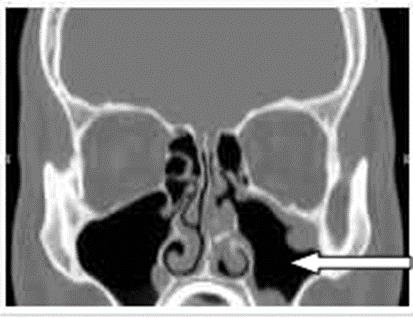
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
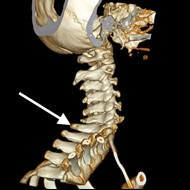
Na obrazie TK kręgosłupa strzałką wskazano wyrostek
W radiologii analogowej lampy rentgenowskiej z tubusem używa się do wykonania zdjęcia
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
Który radioizotop jest emiterem promieniowania alfa?
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Pielografia zstępująca umożliwia diagnostykę
Urografia polega na
Obrazowanie portalowe w radioterapii służy do
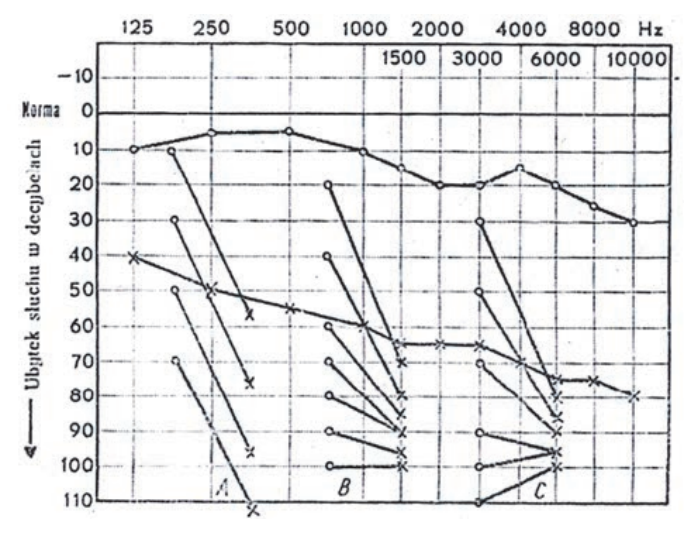
Audiogram przedstawia próbę
Przemiana promieniotwórcza radu w ren opisana wzorem \( {}_{88}^{226}\text{Ra} \to {}_{86}^{222}\text{Rn} + {}_{2}^{4}\text{He} \) jest rozpadem