Pytanie 1
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Wynik: 24/40 punktów (60,0%)
Wymagane minimum: 20 punktów (50%)
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

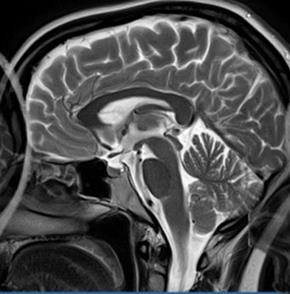
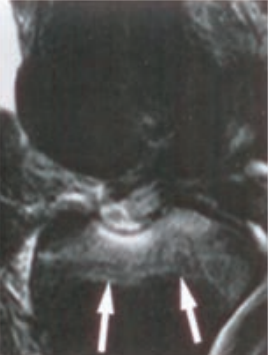
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
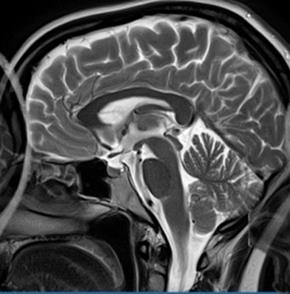
Co jest przyczyną artefaktu widocznego na obrazie MR?
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?
Nieostrość geometryczna obrazu rentgenowskiego zależy od
W scyntygrafii kośćca „ogniska gorące” oznaczają miejsca
Jednym z kryteriów poprawnie wykonanego badania spirometrycznego jest czas trwania natężonego wydechu, który powinien wynosić u osób powyżej 10 roku życia co najmniej
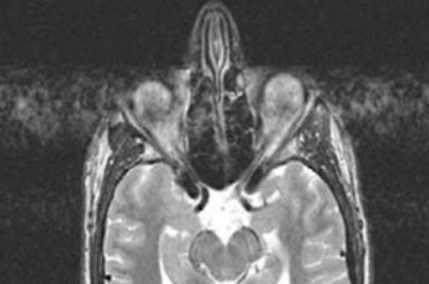
Na przekroju poprzecznym rezonansu magnetycznego strzałką oznaczono
Wskaż osłonę radiologiczną, która jest stosowana w pracowniach radiodiagnostyki stomatologicznej.




Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
Który system informatyczny służy do archiwizacji i transmisji obrazów radiologicznych?
Jak przebiega promień centralny w projekcji AP czaszki?
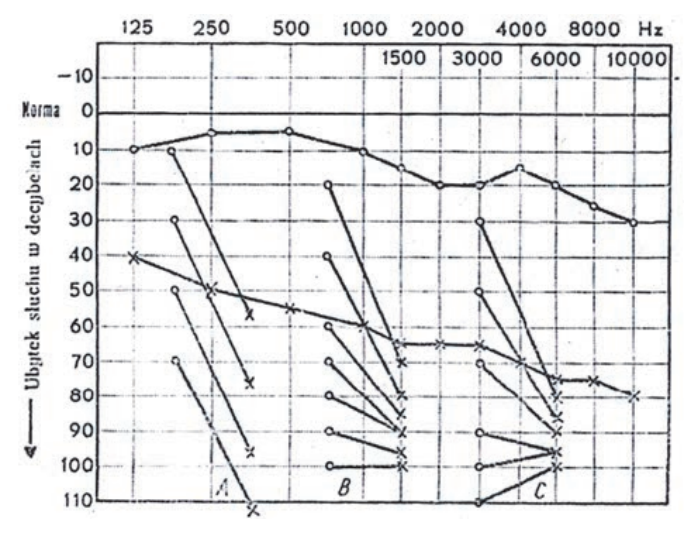
Audiogram przedstawia próbę
Efekt „tea cup” widoczny jest na mammografach wykonanych w projekcji
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
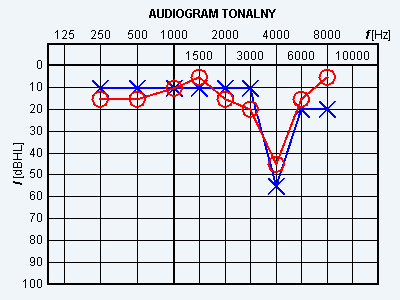
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
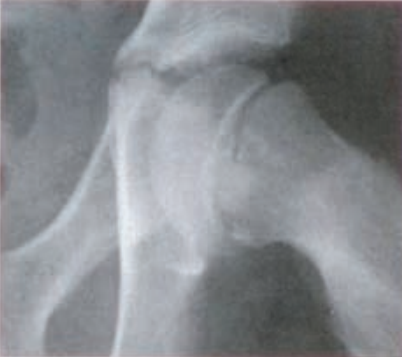
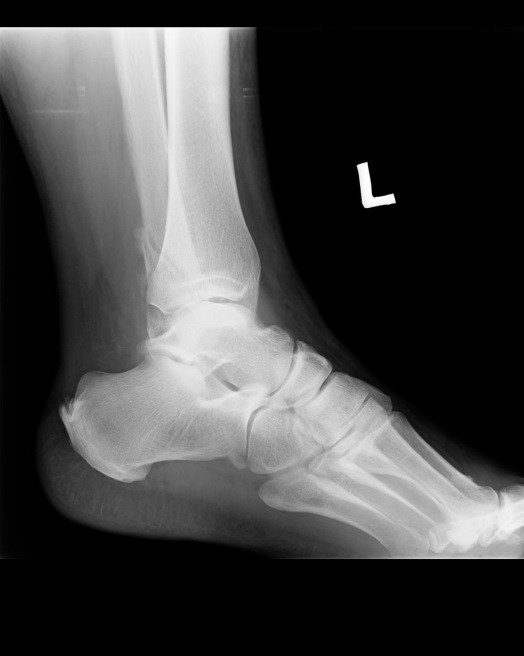
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
Czym charakteryzuje się późny odczyn popromienny?
Gruboziarnista folia wzmacniająca wpływa na zwiększenie na obrazie rentgenowskim nieostrości
Do pomiaru dawek indywidualnych u osób narażonych zawodowo na promieniowanie rentgenowskie są stosowane
Podczas wykonywania zdjęć wewnątrzustnych zębów górnych linia Campera powinna przebiegać w stosunku do płaszczyzny podłogi
Na obrazie radiologicznym uwidoczniono złamanie kości
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
W badaniu audiometrycznym rezerwa ślimakowa to odległość między krzywą
Kolonoskopia to badanie, które ma na celu ocenę błony śluzowej
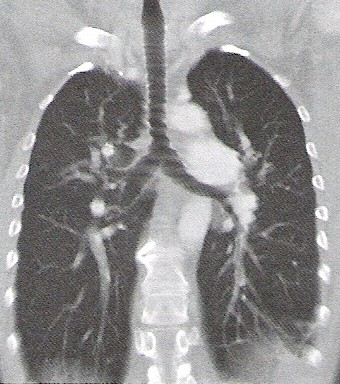
Skrótem HRCT (High Resolution Computed Tomography) określa się tomografię komputerową
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
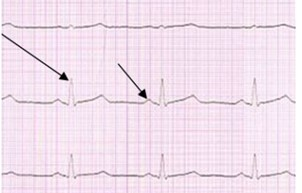
Na elektrokardiogramie strzałki wskazują załamki
W medycznym przyspieszaczu liniowym jest generowana wiązka fotonów o energii w zakresie
W ultrasonografii występuje zależność:
Obraz stawu kolanowego otrzymano metodą
Obrazowanie portalowe w radioterapii służy do
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
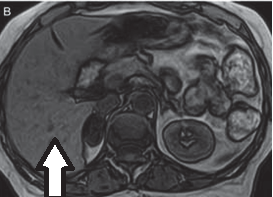
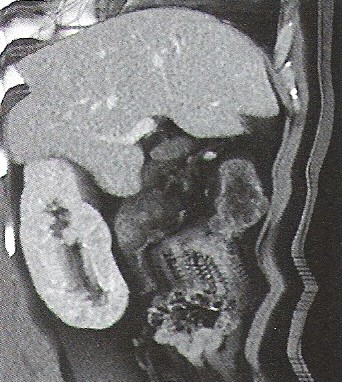
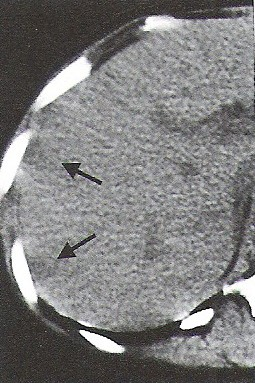
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

W scyntygrafii wykorzystywane są głównie radioizotopy emitujące promieniowanie