Pytanie 1
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Podczas wykonywania badania EEG elektrodę P4 umieszcza się w okolicy
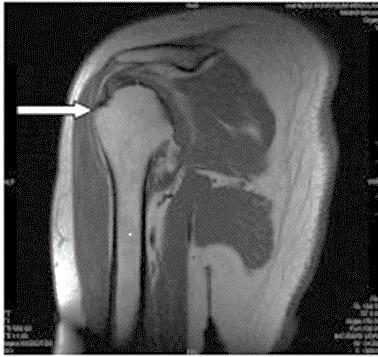
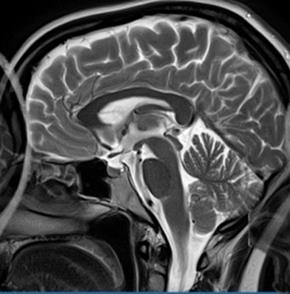
Którą strukturę anatomiczną oznaczono na zamieszczonym obrazie rezonansu magnetycznego?
Lordoza to fizjologiczna krzywizna kręgosłupa występująca
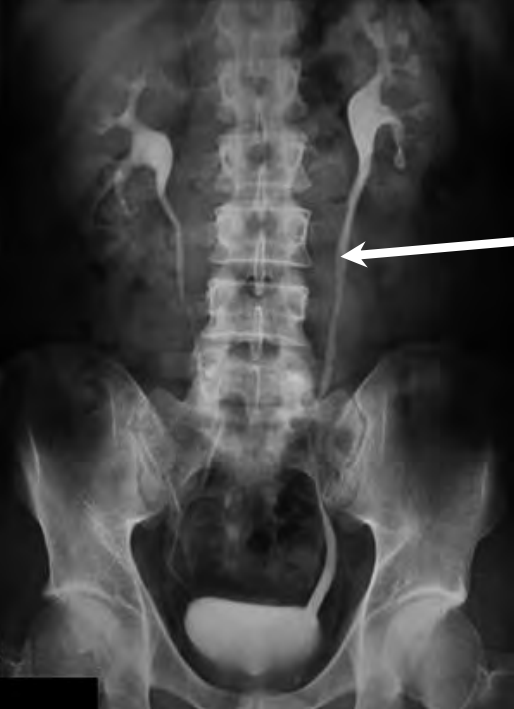
Na prawidłowo przedstawionym radiogramie badania kontrastowego strzałką zaznaczono
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
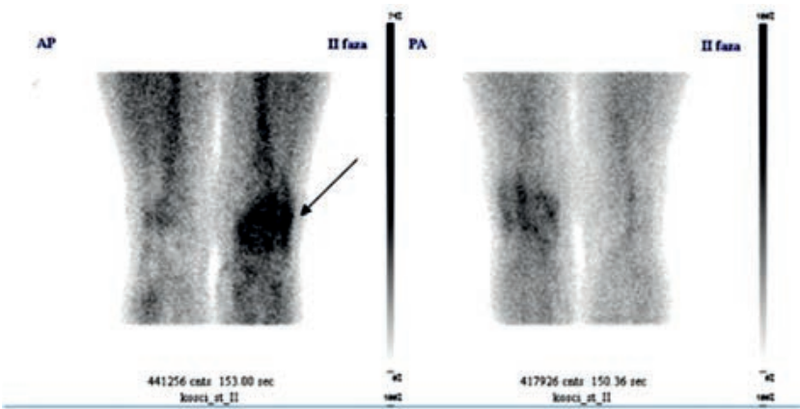
Na przedstawionym scyntygramie ukazano duży obszar
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
W obrazowaniu MR wykorzystuje się moment magnetyczny
Na zamieszczonym przekroju poprzecznym TK kręgosłupa szyjnego strzałką wskazano

W jakich jednostkach mierzy się natężenie dźwięku?
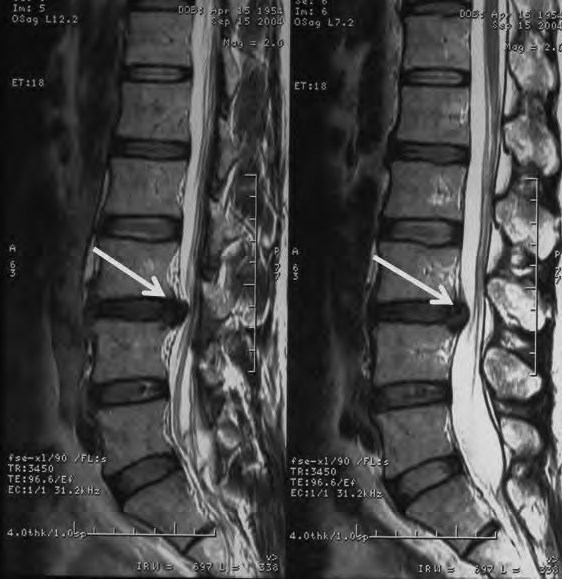
Na obrazie RM uwidoczniono odcinek kręgosłupa
Diagnozowanie metodą PET oparte jest na zjawisku
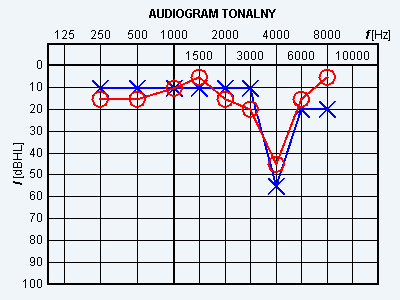
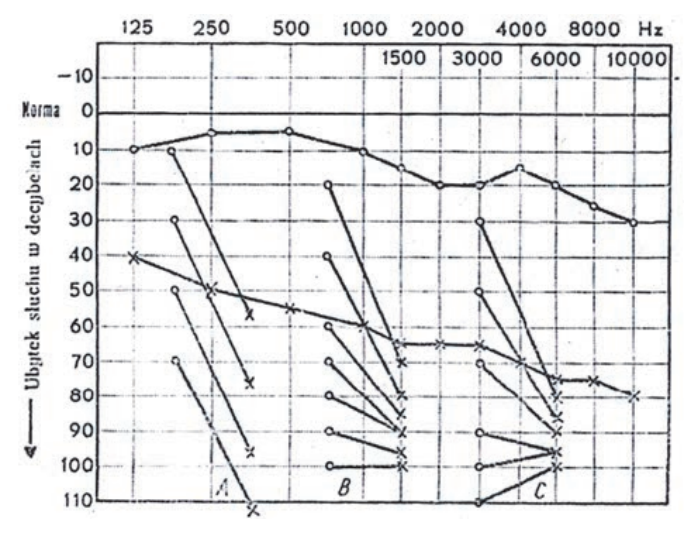
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
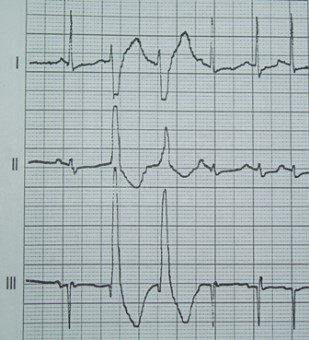
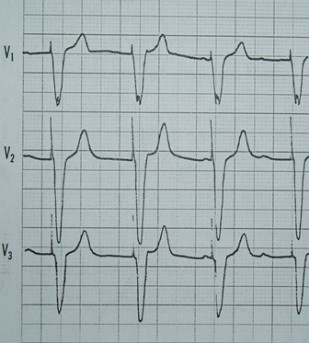
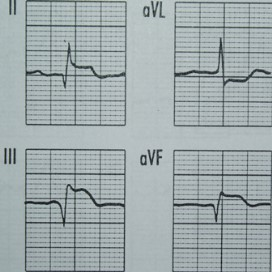
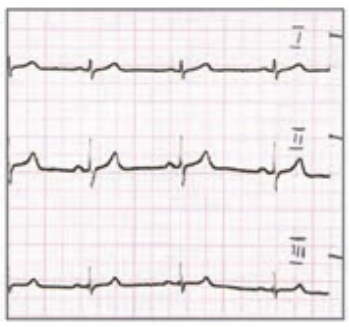
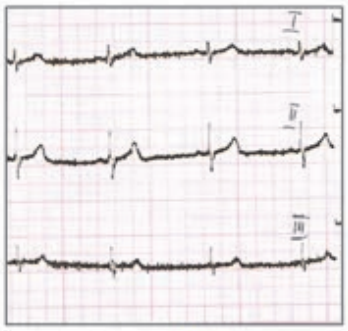
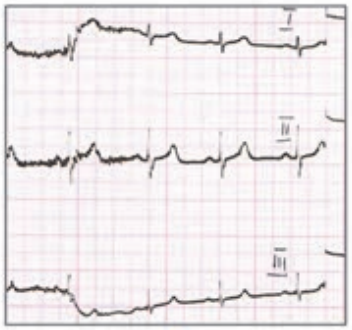
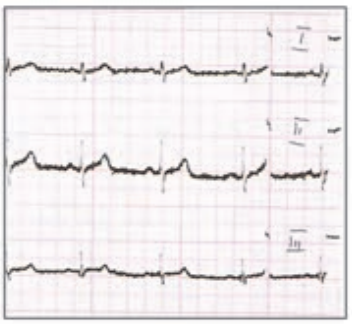
Na którym z zapisów EKG została uwidoczniona fala Pardee'go?
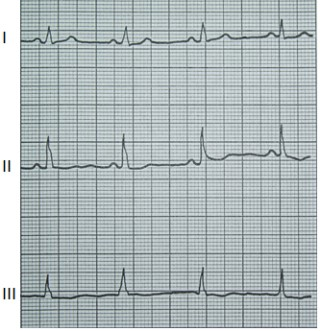
W zapisie EKG załamek U występuje bezpośrednio po załamku
Do planowego badania TK klatki piersiowej z użyciem środka cieniującego pacjent powinien zgłosić się
Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
W badaniu EKG elektrodę przedsercową V4 należy umocować
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
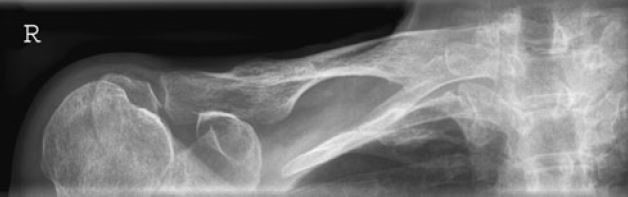
W jakiej projekcji i pod jakim kątem padania promienia centralnego został wykonany radiogram obojczyka?
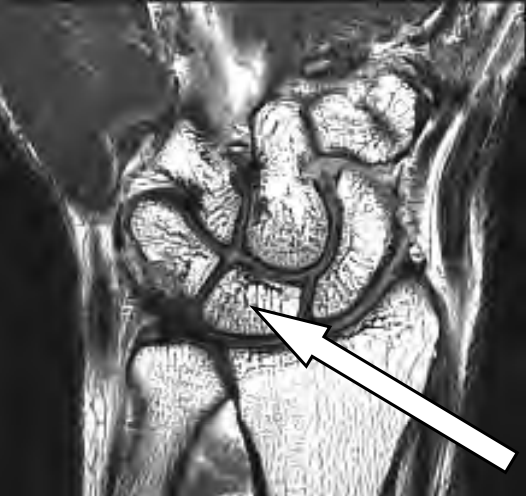
Na obrazie RM nadgarstka lewego strzałką oznaczono kość
Rytm alfa i beta rejestruje się podczas badania
Do badania MR nadgarstka pacjenta należy ułożyć
Promieniowanie rentgenowskie powstaje w wyniku hamowania
Badanie polegające na wprowadzeniu cewnika przez pęcherz moczowy do moczowodu i miedniczki nerkowej i podaniu środka kontrastującego to
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
W radiologii stomatologicznej ząb o numerze 23 to kieł
Która sekwencja w obrazowaniu MR jest stosowana do uwidocznienia naczyń krwionośnych?
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Audiogram przedstawia próbę
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
Który elektrokardiogram jest poprawny technicznie?
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
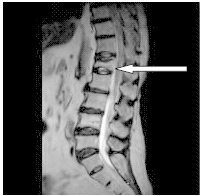
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
W badaniu PET CT wykorzystuje się radioizotopy emitujące promieniowanie