Pytanie 1
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
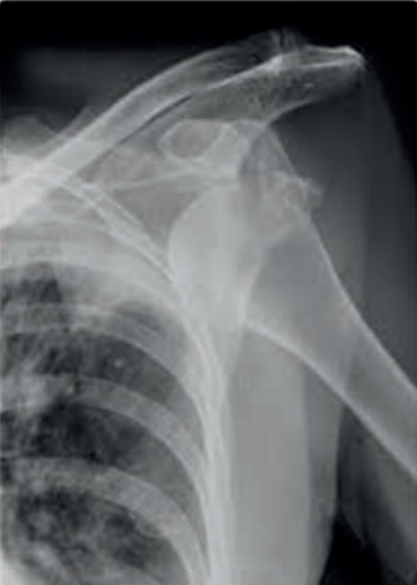
Wynik: 40/40 punktów (100,0%)
Wymagane minimum: 20 punktów (50%)
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?

Jakie źródła promieniowania stosowane są w brachyterapii?
Glukoza podawana pacjentowi w badaniu PET jest znakowana radioaktywnym
W celu maksymalnego ograniczenia dawki promieniowania badanie rentgenowskie u dzieci należy wykonać
W badaniu EKG elektrodę przedsercową V4 należy umocować
Które ciało obce w obszarze badania nie stanowi przeciwwskazania do wykonania MR?
Którą strukturę anatomiczną oznaczono strzałką na obrazie rezonansu magnetycznego?
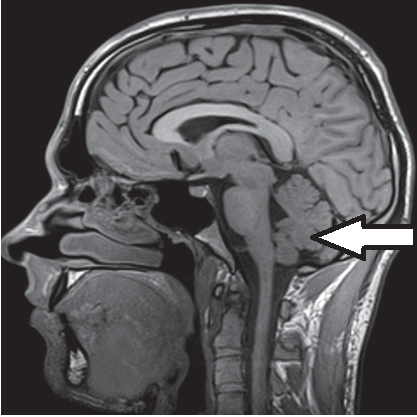
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
Bezwzględnym przeciwwskazaniem do badania spirometrycznego jest
Na radiogramie strzałką oznaczono
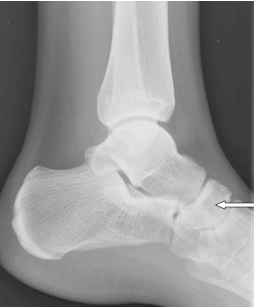
Którą tętnicę zaznaczono strzałką na obrazie MR?
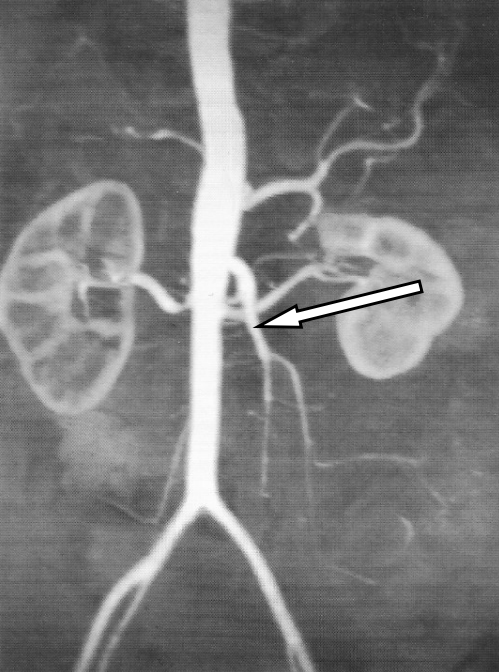
W systemie międzynarodowym ząb pierwszy przedtrzonowy po stronie lewej oznacza się symbolem
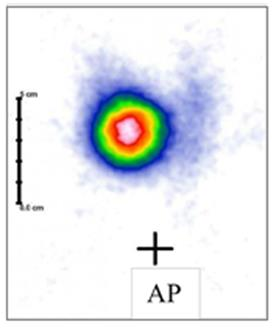
Na scyntygramie tarczycy uwidoczniono guzek
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Warstwa półchłonna (WP) jest wyrażona w mm Cu dla
Zamieszczony elektrokardiogram przedstawia
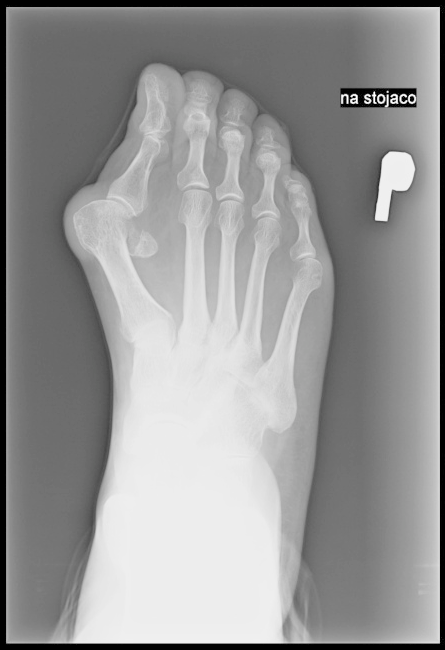
Na radiogramie uwidoczniono
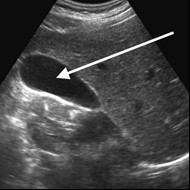
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
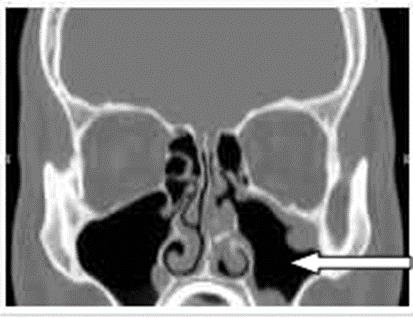
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W badaniu EEG elektrody referencyjne przymocowane do płatka ucha to
W badaniu EKG elektrodę przedsercową V4 należy umocować
Promieniowanie jonizujące pośrednio to
W standardowym badaniu elektrokardiograficznym elektrodę C4 należy umieścić
W sekwencji echa spinowego obraz T2-zależny uzyskuje się przy czasie repetycji TR
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
W obrazowaniu MR do uwidocznienia naczyń krwionośnych jest stosowana sekwencja
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
W pozytonowej emisyjnej tomografii komputerowej PET radioznacznik podawany jest pacjentowi najczęściej
Badanie metodą Dopplera umożliwia
Znak umieszczony w pracowni rezonansu magnetycznego zakazuje wstępu osobom

Folia wzmacniająca umieszczona w kasecie rentgenowskiej emituje pod wpływem promieniowania X światło
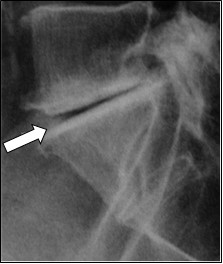
Na rentgenogramie strzałką zaznaczono
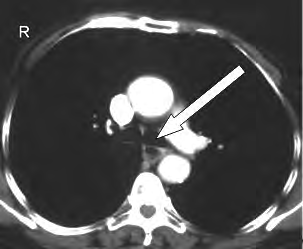
Na obrazie TK klatki piersiowej w przekroju poprzecznym strzałką oznaczono
W radiografii mianem SID określa się
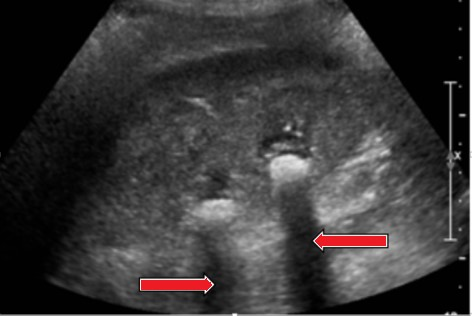
Który artefakt wskazano strzałkami na obrazie USG nerki?
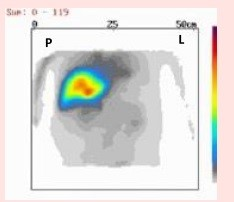
Który narząd został uwidoczniony na przedstawionym obrazie scyntygraficznym?
W obrazowaniu MR wykorzystuje się moment magnetyczny
Źródłem promieniowania protonowego stosowanego w radioterapii jest