Pytanie 1
Jak definiuje się próbkę wzorcową?
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Jak definiuje się próbkę wzorcową?
Odważka analityczna przygotowana w fabryce zawiera 0,1 mola EDTA. Posiadając taką jedną odważkę analityczną, jakie roztwory można przygotować?
Odczynnik chemiczny, w którym zawartość domieszek wynosi od 1 do 10%, jest nazywany odczynnikiem
Na podstawie zamieszczonych w tabeli opisów metod rozdzielania mieszanin, dobierz odpowiadające im nazwy.
| Tabela. Metody rozdzielania mieszanin | |
|---|---|
| Lp. | Opis metody |
| I. | Zlewanie cieczy znad osadu. |
| II. | Przeprowadzenie ciekłego rozpuszczalnika w stan pary. |
| III. | Wyodrębnianie z mieszaniny ciał stałych lub cieczy składnika przy pomocy rozpuszczalnika tak dobranego, aby rozpuszczał żądany związek chemiczny. |
| IV. | Powolne opadanie cząstek substancji stałej w cieczy pod wpływem własnego ciężaru. |
Jak przebiega procedura unieszkodliwiania rozlanego kwasu siarkowego(VI)?
Aby uzyskać roztwór 25 gramów CuSO4 w 50 gramach wody, konieczne jest podgrzanie mieszanki do temperatury w przybliżeniu
W laboratorium chemicznym przewody instalacji rurowych są oznaczane różnymi kolorami, zgodnie z obowiązującymi normami. Polska Norma PN-70 N-01270/30 określa kolor dla wody jako
Na diagramie przedstawiającym proces pobierania prób środowiskowych do analizy literą Y oznaczono próbkę
Zgodnie z instrukcją dotyczącą pobierania próbek nawozów (na podstawie normy PN-EN 12579:2001), liczbę punktów pobierania próbek pierwotnych ustala się według wzoru nsp = 0,5·√V, gdzie V oznacza objętość jednostki badanej w m3. Wartość nsp zaokrągla się do liczby całkowitej, a dodatkowo nie może być mniejsza niż 12 ani większa niż 30.
Dlatego dla objętości V = 4900 m3, nsp wynosi
Na rysunku przedstawiono palnik gazowy
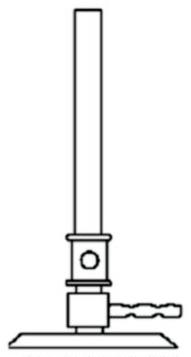
Aby otrzymać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy
Z uwagi na bezpieczeństwo pracy, ciecze żrące powinny być podgrzewane w łaźniach
Najskuteczniejszą techniką separacji ketonu oraz kwasu karboksylowego obecnych w roztworze benzenowym jest
Proces oddzielania składników jednorodnej mieszaniny, polegający na eliminacji jednego lub większej ilości składników z roztworu lub substancji stałej przy użyciu odpowiednio wybranego rozpuszczalnika, to
Które z wymienionych reakcji chemicznych stanowi reakcję redoks?
W celu przygotowania roztworu mianowanego należy użyć sprzętu przedstawionego na rysunku
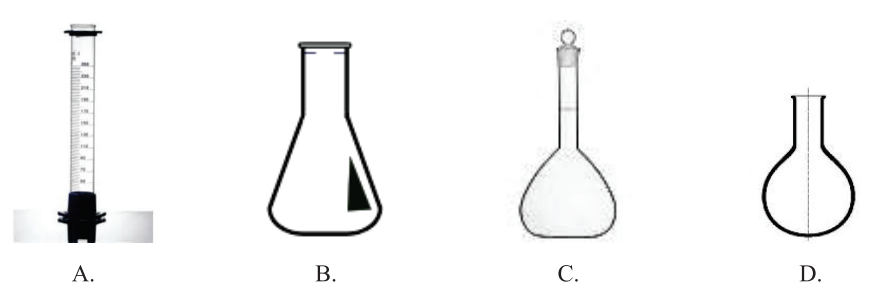
Aby uzyskać roztwór CuSO4 o stężeniu 15%, w jakim stosunku należy połączyć roztwory 10% oraz 20%?
Ile wynosi objętość roztworu o stężeniu 0,5 mol/dm3, jeśli przygotowano go z 0,1 mola KOH?
W laboratorium chemicznym systemy wodne zazwyczaj oznacza się kolorem zielonym
Podstawowy zestaw do filtracji, oprócz statywu i sączka, obejmuje
Aby uzyskać roztwór AgNO3 (masa molowa AgNO3 to 169,8 g/mol) o stężeniu 0,1 mol/dm3, należy rozpuścić w wodzie destylowanej i dopełnić kolbę wodą destylowaną do zaznaczonej kreski.
Jaką masę NaCl uzyskuje się poprzez odparowanie do sucha 250 g roztworu 10%?
Na rysunku przedstawiono zestaw do oczyszczania jodu w procesie
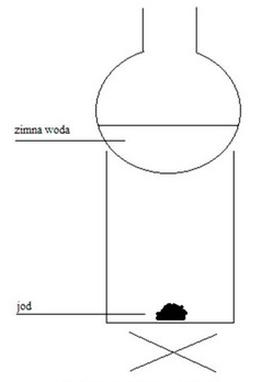
Oblicz masę wapienia, który został rozłożony, jeśli w trakcie reakcji uzyskano 44,8 dm3 CO2 (w warunkach standardowych).
MC = 12 g/mol, MCa = 40 g/mol, MO = 16 g/mol
Jaką objętość zasady sodowej o stężeniu 1,0 mol/dm3 należy dodać do 56,8 g kwasu stearynowego, aby otrzymać mydło sodowe (stearynian sodu)?
| C17H35COOH + NaOH → C17H35COONa + H2O |
| (MC17H35COOH = 284 g/mol, MC17H35COONa = 306 g/mol, MNaOH = 40 g/mol, MH2O= 18 g/mol) |
Na podstawie danych w tabeli określ, dla oznaczania którego parametru zalecaną metodą jest chromatografia jonowa.
| Parametr | Metoda podstawowa |
|---|---|
| pH | metoda potencjometryczna, kalibracja przy zastosowaniu minimum dwóch wzorców o pH zależnym od wartości oczekiwanych w próbkach wody |
| azotany(V) | chromatografia jonowa |
| fosforany(V) | spektrofotometria |
| Na, K, Ca, Mg | AAS (spektrometria absorpcji atomowej) |
| zasadowość | miareczkowanie wobec fenoloftaleiny oraz oranżu metylowego |
| tlen rozpuszczony, BZT₅ | metoda potencjometryczna |
Jakie urządzenie jest wykorzystywane do oczyszczania próbki gazowej?
Czułość bezwzględna wagi definiuje się jako
Podczas przygotowywania roztworu mianowanego kwasu solnego o określonym stężeniu należy:
Na rysunku przedstawiono
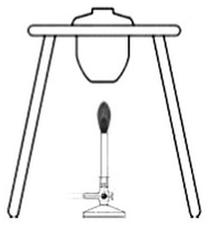
Aby uzyskać sole sodowe fenoli, należy stopić dany fenol z sodą (M = 106 g/mol), stosując 10% nadmiar w porównaniu do ilości stechiometrycznej, według równania:
2 ArOH + Na2CO3 → 2 ArONa + H2O + CO2 Ile sody jest wymagane do reakcji z 7,2 g 2-naftolu (M = 144 g/mol)?
Piktogramem przedstawionym na rysunku znakuje się opakowanie substancji

Do systemu odprowadzania ścieków, w formie rozcieńczonego roztworu wodnego o maksymalnej masie 100 g na raz, można wprowadzić
Wybierz spośród wymienionych właściwości tę, która nie dotyczy naczyń kwarcowych.
Do przechowywania zamrożonych próbek wody stosuje się naczynia wykonane
Technika oddzielania płynnych mieszanin, w której wykorzystuje się różnice w prędkości migracji składników przez odpowiednią bibułę, nazywa się
Gdzie należy przechowywać cyjanek potasu KCN?
Temperatura topnienia mocznika wynosi 133 °C. W celu określenia czystości preparatów tej substancji, przeprowadzono badania temperatury ich topnienia, uzyskując wyniki przedstawione w tabeli. Wskaż preparat o najmniejszym stopniu czystości.
| Preparat | A | B | C | D |
|---|---|---|---|---|
| Zakres temperatury topnienia [°C] | 132-133 | 130-133 | 125-133 | 128-133 |
W wypadku oblania skóry kwasem mrówkowym należy
| Wyciąg z karty charakterystyki Skład: kwas mrówkowy 80%, woda 11-20% Pierwsza pomoc. Po narażeniu przez drogi oddechowe. Natychmiast wezwać lekarza. Po kontakcie ze skórą. Zanieczyszczoną skórę natychmiast przemyć dużą ilością wody. |
W trakcie określania miana roztworu NaOH, do zmiareczkowania 25,0 cm3 tego roztworu, użyto 30,0 cm3 roztworu HCl o stężeniu 0,1000 mol/dm3. Jakie miało miano zasady?