Pytanie 1
Kiedy w procesie terapii wykonuje się badanie CBCT (cone beam computed tomography)?
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
Kiedy w procesie terapii wykonuje się badanie CBCT (cone beam computed tomography)?
Do zadań technika elektroradiologa w pracowni hemodynamicznej należy
Jaki jest cel stosowania bolusa w radioterapii?
Kto jest odpowiedzialny za wykonywanie testów podstawowych kontroli jakości gammakamery w Zakładzie Medycyny Nuklearnej?
Który radioizotop stosuje się do badania scyntygraficznego kości?
Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
Zwiększenie napięcia na lampie rentgenowskiej powoduje
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Przyczyną zaniku kostnego jest
Odprowadzenie EKG mierzące różnicę potencjałów między lewym podudziem a prawym przedramieniem oznacza się jako
Przy ułożeniu do zdjęcia kręgów szyjnych CIII-CVII w projekcji przednio-tylnej lampa może być odchylona o kąt
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
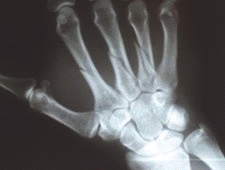
Na radiogramie uwidoczniono złamanie
Do wczesnych odczynów popromiennych po radioterapii zalicza się
W leczeniu izotopowym tarczycy podaje się
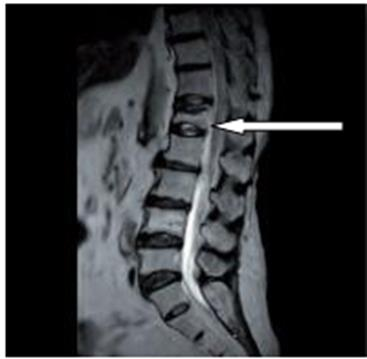
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
W celu wykonania badania scyntygraficznego układu kostnego radiofarmaceutyk należy podać pacjentowi
W zapisie EKG załamek U występuje bezpośrednio po załamku
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Co określa M₀ w systemie klasyfikacji nowotworów TNM?
Która przyczyna spowodowała powstanie artefaktu widocznego na zamieszczonym obrazie MR?
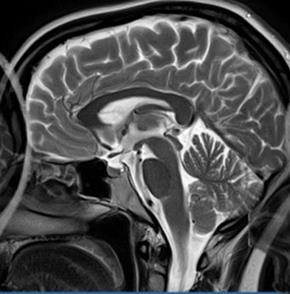
Na obrazie uwidoczniono
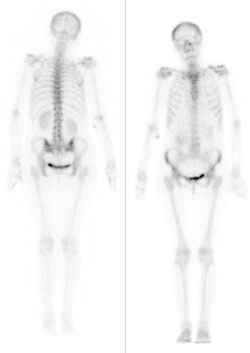
Zamieszczony rentgenogram został zarejestrowany podczas wykonania
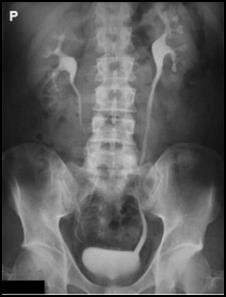
Technikę bramkowania oddechowego stosuje się w badaniu MR
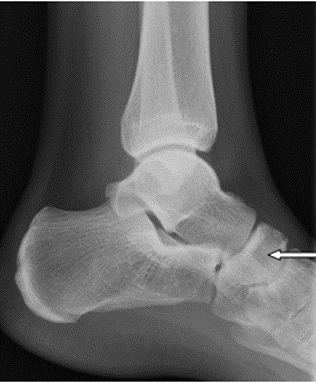
Na radiogramie stopy strzałką wskazano kość
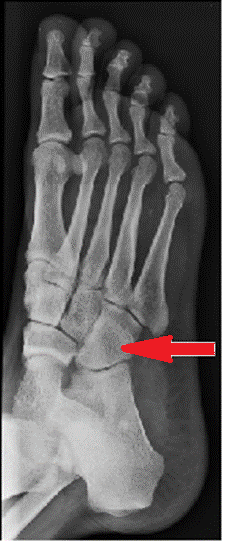
W radiografii mianem SID określa się
Wskazaniem do wykonania scyntygrafii perfuzyjnej jest
Jakie symbole mają odprowadzenia kończynowe dwubiegunowe w badaniu EKG?
Na rentgenogramie strzałką zaznaczono
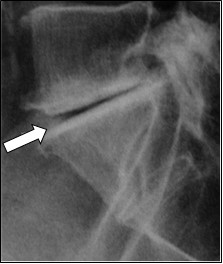
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Które odprowadzenie w badaniu EKG rejestruje różnice potencjałów pomiędzy lewym a prawym przedramieniem?
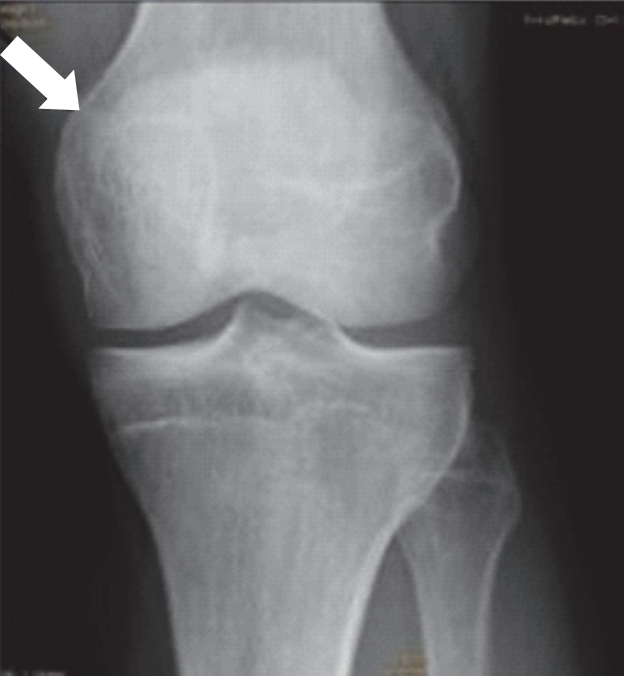
Którą strukturę anatomiczną zaznaczono na radiogramie stawu kolanowego?
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
W jakich jednostkach mierzy się natężenie dźwięku?
W radiologii stomatologicznej ząb o numerze 23 to kieł
Na zamieszczonym radiogramie strzałką oznaczono kość
Jak zgodnie ze standardem należy ustawić pacjenta do badania rentgenowskiego w skosie tylnym prawym?
Miejscem wykonania pomiaru densytometrycznego z kości przedramienia jest
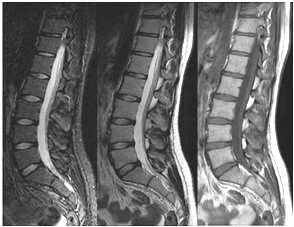
Które kolejne sekwencje badania kręgosłupa lędźwiowego uwidoczniono na przedstawionych obrazach?