Pytanie 1
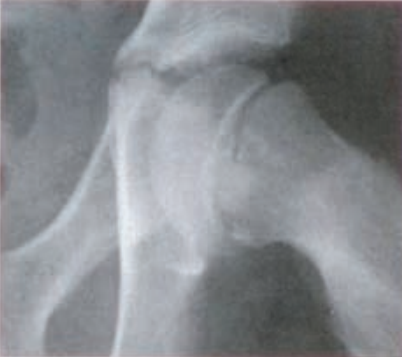
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu
Wynik: 25/40 punktów (62,5%)
Wymagane minimum: 20 punktów (50%)
Na rentgenogramie przedstawione jest złamanie Saltera-Harrisa typu

Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
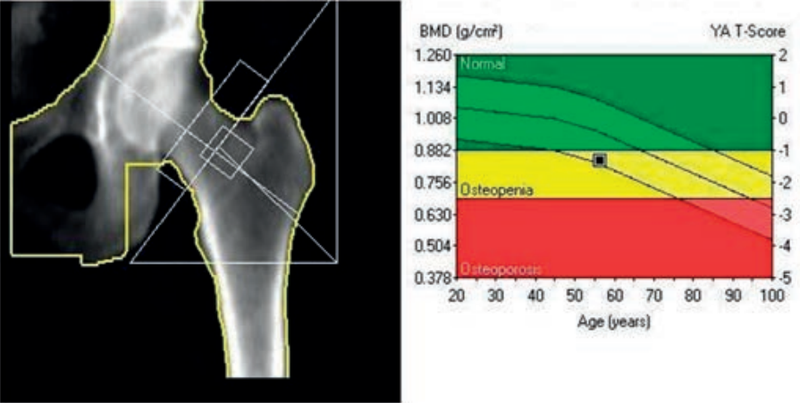
Zamieszczone obrazy związane są z badaniem
Jaki jest cel stosowania bolusa w radioterapii?
Podczas badania EEG otwarcie oczu powoduje
W której projekcji należy wykonać badanie radiologiczne kręgosłupa lędźwiowego, by na otrzymanym zdjęciu wyrostki kręgów lędźwiowych układały się w charakterystyczny kształt piesków (teriera szkockiego)?
Limfografia to badanie kontrastowe
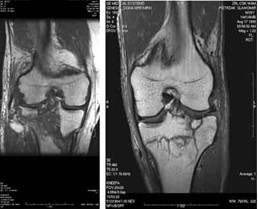
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
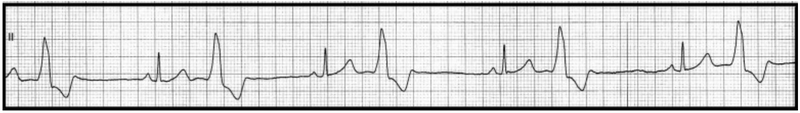
Przedstawiony zapis elektrokardiograficzny może wskazywać na
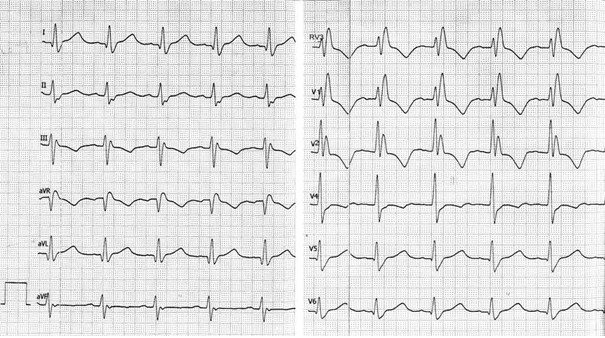
Który stan patologiczny został zarejestrowany podczas wykonywania badania EKG?
Wskazaniem do wykonania badania spirometrycznego jest
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
Jaka jest moc dawki pochłoniętej w brachyterapii HDR?
W jakich jednostkach mierzy się natężenie dźwięku?
W diagnostyce mammograficznej punktowy ucisk sutka stosuje się w projekcji
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
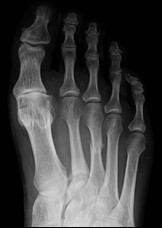
Na radiogramie stopy uwidocznione jest złamanie trzonu
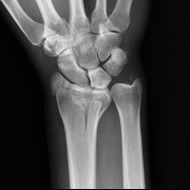
Na obrazie radiologicznym nadgarstka uwidoczniono złamanie nasady
Pielografia to badanie układu
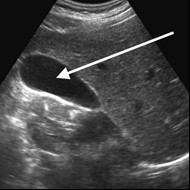
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
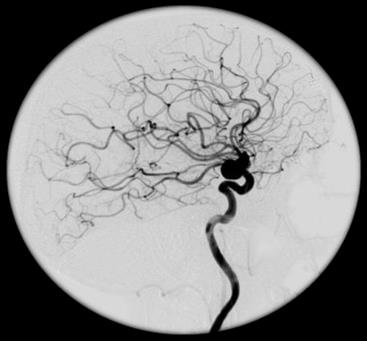
W przedstawionym na ilustracji obrazie badania angiograficznego uwidoczniono
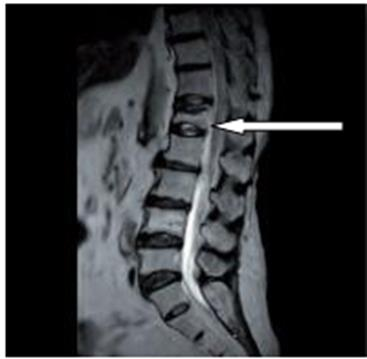
Na obrazie rezonansu magnetycznego strzałką wskazano patologiczny kręg
Na ilustracji przedstawiono pozycjonowanie pacjentki do badania mammograficznego w projekcji
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Elementem systemu rejestracji obrazu, w którym fotony promieniowania X są bezpośrednio konwertowane na sygnał elektryczny, jest
Do podstawowych projekcji stosowanych w diagnostyce mammograficznej należą
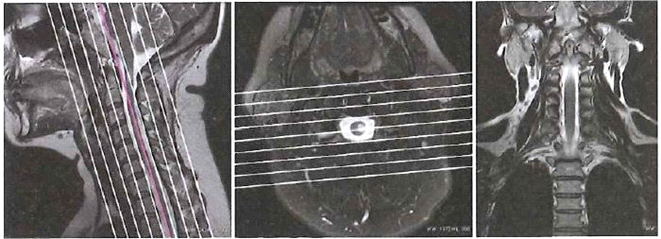
Obrazy MR kręgosłupa szyjnego przedstawiają etap planowania badania warstw
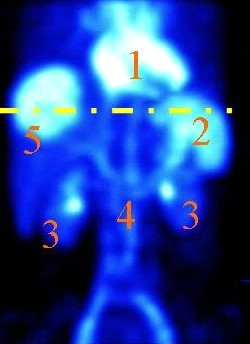
Który narząd na obrazie scyntygrafii znakowanej erytrocytami zaznaczono cyfrą 2?
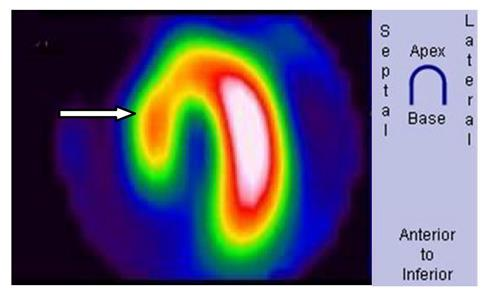
Na obrazie scyntygrafii perfuzyjnej serca strzałką wskazano ścianę
Celem radioterapii paliatywnej nie jest
W zapisie EKG linia izoelektryczna obrazuje
W jaki sposób należy oprzeć stroik w audiometrycznym badaniu przewodnictwa kostnego?
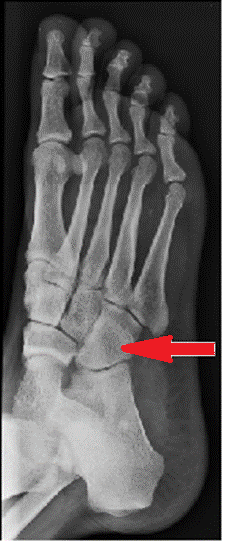
Na radiogramie stopy strzałką wskazano kość
W pozytonowej tomografii emisyjnej PET zostaje zarejestrowane promieniowanie powstające podczas
Jaki rozmiar kasety należy zastosować, wykonując standardowe zdjęcie stawu kolanowego w projekcji bocznej?