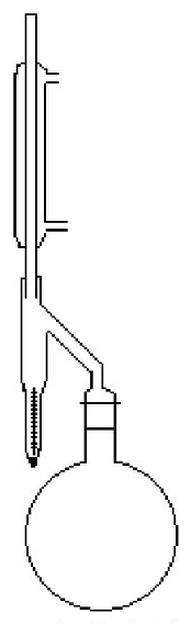
Pytanie 1
Na rysunku przedstawiono aparat służący do badania zawartości wody w surowcach metodą
Wynik: 29/40 punktów (72,5%)
Wymagane minimum: 20 punktów (50%)
Na rysunku przedstawiono aparat służący do badania zawartości wody w surowcach metodą

Ebuliometr to przyrząd używany do pomiaru temperatury
Do zmiareczkowania próbki roztworu NaOH wykorzystano 10 cm3 roztworu HCl o stężeniu 0,1 mol/dm3. Ile NaOH (M = 40 g/mol) znajdowało się w próbce?
W celu wykrywania fluorowców w cząsteczkach związków organicznych stosuje się reakcje z wodą chlorową w towarzystwie chloroformu.
Cl2 + 2 I- → I2 + 2 Cl-Na podstawie podanych reakcji można stwierdzić, że w pierwszej kolejności woda chlorowa
I2 + 5 Cl2 + 6 H2O → 2 IO3- + 10 Cl- + 12 H+
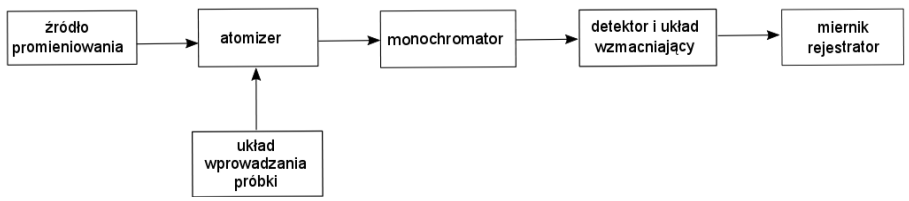
Na rysunku przedstawiono schemat blokowy
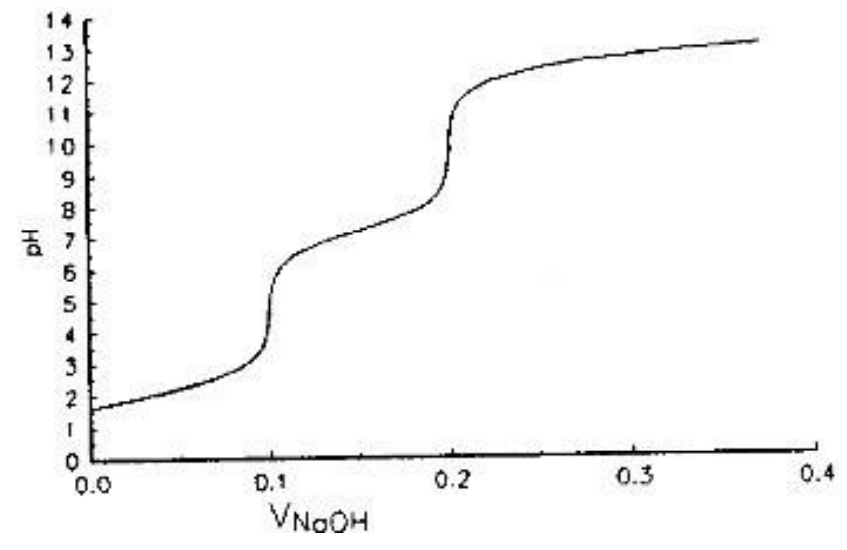
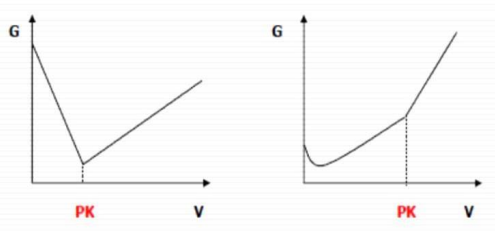
Wykresy przedstawiają przebieg krzywych miareczkowania
Na ilustracji przedstawiono

Związki lotne, które występują w wielu roślinach i mogą być wydobywane, np. poprzez destylację z parą wodną lub dzięki ciągłej ekstrakcji w aparacie Soxhleta, to
Elektroforeza to technika wykorzystywana głównie do segregacji mieszaniny
Jeżeli przewodnictwo właściwe wody destylowanej mieści się w granicach 0,1•10-4 do 1•10-4 mS/cm, to do pomiarów należy zastosować czujnik konduktometryczny o wartości stałej naczynka K równej

Na podstawie informacji zamieszczonych w tabeli wskaż wzór związku, który wytrąci się w postaci osadu.
| Badany kation | Odczynnik grupowy | NaOH | Barwienie płomienia |
|---|---|---|---|
| Mg2+ | brak | biały osad | |
| K+ | brak | fiołkowy | |
| Na+ | brak | żółty |
Wskaź kationy, które są możliwe do wykrycia poprzez próbę płomieniową?
Na rysunku przedstawiono aparat

Zjawisko polegające na przepuszczaniu rozpuszczalnika przez membranę półprzepuszczalną z roztworu o wyższym stężeniu do roztworu o niższym stężeniu substancji rozpuszczonej określa się mianem
Aby określić całkowitą zawartość żelaza w próbce wody, konieczne jest zredukowanie żelaza(III) do żelaza(II), a następnie wykorzystanie metody analitycznej, która nazywa się
Czym jest wskaźnik metalochromowy?
Na zmiareczkowanie odważki KOH zużyto 30,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3. Ile gramów KOH zawierała odważka?
| MKOH = 56 g/mol |
Aby zidentyfikować substancje poprzez pomiar wartości współczynników załamania światła, wykorzystuje się
Punkt ekwiwalentny miareczkowania to moment, w którym analizowany składnik całkowicie zareagował
To pytanie jest dostępne tylko dla uczniów i nauczycieli. Zaloguj się lub utwórz konto aby zobaczyć pełną treść pytania.
Odpowiedzi dostępne po zalogowaniu.
Wyjaśnienie dostępne po zalogowaniu.
Jakie urządzenie wykorzystuje się do pomiaru zasolenia wody?
Pomiar intensywności światła rozproszonego Ir po przejściu przez roztwór koloidalny wykonuje się z zastosowaniem
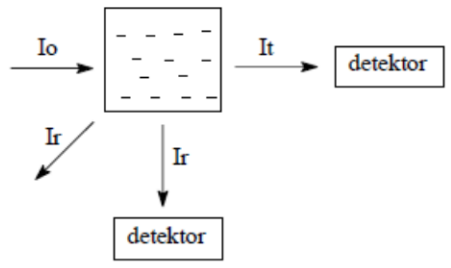
Jaką funkcję pełni batometr?
W laboratorium mikrobiologicznym do przeprowadzania jałowienia na zimno wykorzystuje się
Metoda obrączkowa jest wykorzystywana do rozpoznawania jonu
Oznaczono LZ i LJ dla czterech różnych próbek tłuszczów. Wyniki zestawiono w tabeli:
Na podstawie zamieszczonych danych o liczbach właściwych wybranych tłuszczów wskaż próbkę, którą stanowi olej rzepakowy.
| Liczby właściwe wybranych tłuszczów | ||
|---|---|---|
| Rodzaj tłuszczu | Liczba zmydlania (LZ) mg KOH / g tłuszczu | Liczba jodowa (LJ) g I₂ / 100 g tłuszczu |
| Olej lniany | 187 – 197 | 169 – 192 |
| Olej sojowy | 188 – 195 | 114 – 138 |
| Olej rzepakowy | 167 – 179 | 94 – 106 |
| Tran wielorybi | 170 – 202 | 102 – 144 |
| Masło krowie | 218 – 245 | 25 – 38 |
| Smalec wieprzowy | 193 – 200 | 46 – 66 |
| Próbka | Liczba zmydlania (LZ) | Liczba jodowa (LJ) |
|---|---|---|
| 1 | 190 | 140 |
| 2 | 171 | 99 |
| 3 | 194 | 105 |
| 4 | 195 | 60 |
Na podstawie zamieszczonych w tabeli informacji wskaż związek chemiczny, którego należy użyć w celu oddzielenia kationu Pb2+ z mieszaniny kationów grupy pierwszej.
| Pb2+ | Hg22+ | Ag+ |
| + rozc. HCl | ||
| PbCl2↓ | Hg2Cl2↓ | AgCl↓ |
| Dodać kilka kropli H2O, ogrzać na łaźni, odsączyć na gorąco | ||
| Pb2+ | Hg2Cl2↓ | AgCl↓ |
| + K2CrO4 | + NH3 aq | +stęż. NH3 aq |
Opisana metoda miareczkowania zaliczana jest do
| Ilościowe oznaczenie cukrów polega na redukcji soli miedzi(II) roztworem cukru, a następnie dodaniu do próbki roztworu KI i odmiareczkowaniu wydzielonego jodu mianowanym roztworem tiosiarczanu sodu |
Na schemacie przedstawiono
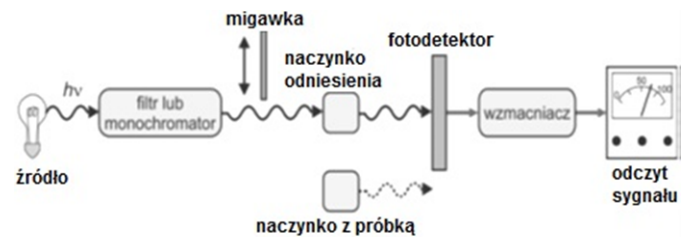
Na rysunku przedstawione jest pole widzenia
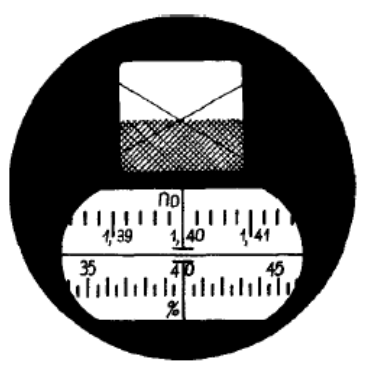
Na podstawie zamieszczonego schematu ilustrującego przeprowadzone badania wskaż, jaką barwę przyjmie roztwór w probówce oznaczonej numerem 2.
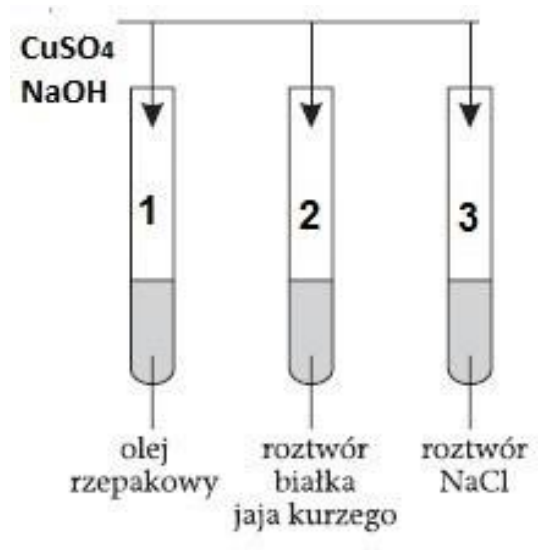
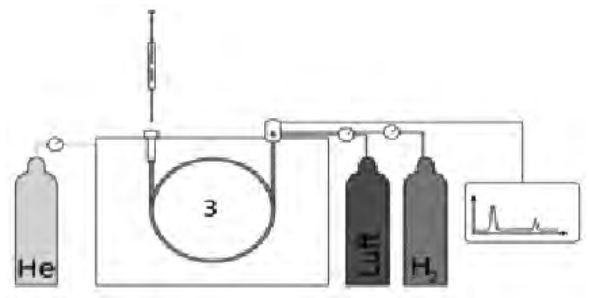
Na rysunku przedstawiającym schemat chromatografu gazowego numerem 3 oznaczono
Jaką metodę można wykorzystać do oznaczania białek w produktach żywnościowych?
Próbkę żywności poddano ogrzewaniu w suszarce laboratoryjnej, a następnie obliczono X według wzoru. Wartość liczbowa X określa
$$ X = \frac{b - c}{a - c} \times 100\% $$gdzie:
\( a \) – masa naczyńka z badaną próbką przed ogrzewaniem [g]
\( b \) – masa naczyńka z badaną próbką po ogrzewaniu [g]
\( c \) – masa pustego naczyńka [g]
W celu identyfikacji cukru sporządzono jego roztwór i przelano do trzech probówek. Następnie przeprowadzono doświadczenia, których wyniki zapisano w tabeli:
Badanym cukrem była
| Badany roztwór | Dodany odczynnik | Obserwacje |
|---|---|---|
| Probówka 1. | Cu(OH)2 | Zawiesina Cu(OH)2 rozpuściła się, a roztwór przyjął szafirową barwę |
| Cu(OH)2 | Po ogrzaniu probówki pojawił się ceglasto-czerwony osad | |
| Probówka 2. | [Ag(NH3)2]+ | Po ogrzaniu na ściankach probówki pojawiło się srebro metaliczne |
| Probówka 3. | Br2(aq) + roztwór NaHCO3 | Woda bromowa uległa odbarwieniu |
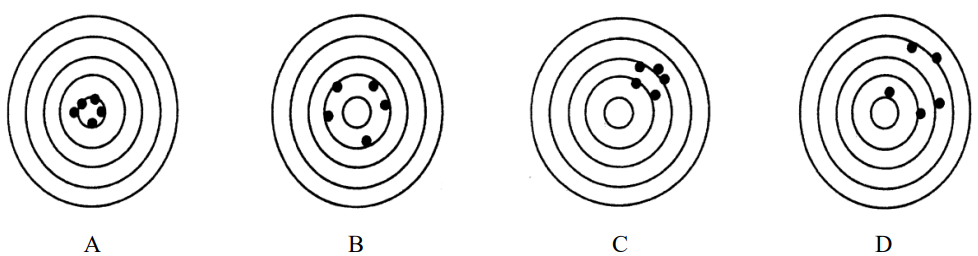
Na rysunkach przedstawiono serie pomiarów o różnej dokładności i precyzji (środek najmniejszego okręgu oznacza wartość prawdziwą). Serię pomiarów precyzyjnych, ale niedokładnych przedstawiono na rysunku
Rozpraszanie promieniowania świetlnego przez cząstki koloidalne, które mają wymiary mniejsze od długości fali światła, to zjawisko
Rysunek przedstawia
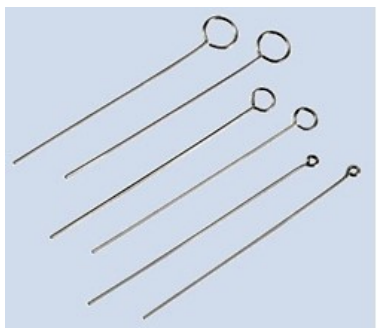
Jakie urządzenie wykorzystuje się do hodowli bakterii w warunkach beztlenowych?
Przedstawiona na rysunku krzywa miareczkowania jest charakterystyczna dla