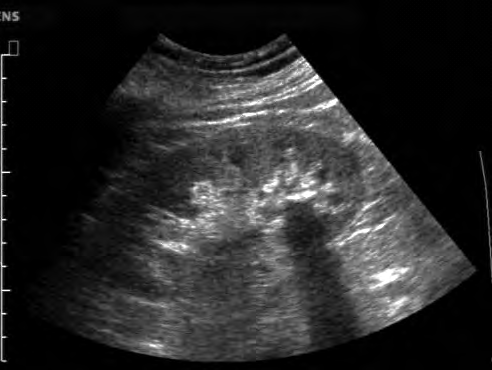
Pytanie 1
Na radiogramie uwidoczniono
Wynik: 23/40 punktów (57,5%)
Wymagane minimum: 20 punktów (50%)
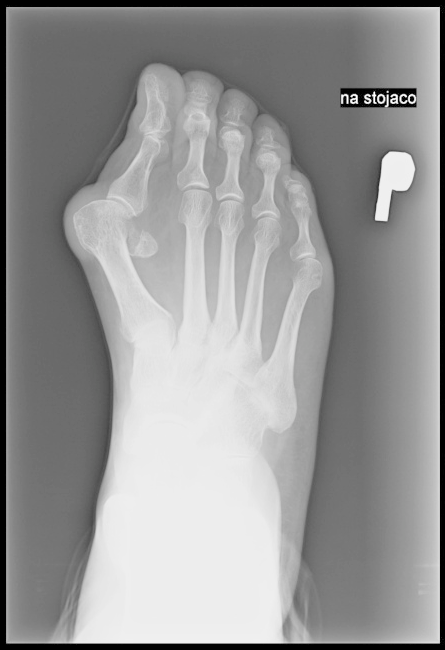
Na radiogramie uwidoczniono

Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje
Którym skrótem oznacza się tomografię komputerową wysokiej rozdzielczości?
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Zwiększenie napięcia na lampie rentgenowskiej powoduje
W pracowni ultrasonograficznej technik elektroradiolog nie korzysta z przepisów dotyczących
Którą tętnicę zaznaczono strzałką na obrazie MR?
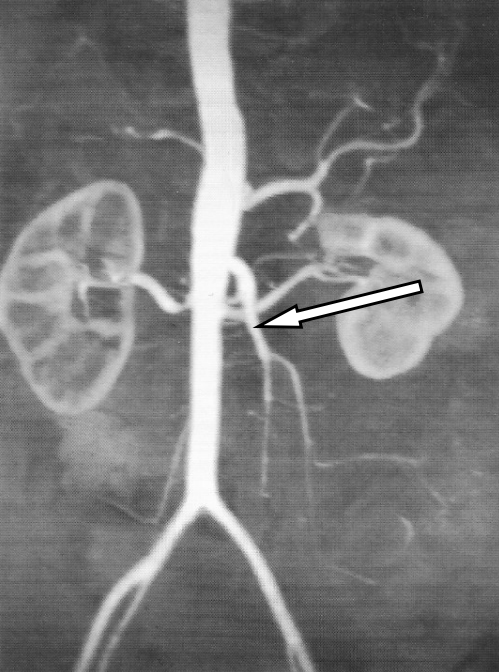
W diagnostyce metodą rezonansu magnetycznego biorą udział
W których projekcjach podstawowych wykonuje się standardowe badanie mammograficzne?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Które zdjęcia należy wykonać pacjentom z chorobą reumatoidalną stawów kolanowych?
Który typ głowicy ultrasonograficznej przedstawiono na ilustracji?

Do zdjęcia lewobocznego kręgosłupa lędźwiowo-krzyżowego pacjenta należy ułożyć na boku
Którą ochronę radiologiczną należy zastosować podczas wykonywania zdjęcia rentgenowskiego przeglądowego klatki piersiowej u pacjentki w okresie rozrodczym?
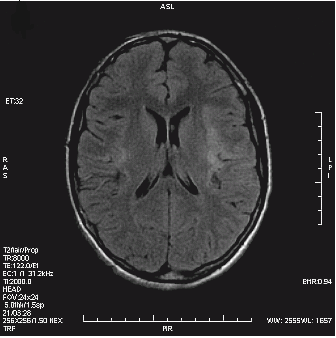
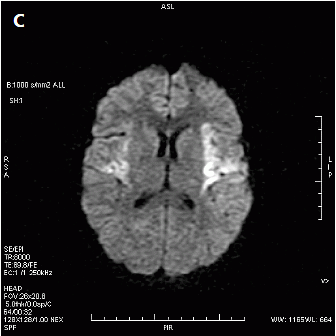
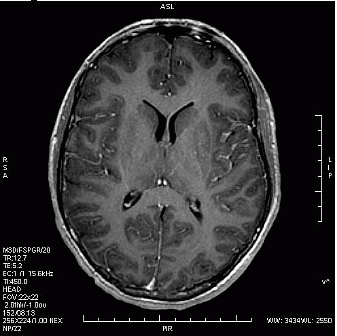
Który obraz MR mózgu został wykonany w sekwencji DWI?
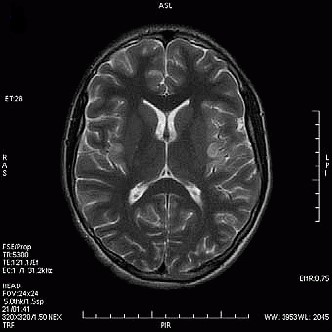
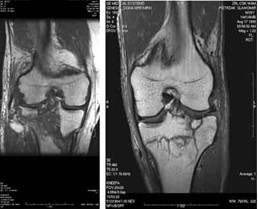
Którą metodą i w której płaszczyźnie zostało wykonane badanie stawu kolanowego zobrazowane na zdjęciach?
Na obrazie MR jamy brzusznej strzałką wskazano
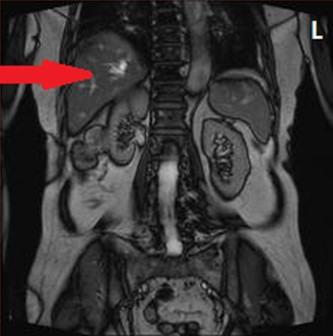
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
Na rentgenogramie strzałką zaznaczono
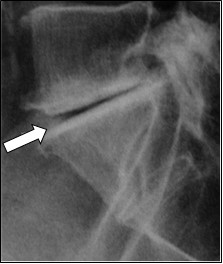
Pielografia to badanie układu
Na radiogramie uwidoczniono
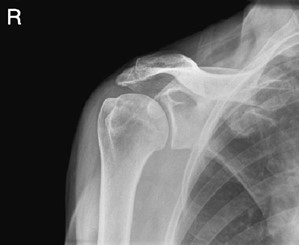
Do zdjęcia rentgenowskiego kręgosłupa piersiowego w projekcji AP pacjenta należy ułożyć
W jaki sposób należy ustawić promień centralny w stosunku do ramienia i przedramienia, by wykonać zdjęcie rentgenograficzne stawu łokciowego u pacjenta z przykurczem?
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
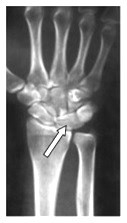
W sekwencji echa spinowego obraz T2-zależny uzyskuje się przy czasie repetycji TR
Na radiogramie uwidoczniono złamanie
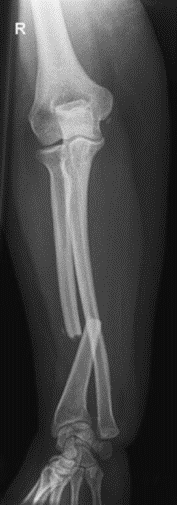
Które zdjęcie RTG stawu łokciowego zostało wykonane w projekcji skośnej w rotacji zewnętrznej?
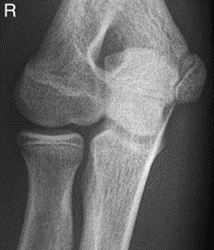
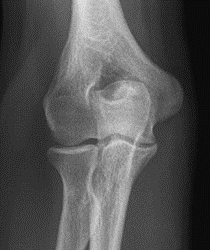
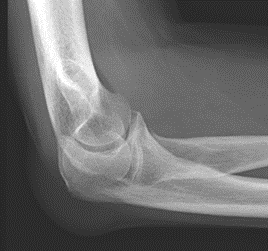
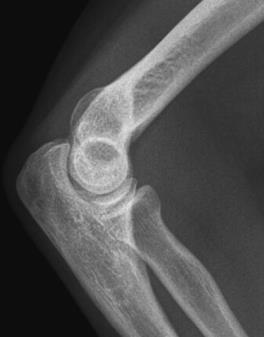
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
Co zostało uwidocznione na zamieszczonym radiogramie?
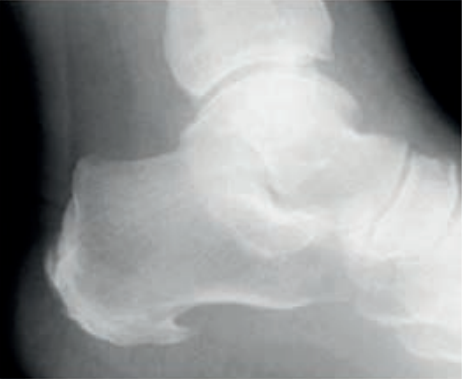
Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
W którym okresie ciąży wykonanie u kobiety zdjęcia rentgenowskiego klatki piersiowej jest najbardziej szkodliwe dla płodu?
Który środek kontrastujący stosuje się w badaniu metodą rezonansu magnetycznego?
Na obrazie ultrasonograficznym jamy brzusznej strzałką wskazano
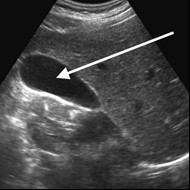
Cholangiografia to badanie radiologiczne
Kasety do pośredniej radiografii cyfrowej CR są wyposażone
Strzykawka automatyczna do podawania kontrastu jest stosowana przy wykonywaniu
Dobierz dla standardowego pacjenta projekcję, pozycję i sposób ułożenia kasety o wymiarach 30 cm x 40 cm do zdjęcia przeglądowego układu moczowego.
| Projekcja | Pozycja | Ułożenie kasety | |||
|---|---|---|---|---|---|
| 1. | AP | 3. | stojąca | 5. | poprzeczne |
| 2. | PA | 4. | leżąca | 6. | podłużne |
Głowica typu convex w USG służy do badania
Który parametr ekspozycji ma decydujący wpływ na kontrast obrazu rentgenowskiego?
Na obrazie ultrasonograficznym jamy brzusznej uwidoczniono