Pytanie 1
Jakie substancje wykorzystuje się do wykrywania obecności jonów chlorkowych w wodzie mineralnej?
Wynik: 28/40 punktów (70,0%)
Wymagane minimum: 20 punktów (50%)
Jakie substancje wykorzystuje się do wykrywania obecności jonów chlorkowych w wodzie mineralnej?
Zjawisko fizyczne, które polega na rozkładaniu struktury krystalicznej substancji stałej oraz przenikaniu jej cząsteczek lub jonów do cieczy, nosi nazwę
W laboratoriach roztwór potasu dichromianu(VI) w stężonym kwasie siarkowym(VI) wykorzystuje się do
Wskaż sprzęt, którego należy użyć, aby przygotować 100 cm3 roztworu NaOH o stężeniu 0,1 mol/dm3.
| 1 | 2 | 3 | 4 | 5 |
| naczynko wagowe | waga analityczna | kolba stożkowa | kolba miarowa pojemności 50 cm3 | kolba miarowa pojemności 100 cm3 |
W próbkach obecne są składniki, które znacznie różnią się pod względem zawartości. Składnik, którego procentowy udział w próbce jest niższy od 0,01%, nazywamy
Jaki jest błąd względny pomiaru na wadze o precyzji 0,1 g dla próbki o wadze 1 g?
Jakie jest stężenie roztworu HNO3, który powstał w wyniku połączenia 50 cm3 roztworu HNO3 o stężeniu 0,2 mol/dm3 oraz 25 cm3 roztworu HNO3 o stężeniu 0,5 mol/dm3?
Urządzeniem pomiarowym nie jest
W trakcie kalibracji stężenia roztworu kwasu solnego na przynajmniej przygotowany roztwór zasady sodowej ma miejsce reakcja
Podczas rozkładu chloranu(V) potasu powstają chlorek potasu oraz tlen. Ile gramów tlenu zostanie wydzielonych w trakcie rozkładu 24,5 g chloranu(V) potasu, jeśli jednocześnie uzyskano 14,9 g chlorku potasu? Masy molowe pierwiastków: K = 39 g/mol, Cl = 35,5 g/mol, O=16 g/mol?
Jaką objętość zasady sodowej o stężeniu 1,0 mol/dm3 należy dodać do 56,8 g kwasu stearynowego, aby otrzymać mydło sodowe (stearynian sodu)?
| C17H35COOH + NaOH → C17H35COONa + H2O |
| (MC17H35COOH = 284 g/mol, MC17H35COONa = 306 g/mol, MNaOH = 40 g/mol, MH2O= 18 g/mol) |
Roztwór zawierający 16,00 g siarczanu(VI) miedzi(II) nasycono siarkowodorem. Masa wytrąconego siarczku miedzi(II), po odsączeniu i wysuszeniu, wynosiła 8,64 g. Oblicz procentową wydajność tej reakcji.
Równanie reakcji:
\( \text{CuSO}_4 + \text{H}_2\text{S} \rightarrow \text{CuS} + \text{H}_2\text{SO}_4 \)
\( \text{M CuSO}_4 = 160 \, \text{g/mol} \)
\( \text{M CuS} = 96 \, \text{g/mol} \)
Reagenty o czystości na poziomie 99,999% — 99,9999% to reagenty
Do wykrywania pierwiastków w niskich stężeniach w badaniach spektrograficznych należy używać reagentów
Które równanie przedstawia reakcję otrzymywania mydła?
| CH3COOH + NaOH →CH3COONa + H2O | 2 CH3COOH + Na2O →2 CH3COONa + H2O | 2 C2H5COOH + 2 Na →2 C2H5COONa + H2↑ | C17H35COOH + NaOH →C17H35COONa + H2O |
Którą z poniższych czynności należy wykonać, aby zapewnić wysoką dokładność pomiaru masy substancji podczas przygotowywania próbki do analizy chemicznej?
W wypadku oblania skóry kwasem mrówkowym należy
| Wyciąg z karty charakterystyki Skład: kwas mrówkowy 80%, woda 11-20% Pierwsza pomoc. Po narażeniu przez drogi oddechowe. Natychmiast wezwać lekarza. Po kontakcie ze skórą. Zanieczyszczoną skórę natychmiast przemyć dużą ilością wody. |
Aparat przedstawiony na rysunku służy do
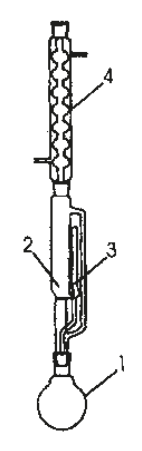
Wodę do badań mikrobiologicznych powinno się pobierać do butelek
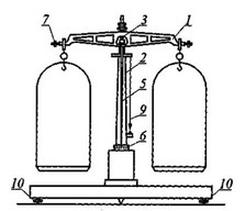
Waga przedstawiona na rysunku umożliwia ważenie substancji z dokładnością do

Intensywna reakcja z FeCl3 jest wykorzystywana do identyfikacji
Aspirator jest urządzeniem wykorzystywanym do pobierania próbek
Przebieg: Po zważeniu dwóch suchych zlewek, odważ kolejno: do jednej 3,63 g Co(NO3)2·6H2O, a do drugiej 3,75 g Na2CO3·10H2O. Następnie do obu zlewek wlej 25 cm3 gorącej wody i mieszając za pomocą bagietki doprowadź do całkowitego rozpuszczenia soli. Do roztworu Co(NO3)2 dodaj gorący roztwór Na2CO3 podczas mieszania. Otrzymany roztwór schłodź w łaźni wodnej z 3 kostkami lodu do temperatury pokojowej. Schłodzony roztwór przefiltruj przy użyciu zestawu do sączenia pod próżnią. Osad na lejku przepłucz wodą destylowaną, aż osiągnie obojętny odczyn przesączu. Przesączony osad osusz z sączkiem międzyposiadającym złożone arkusze bibuły w temperaturze pokojowej. Po wyschnięciu osad zważ i oblicz wydajność. Określ, jaki czynnik wpływa na skład jakościowy uzyskanego węglanu kobaltu(II)?
Odpady z rozpuszczalników organicznych, takich jak benzen czy aceton, zawierające co najmniej 80% danego rozpuszczalnika, należy
Aby otrzymać 200 g roztworu siarczanu(VI) sodu o stężeniu 12%, należy wykorzystać
(Na – 23 g/mol; S – 32 g/mol; H – 1 g/mol; O – 16 g/mol)
200 g soli zostało poddane procesowi oczyszczania poprzez krystalizację. Uzyskano 125 g czystego produktu. Jaką wydajność miała krystalizacja?
W wyniku rozkładu 100 g węglanu wapnia, otrzymano 25 g tlenku wapnia. Wydajność procentowa reakcji wynosi
| MCaCO3 = 100g / mol | MCaO = 56g / mol |
Jednym z sposobów oddzielania jednorodnych mieszanin jest
Aby obliczyć gęstość cieczy przy użyciu metody hydrostatycznej, należy zastosować
Co oznacza skrót AKT?
Piktogram nie jest konieczny dla
Rysunek przedstawia wagę techniczną. Numerem 7 oznaczono
Na podstawie zamieszczonych w tabeli opisów metod rozdzielania mieszanin, dobierz odpowiadające im nazwy.
| Tabela. Metody rozdzielania mieszanin | |
|---|---|
| Lp. | Opis metody |
| I. | Zlewanie cieczy znad osadu. |
| II. | Przeprowadzenie ciekłego rozpuszczalnika w stan pary. |
| III. | Wyodrębnianie z mieszaniny ciał stałych lub cieczy składnika przy pomocy rozpuszczalnika tak dobranego, aby rozpuszczał żądany związek chemiczny. |
| IV. | Powolne opadanie cząstek substancji stałej w cieczy pod wpływem własnego ciężaru. |
Aby przeprowadzać ręczną obróbkę szkła w laboratorium, konieczne jest posiadanie okularów ochronnych oraz rękawic.
Na rysunku przedstawiono urządzenie stosowane do pobierania próbek
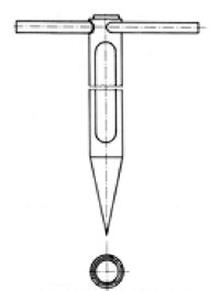
Reakcja neutralizacji wodorotlenku sodu z kwasem solnym zrealizowana jest zgodnie z równaniem:
NaOH + HCl → NaCl + H2O Masy molowe: MNaOH = 40 g/mol, MHCl = 36,5 g/mol Aby zneutralizować 10 g wodorotlenku sodu, wymagane jest
Która z metod pozwala na oddzielanie składników mieszaniny na podstawie różnic w ich zachowaniu w układzie składającym się z dwóch faz, z których jedna jest fazą stacjonarną, a druga porusza się w określonym kierunku względem niej?
Na ilustracji przedstawiono sprzęt stosowany do sączenia osadu
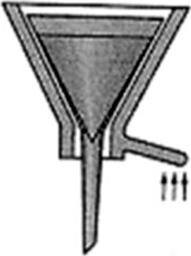
W tabeli przedstawiono wymiary, jakie powinny mieć oznaczenia opakowań substancji niebezpiecznych.
Korzystając z informacji w tabeli, określ minimalne wymiary, jakie powinno mieć oznaczenie dla cysterny o pojemności 32840 dm3.
| Pojemność opakowania | Wymiary (w centymetrach) |
|---|---|
| Nieprzekraczająca 3 litrów | co najmniej 5,2 x 7,4 |
| Ponad 3 litry, ale nieprzekraczająca 50 litrów | co najmniej 7,4 x 10,5 |
| Ponad 50 litrów, ale nieprzekraczająca 500 litrów | co najmniej 10,5 x 14,8 |
| Ponad 500 litrów | co najmniej 14,8 x 21,0 |
Technika oddzielania płynnych mieszanin, w której wykorzystuje się różnice w prędkości migracji składników przez odpowiednią bibułę, nazywa się