Pytanie 1
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
Wynik: 37/40 punktów (92,5%)
Wymagane minimum: 20 punktów (50%)
Wysoką rozdzielczość przestrzenną obrazowania MR uzyskuje się przez
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Na schemacie oznaczono
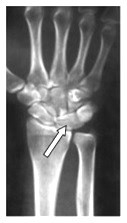
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
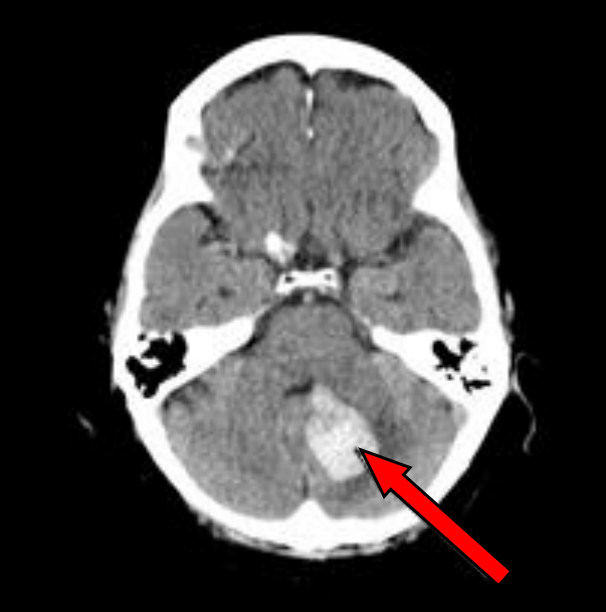
Na przekroju poprzecznym TK mózgu strzałką wskazano obszar
Droga przewodnictwa powietrznego fali akustycznej przebiega przez
Do badania mammograficznego w projekcji skośnej przyśrodkowo-bocznej kąt lampy powinien być ustawiony w zakresie
Podczas wykonywania badania EKG czarną elektrodę kończynową należy umieścić na kończynie dolnej
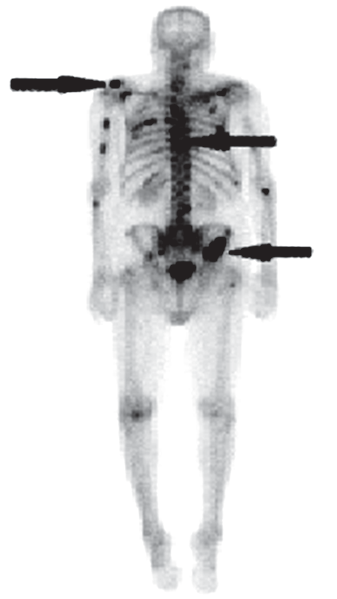
Na scyntygramie kości strzałkami oznaczono ogniska
Diagnozowanie metodą PET oparte jest na zjawisku
Który załamek odzwierciedla repolaryzację komór w zapisie EKG?
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
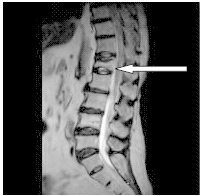
Na obrazie rezonansu magnetycznego strzałką oznaczono patologiczny kręg
Hiperfrakcjonowanie dawki w radioterapii oznacza napromienienie pacjenta
Jaka jest odległość pomiędzy źródłem promieniowania a powierzchnią ciała pacjenta w technice izocentrycznej radioterapii?
Za wyrównanie ciśnienia między uchem środkowym a otoczeniem odpowiada
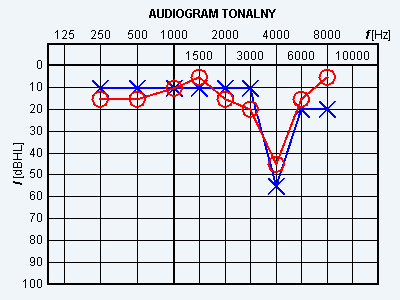
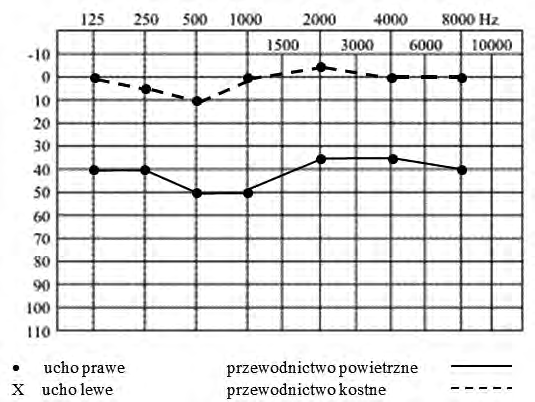
Wynik badania słuchu metodą audiometrii tonalnej wskazuje na
Parametr SNR w obrazowaniu MR oznacza
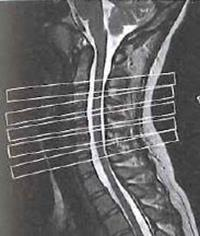
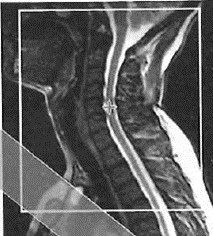
Na którym obrazie MR jest widoczne pasmo saturacji?
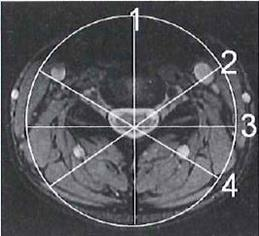

Do pomiaru dawek indywidualnych u osób narażonych zawodowo na promieniowanie rentgenowskie są stosowane
Który obszar napromieniania w radioterapii oznacza się skrótem PTV?
Wskaż przyczynę powstania artefaktu widocznego na obrazie MR.
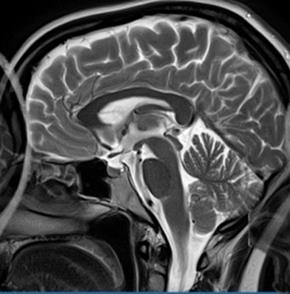
Którą strukturę anatomiczną i w jakiej projekcji uwidoczniono na radiogramie?
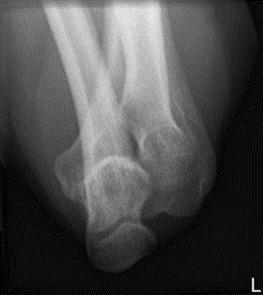
W badaniu MR czas repetycji TR jest parametrem określającym odstęp czasu między
Na jakim etapie procesu karcynogenezy dochodzi do inwazji miejscowej nowotworu i tworzenia przerzutów odległych?
Który środek ochrony radiologicznej należy zastosować podczas badania czaszki 53-letniego pacjenta za pomocą tomografii komputerowej?
Jakie są wielkości mocy dawki stosowanej w brachyterapii HDR?
Podczas teleradioterapii piersi lewej narządem krytycznym jest
Który radioizotop jest emiterem promieniowania alfa?
W których projekcjach wykonuje się standardowe badanie mammograficzne?
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Wskazaniem do wykonania badania spirometrycznego jest
Parametrem krwi, który powinien zostać oznaczony u pacjenta przed wykonaniem badania MR z kontrastem, jest
Zamieszczone obrazy związane są z badaniem
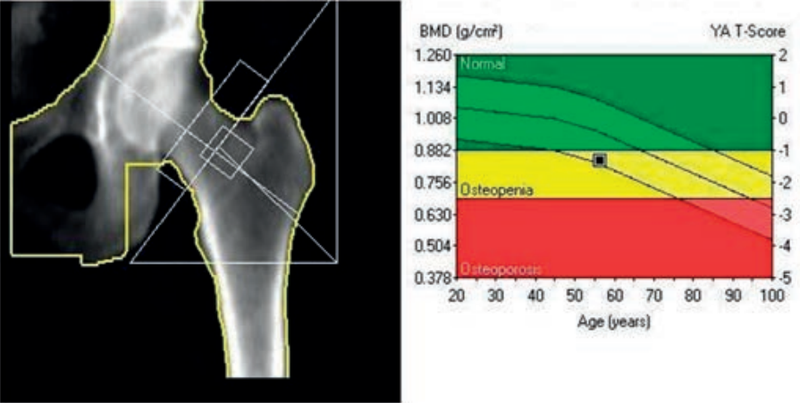
Zdjęcie zatok przynosowych wykonuje się w pozycji
Zdjęcie rentgenowskie nadgarstka w przywiedzeniu dołokciowym jest wykonywane w celu uwidocznienia kości
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
W celu oceny wieku kostnego u dziecka praworęcznego, wykonuje się pojedyncze zdjęcie w projekcji
Na podstawie zapisu badania audiometrycznego rozpoznano u pacjenta uszkodzenie słuchu
Hiperfrakcjonowanie dawki w teleradioterapii polega na napromienianiu 2 do 3 razy dziennie dawką frakcyjną