Pytanie 1
Do zmiareczkowania 30,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3 użyto KOH. Jaką masę KOH zawierała ta odważka?
MKOH = 56 g/mol
Wynik: 39/40 punktów (97,5%)
Wymagane minimum: 20 punktów (50%)
Do zmiareczkowania 30,0 cm3 roztworu HCl o stężeniu 0,1 mol/dm3 użyto KOH. Jaką masę KOH zawierała ta odważka?
MKOH = 56 g/mol
Krzywa na rysunku obrazuje miareczkowanie

W równaniu dotyczącym iloczynu rozpuszczalności siarczanu(VI) baru: Kso = [Ba2+][SO42-], jonowe stężenia Ba2+ oraz SO42- są przedstawione jako
Formy przetrwalnikowe bakterii nie obejmują
Korzystając ze wzoru, oblicz zawartość tlenu (w procentach nasycenia X) w próbce wody, jeżeli stężenie rozpuszczonego w niej tlenu wynosi 7,7 mg/dm3, a temperatura wody jest równa 284 K.
| Temperatura °C | Rozpuszczalność O2 mg/dm3 |
|---|---|
| 0 | 14,64 |
| 1 | 14,22 |
| 3 | 13,44 |
| 5 | 12,74 |
| 7 | 12,11 |
| 9 | 11,53 |
| 11 | 11,00 |
| 13 | 10,53 |
| 15 | 10,08 |
| 17 | 9,66 |
| 19 | 9,27 |
| X = a · 100% b |
| gdzie: a – oznaczona zawartość tlenu rozpuszczonego w wodzie, mg/dm3 b – rozpuszczalność O2, mg/dm3 |
Badanie tłuszczów, w tym m.in. ustalenie ilości mg KOH, potrzebnego do neutralizacji wolnych kwasów tłuszczowych znajdujących się w jednym gramie tłuszczu, dotyczy określenia liczby
Część enzymu, która nie ma budowy białkowej i jest trwale związana z jego białkowym komponentem, nosi nazwę
W tabeli przedstawiono zakresy długości fal promieniowania wykorzystywanego w spektrofotometrii Którym zakresom odpowiada podczerwień (IR), nadfiolet (UV) i światło widzialne (VIS)?
| 1 | 2 | 3 |
| 200 – 400 nm | 400 – 800 nm | 25 – 2,5 μm (4000 – 400 cm-1) |
Ile miligramów wapnia (MCa = 40,0 g/mol) znajdowało się w analizowanym roztworze, jeśli do zmiareczkowania próbki wykorzystano 20 cm3 0,0100-molowego roztworu EDTA?
Aby wykryć obecność jonów SO42- w wodzie, należy zastosować roztwór
Na rysunku przedstawiającym schemat polarymetru, cyfrą 4 oznaczono
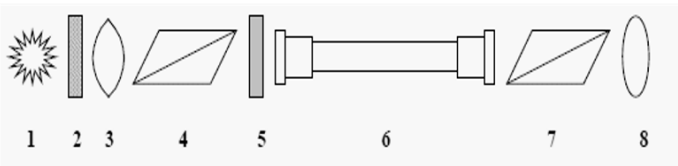
Na rysunkach przedstawiono serie pomiarów o różnej dokładności i precyzji (środek najmniejszego okręgu oznacza wartość prawdziwą). Serię pomiarów nieprecyzyjnych, ale dokładnych, przedstawiono na rysunku
Piknometr umożliwia określenie
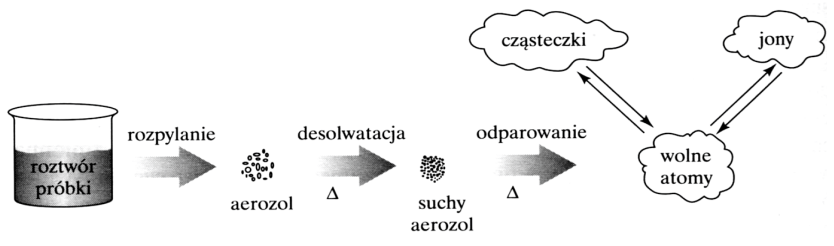
Na schemacie przedstawiono procesy, które zachodzą podczas przygotowania próbek do badań z wykorzystaniem
Dawka substancji, która powoduje pierwsze widoczne zmiany w organizmie, nazywana jest
Zjawisko zatrzymywania obcych jonów wewnątrz strącanej substancji podczas analizy wagowej określa się mianem
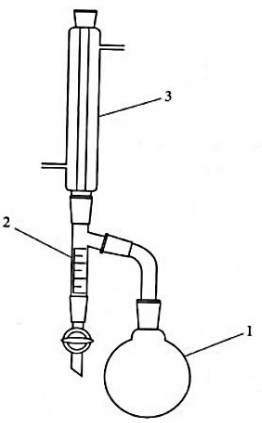
Zestaw przedstawiony na rysunku służy do oznaczania zawartości
Opis schematu:
1 - kolba okrągłodenna
2 - odbieralnik
3 - chłodnica zwrotna
W tabeli przedstawiono potencjały normalne niektórych układów redox Metodą jodometryczną pośrednią ilościowo można oznaczyć
| Układ redox | Potencjał normalny [V] |
|---|---|
| I2 + 2 e- ⟷ 2 I- | 0,55 |
| Pb2+ + 2 e- ⟷ Pb0 | -0,13 |
| Sn2+ + 2 e- ⟷ Sn0 | 0,15 |
| Bi3+ + 3 e- ⟷ Bi0 | 0,23 |
| Fe3+ + 1 e- ⟷ Fe2+ | 0,77 |
Zwiększenie efektu toksycznego jednej substancji chemicznej poprzez inną substancję, która jest jednocześnie dostarczana do organizmu, nazywa się działaniem
Podczas elektrolizy wodnego roztworu kwasu solnego na katodzie zachodzi reakcja opisana równaniem
| A. | 2 H2O + 2e− → H2 + 2 OH− |
| B. | 2 H2O + 4e− → 4H+ + O2 |
| C. | 2 Cl− → Cl2 + 2e− |
| D. | 2 H+ + 2e− → H2 |
Nie można wytworzyć roztworu mianowanego, wykorzystując jako substancję wyjściową naważkę
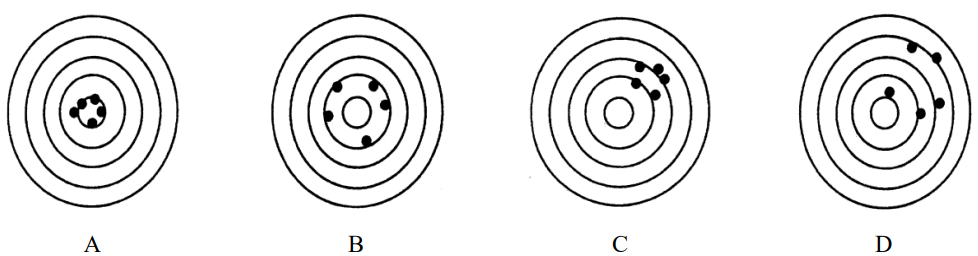
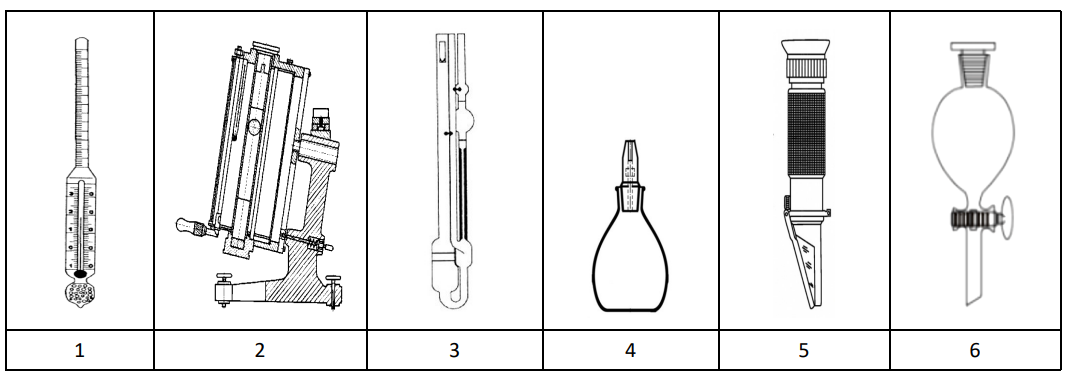
Do wyznaczania gęstości cieczy służą przyrządy oznaczone numerami
Wskaź kationy, które są możliwe do wykrycia poprzez próbę płomieniową?
Przeprowadzono orientacyjną ocenę jakości mikrobiologicznej mleka w tak zwanej próbie azotanowej, która zabarwiła się na kolor bladoróżowy, co znaczy, że jakość mleka wziętego do analizy była
| Zabarwienie próbki mleka | Ocena jakości próbki Mleko: |
|---|---|
| bez zmiany barwy | bardzo dobre i dobre |
| lekko lub wyraźnie różowa | średniej jakości |
| intensywnie różowa, czerwona lub brunatna | złej jakości |
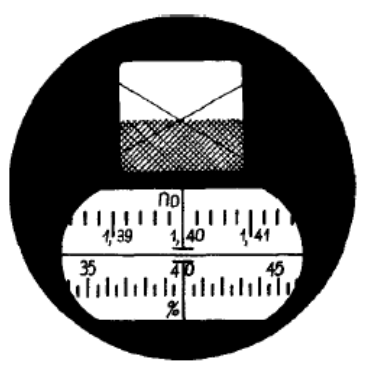
Na rysunku przedstawione jest pole widzenia
W mikrobiologii metoda sterylizacji przy użyciu suchego, gorącego powietrza zalicza się do
Na ilustracji przedstawiono schemat

Który zbiór zawiera jedynie odczynniki grupowe używane w analizie jakościowej jonów?
Który ze związków będzie barwny w świetle widzialnym?
Na rysunku pokazano efekt reakcji chemicznej, polegającej na dodaniu do badanego roztworu jonów żelaza (II) w obecności stężonego kwasu siarkowego(VI). Reakcja ta jest stosowana w celu wykrywania jonów

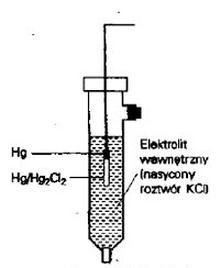
Który rodzaj elektrody odniesienia przedstawiono na rysunku?
Podłoże wykorzystywane do uzyskiwania hodowli o dużej liczbie drobnoustrojów danego szczepu nazywa się
Na rysunku przedstawiono wykonanie analizy metodą
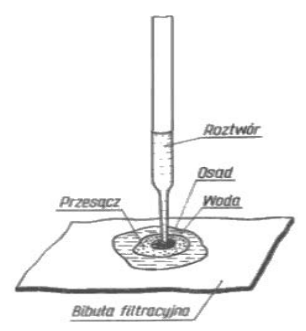
Zjawisko alkalizacji gleby jest spowodowane
W celu wykonania analizy mieszaniny kationów grup I - V należy wybrać sprzęt oznaczony w tabeli numerami:
| Palnik gazowy | Kolba stożkowa | Drut platynowy na pręcie szklanym | Biureta | Płytka ceramiczna do eksperymentów kroplowych | Kolba miarowa |
| 1 | 2 | 3 | 4 | 5 | 6 |
Wskaż błędnie określone efekty reakcji analitycznych kationów I grupy.
| Odczynnik strącający | Reakcje analityczne | |||
|---|---|---|---|---|
| Ag+ | Hg22+ | Pb2+ | ||
| A. | HCl | biały osad AgCl rozpuszczalny w NH3·H2O | biały osad Hg2Cl2 | biały osad PbCl2 rozpuszczalny w gorącej wodzie |
| B. | H2SO4 | biały Ag2SO4 (ze stężonych roztworów), rozpuszczalny w gorącej wodzie | biały osad Hg2SO4 rozpuszczalny w wodzie królewskiej | biały osad PbSO4 rozpuszczalny w roztworze NaOH |
| C. | NaOH | brunatny osad Ag2O rozpuszczalny w NH3·H2O | czarny osad HgO i Hg | biały osad Pb(OH)2 rozpuszczalny w roztworze NaOH |
| D. | NH3aq | brunatny jon kompleksowy Ag(NH3)2+ | biały osad soli amidortęciowej rozpuszczalny w stężonym HNO3 | żółty osad Pb(OH)2 rozpuszczalny w gorącej wodzie |
Na ilustracji przedstawiono poszczególne etapy wykonania preparatu mikroskopowego utrwalonego. Cyfrą 3 oznaczono
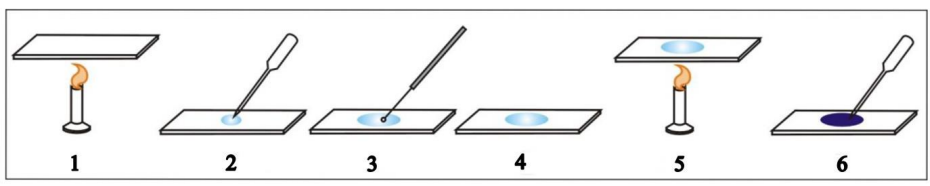
Jakie jest zastosowanie metody Winklera?
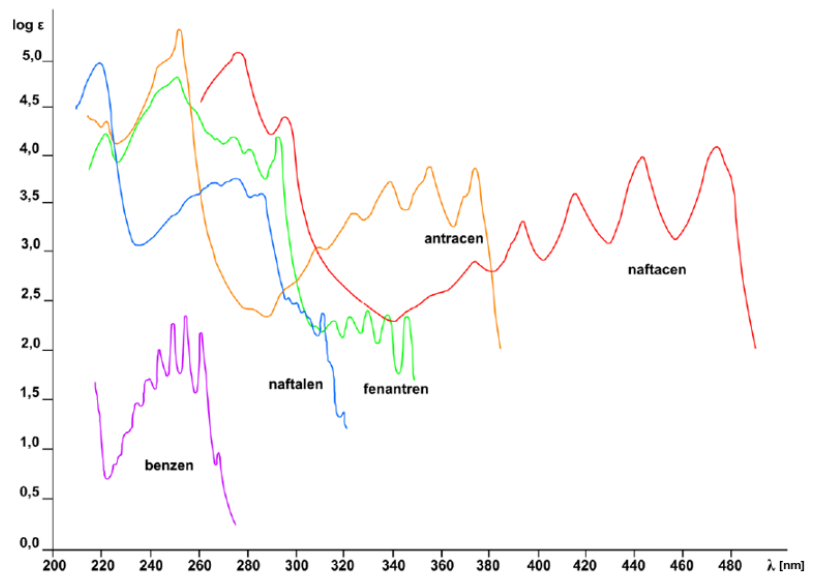
Która z przedstawionych na wykresie długości fali widma absorpcyjnego jonów MnO4- powinna być stosowana jako długość analityczna?
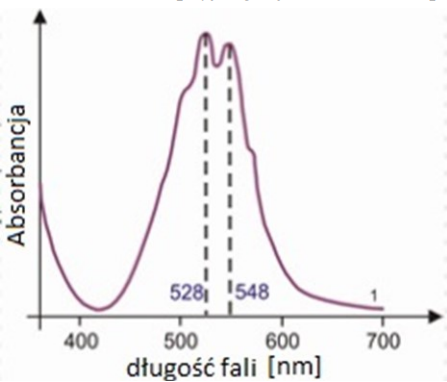
Gdzie wykorzystuje się efekt Tyndalla?