Pytanie 1
SPECT to
Wynik: 27/40 punktów (67,5%)
Wymagane minimum: 20 punktów (50%)
SPECT to
Zgodnie z obowiązującymi przepisami powierzchnia gabinetu rentgenowskiego, w którym jest zainstalowany zestaw rentgenowski do badań naczyniowych, powinna wynosić
W obrazowaniu metodą rezonansu magnetycznego T1 oznacza czas
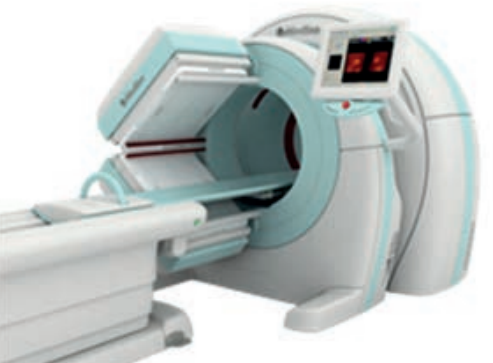
Które urządzenie zostało przedstawione na fotografii i w jakiej pracowni znajduje zastosowanie?
Standardowo do wykonania których zdjęć należy zastosować kratkę przeciwrozproszeniową?
Jaka jest standardowa odległość OF do wykonania rentgenowskich zdjęć kości i stawów kończyny górnej?
Proces chemicznego wywoływania radiogramów polega na
Jakie wiązki promieniowania emituje medyczny akcelerator liniowy?
Obrazy DDR są tworzone w trakcie
Nieostrość geometryczna obrazu rentgenowskiego zależy od
Ile razy i jak zmieni się wartość natężenia promieniowania X przy zwiększeniu odległości OF ze 100 cm do 200 cm?
Testy podstawowe z zakresu geometrii pola rentgenowskiego, przeznaczone do sprawdzenia zgodności pola wiązki promieniowania rentgenowskiego z symulacją świetlną, są wykonywane raz
Jednostką indukcji magnetycznej jest
Gadolin jako dożylny środek kontrastowy stosowany w MR powoduje
W pracowni radioterapii wyświetlenie na ekranie monitora aparatu komunikatu „ROTATION” oznacza prowadzoną terapię
Pracownia radioterapii z przyspieszaczem liniowym jest obszarem
Emisja fali elektromagnetycznej występuje w procesie rozpadu promieniotwórczego
Jak określa się rekonstrukcję obrazów TK, której wynikiem są obrazy dwuwymiarowe tworzone w dowolnej płaszczyźnie przez wtórną obróbkę zestawionych ze sobą wielu przekrojów poprzecznych?
Zadaniem technika elektroradiologa w pracowni naczyniowej jest
W celu wyeliminowania zakłóceń obrazu MR przez sygnały pochodzące z tkanki tłuszczowej, stosuje się
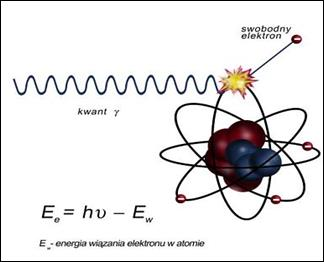
Na ilustracji przedstawiono zjawisko
W badaniu PET stosuje się tylko radioizotopy emitujące
Ligand stosuje się
Brachyterapia polegająca na wielokrotnym wsuwaniu i wysuwaniu źródła promieniowania do tego samego aplikatora nosi nazwę
Która metoda diagnostyczna służy do określenia gęstości minerału kostnego w ujęciu objętościowym g/cm³?
Zastosowana w badaniu radiologicznym kratka przeciwrozproszeniowa powoduje
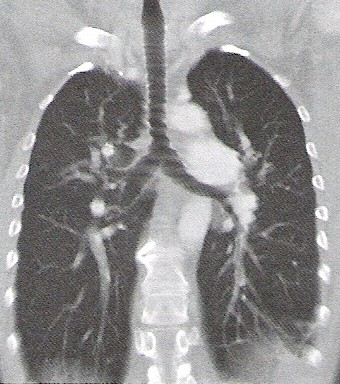
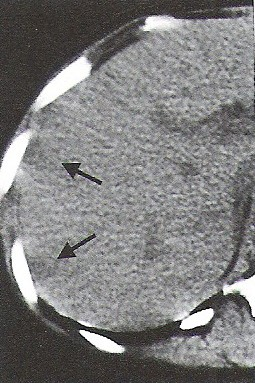
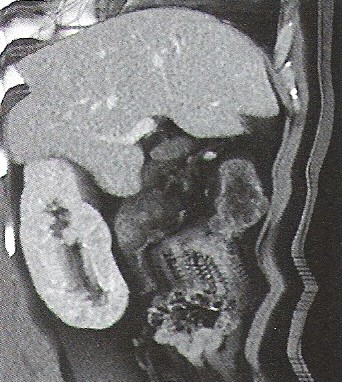
Na którym obrazie TK uwidoczniony jest artefakt spowodowany ruchami oddechowymi pacjenta?

Hiperfrakcjonowanie dawki w radioterapii oznacza napromieniowywanie pacjenta
Który detektor w radiografii wymaga laserowego czytnika obrazu?
W technice napromieniania SSD mierzona jest odległość źródła promieniowania
Promieniowanie rentgenowskie powstaje w wyniku hamowania
Z kratką przeciwrozproszeniową należy wykonać zdjęcie
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Brachyterapia polega na napromieniowaniu pacjenta promieniowaniem
Wiązka elektronów najczęściej stosowana jest do leczenia zmian nowotworowych w obrębie
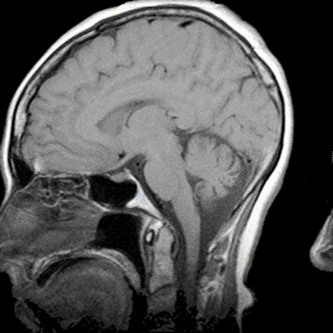
Który artefakt uwidoczniono na skanie RM głowy?
Teleradioterapia 4D na etapie planowania leczenia wykorzystuje obrazy
Źródłem promieniowania protonowego stosowanego w radioterapii jest
W radioterapii hadronowej leczenie odbywa się przy użyciu
W której technice brachyterapii stosuje się źródła promieniowania o mocy dawki 2-12 Gy/h?