Pytanie 1
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
Wynik: 36/40 punktów (90,0%)
Wymagane minimum: 20 punktów (50%)
W lampie rentgenowskiej promieniowanie X powstaje w wyniku hamowania
Fala głosowa rozchodzi się
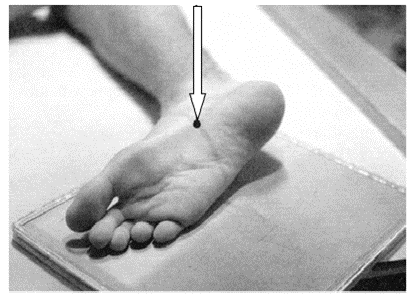
Na zamieszczonej ilustracji przedstawiono ułożenie pacjenta do wykonania zdjęcia rentgenowskiego
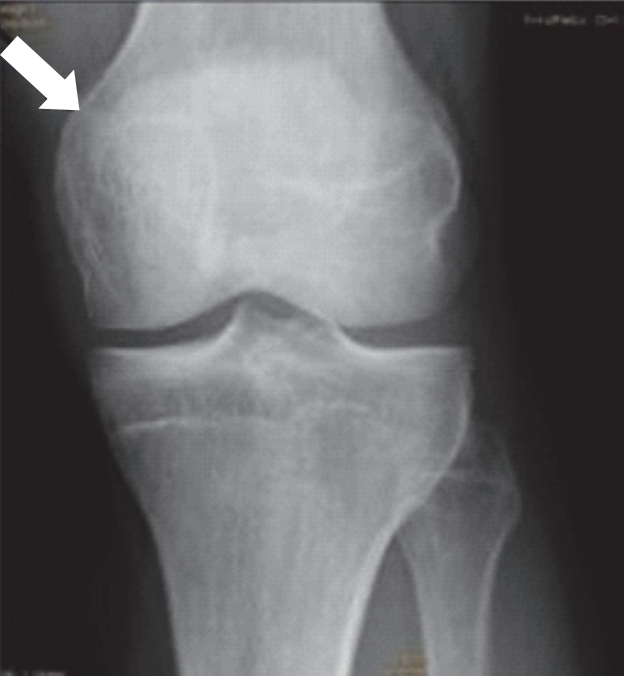
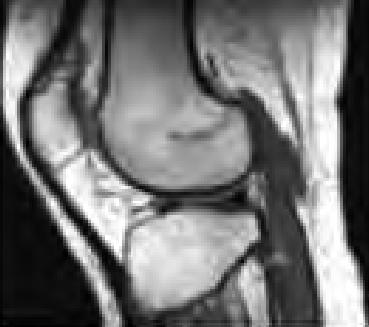
Którą strukturę anatomiczną zaznaczono na radiogramie stawu kolanowego?
Pozytywny środek cieniujący najczęściej stosowany w rentgenodiagnostyce powinien charakteryzować się
Wskaż roczną dawkę graniczną dla osób zatrudnionych w warunkach narażenia na promieniowanie jonizujące.
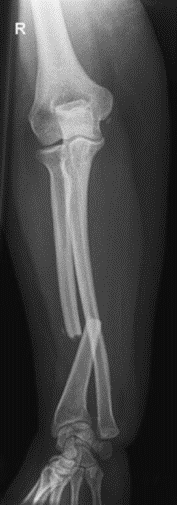
Na radiogramie uwidoczniono złamanie
W ułożeniu do rentgenografii AP stawu kolanowego promień główny pada
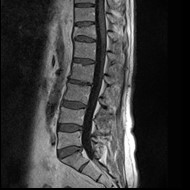
Na obrazie uwidoczniono złamanie kompresyjne kręgu
Podczas wykonywania zdjęcia rentgenowskiego lewobocznego czaszki promień centralny powinien przebiegać
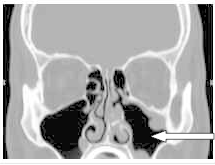
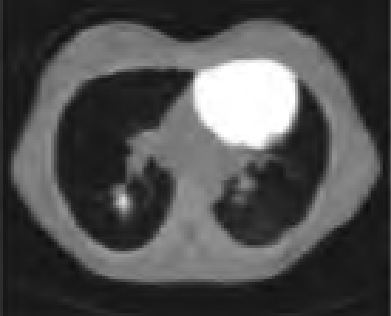
Na obrazie TK zaznaczono zatokę
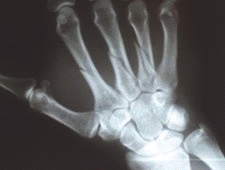
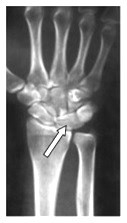
Na obrazie radiologicznym nadgarstka strzałką zaznaczona jest kość
Obszary napromieniania w technice IMRT w trakcie wykonywania zabiegu radioterapeutycznego wyznacza
Bezwzględnym przeciwwskazaniem do badania spirometrycznego jest
Kryterium rozpoznawczym dla fali δ (delta) w badaniu EKG jest
W jakiej pozycji układa się pacjenta do standardowego badania MR kręgosłupa szyjnego?
Chorobą układu oddechowego typu obturacyjnego jest
Na radiogramie uwidoczniono złamanie
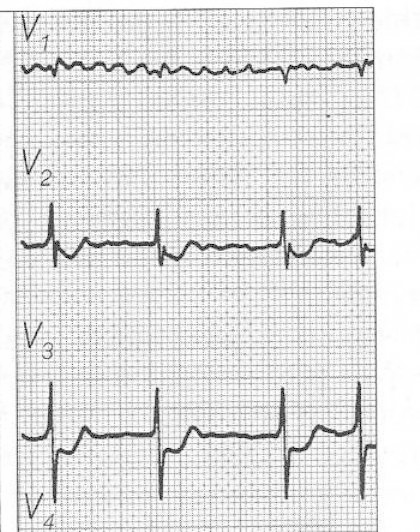
Zamieszczony elektrokardiogram przedstawia
Jak oznacza się w radioterapii obszar tkanek zawierający GTV i mikrorozsiewy w fazie niewykrywalnej klinicznie?
Które środki kontrastujące wykorzystywane są w diagnostyce rezonansem magnetycznym?
Do prób aktywacyjnych stosowanych w badaniu EEG zalicza się
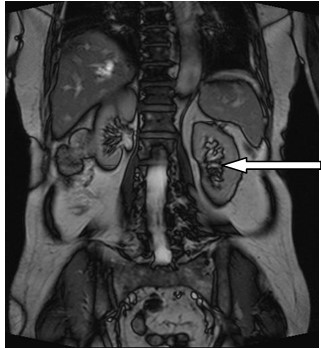
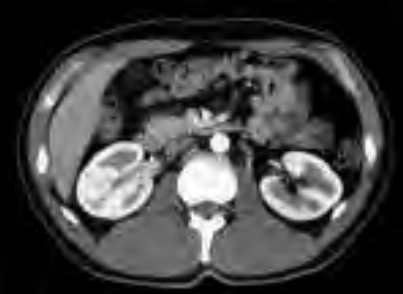
Który narząd został oznaczony strzałką na obrazie rezonansu magnetycznego?
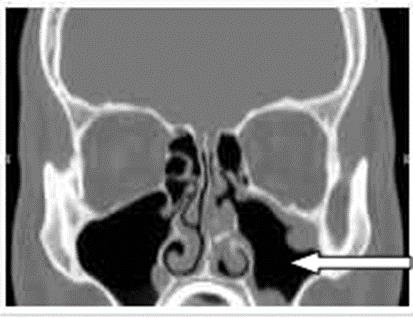
Na zamieszczonym obrazie TK strzałką zaznaczono zatokę
W scyntygrafii kośćca „ogniska gorące” oznaczają miejsca
Czas repetycji w obrazowaniu metodą rezonansu magnetycznego to
Zamieszczone badanie elektrokardiograficzne wykazało u pacjenta
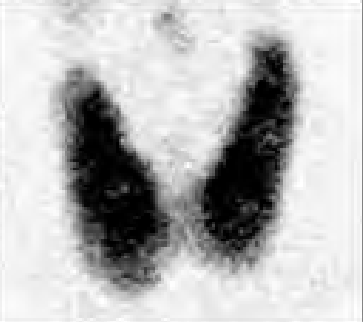
Na którym obrazie zarejestrowano badanie scyntygraficzne?
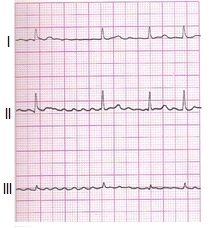
W zapisie EKG linia izoelektryczna obrazuje
W leczeniu izotopowym tarczycy należy podać
Parametr spirometryczny czynnościowa pojemność zalegająca oznaczany jest skrótem
Pomiaru impedancji akustycznej ucha środkowego dokonuje się podczas badania
Ultrasonograficzne środki kontrastowe to
Zgodnie z procedurą wzorcową w badaniu MR należy ułożyć pacjenta na brzuchu do diagnostyki
Która sekwencja obrazowania MR wykorzystuje impulsy RF o częstotliwości rezonansowej tłuszczu do tłumienia sygnału pochodzącego z tkanki tłuszczowej?
Do czego służy do symulator rentgenowski wykorzystywany w procesie radioterapii?
Który z nowotworów jest hormonozależny?
W celu unieruchomienia okolicy badanej podczas wykonywania zdjęcia nadgarstka u osoby dorosłej należy zastosować
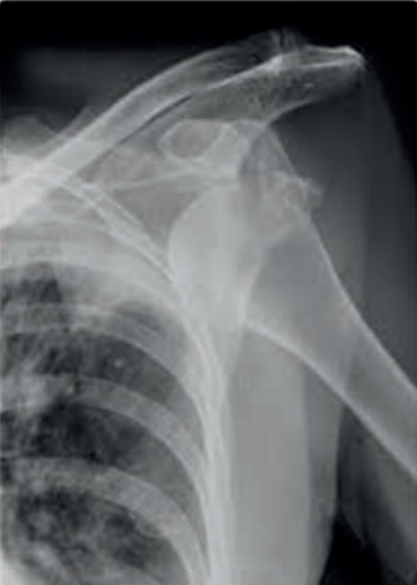
Którą patologię uwidoczniono na zamieszczonym rentgenogramie?
Hałas podczas badania tomografii rezonansu magnetycznego jest efektem ubocznym pracy